Lukas Schwingshackl
Universitatea din Viena, Facultatea de Științe ale Vieții, Departamentul de Științe Nutritive, Viena, Austria,
Georg Hoffmann
Universitatea din Viena, Facultatea de Științe ale Vieții, Departamentul de Științe Nutritive, Viena, Austria,
Conceput și proiectat experimentele: LS GH. Au efectuat experimentele: LS GH. Analiza datelor: LS GH. Reactivi/materiale/instrumente de analiză contribuite: LS GH. Contribuție la scrierea manuscrisului: LS GH.
Date asociate
Autorii confirmă că toate datele care stau la baza constatărilor sunt pe deplin disponibile fără restricții. Toate datele sunt incluse în manuscris și în fișierele cu informații de susținere.
Abstract
fundal
Obiectivul prezentei revizuiri sistematice și meta-analizei a fost investigarea efectelor dietelor bogate în proteine (HP) versus dietele normale/scăzute de proteine (LP/NP) asupra parametrilor funcției renale la subiecții fără afecțiuni renale cronice.
Metode
Interogări de literatură au fost efectuate utilizând bazele de date electronice MEDLINE, EMBASE și Registrul de încercări Cochrane până la 27 februarie 2014. Diferențele medii specifice ponderate ale studiului (MD) au fost combinate utilizând un model de efect aleatoriu de pachetul software Cochrane Review Manager 5.1.
Constatări
Metode
Surse de date și căutări
Interogări de literatură au fost efectuate utilizând bazele de date electronice MEDLINE (până la 27 februarie 2014), EMBASE (până la 27 februarie 2014) și Registrul de studii Cochrane (până la 27 februarie 2014) cu restricții la studiile controlate randomizate, dar fără restricții la limba și data calendaristică folosind următorul termen de căutare: ("proteină") ȘI ("renal" SAU "rinichi" SAU "filtrare glomerulară" SAU "creatinină" SAU "uree" SAU "albumină" SAU "calciu"). Mai mult, listele de referințe din articolele recuperate au fost verificate pentru a căuta alte studii relevante. Această revizuire sistematică a fost planificată, efectuată și raportată în conformitate cu standardele de calitate pentru raportarea meta-analizelor [14]. Căutarea literaturii a fost efectuată independent de ambii autori, cu dezacordurile soluționate prin consens.
Selectarea studiului
Studiile au fost incluse în meta-analiză dacă au îndeplinit toate criteriile următoare: (i) proiectare randomizată controlată sau încrucișată; (ii) perioada minimă de intervenție de 1 săptămână; (iii) compararea unei intervenții dietetice HP cu o intervenție NP/LP (folosind o diferență de 5% în aportul total de energie, așa cum a fost definit anterior de Santesso și colab. 2012 [1]), care au fost proiectate sau nu pentru scăderea în greutate; (iv) vârsta: ≥ 18 ani; (v) mărimea eșantionului: sănătos, supraponderal, obez, diabet de tip 2 (T2D); (vi) evaluarea markerilor „rezultatului interesului”: GFR, creatinină serică, uree serică, excreție urinară de calciu, excreție urinară de albumină, acid uric seric, pH urinar; (vii) raportul valorilor medii post-intervenție (dacă nu este disponibil, s-au utilizat modificări de la valorile de bază) cu deviație standard (sau date de bază pentru calcularea acestor parametri: eroare standard, interval de încredere 95%, valori p) . Dacă datele studiilor în curs au fost publicate ca actualizări, au fost incluse doar rezultatele perioadelor cu cea mai lungă durată. Au fost excluse studiile care au înscris subiecți cu BCR (GFR 2), diabet de tip 1 și macroalbuminurie. Studiile au fost incluse dacă subiecții au avut microalbuminurie, deoarece datele din NHANES III au indicat că 12% din populația inclusă suferea de microalbminurie, în timp ce doar 1,5% au avut macroalbuminurie [15].
Extragerea datelor și evaluarea calității
Instrumentul de evaluare a riscului de prejudecată de către Cochrane Collaboration a fost aplicat specificând următoarele domenii de prejudecată: prejudecată de selecție (generare aleatorie de secvențe, ascundere a alocării), performanță/distorsiune de detectare (orbire a participanților și a personalului/orbire a evaluării rezultatului), rezoluție date ) și tendința de raportare (raportare selectivă) [16] (Figura S1).
Următoarele date au fost extrase din fiecare studiu: numele primului autor, anul publicării, lungimea studiului, distribuția și vârsta sexului, IMC,% diabetici, mărimea eșantionului, aportul de proteine (% din conținutul total de energie, TEC sau g * kg corp greutatea -1 * d -1), proveniența proteinelor, aportul de calciu, conținutul de energie din dietele HP și NP/LP, rezultatele și valorile medii post sau diferențele dintre cele două valori ale punctelor de timp cu abaterea standard corespunzătoare.
Sinteza și analiza datelor
Caracteristicile studiilor și participanților
Toate studiile incluse în această revizuire sistematică au fost ECR cu o durată cuprinsă între 1 săptămână și 24 de luni, publicate între 1993 și 2013 și care au înscris un total de 2160 de participanți. Toate studiile au comparat o dietă HP cu un regim NP/LP. Vârsta medie a participanților a variat între 22,3 și 67 de ani. Aporturile de proteine din grupurile HP au fost în mare parte de origine animală, cu excepția unui studiu, în care a fost utilizată proteina din gluten din grâu [20]. Caracteristicile generale ale studiului sunt date în Tabelul 1 .
tabelul 1
Rezultate
Estimările cumulate ale mărimii efectului efectelor HP în comparație cu NP/LP asupra rezultatelor funcției renale sunt rezumate în Tabelul 2. Modificările creatininei serice (Figura S3), excreția de albumină urinară (Figura S5), acidul uric (Figura S4) și pH-ul urinar (Figura S7) nu au fost semnificativ diferite după dietele HP comparativ cu dietele NP/LP și sunt date ca Suplimentare material.
masa 2
| Rezultate | Nu. de Studii | Marime de mostra | MD | IC 95% | valorile p | Inconsistență I 2 |
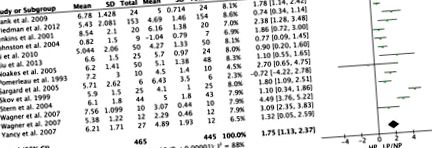
| GFR (ml/min/1,73 m 2) | 21 | 1599 | 7.18 | [4.45, 9.91] | 2 (IC 95% 4,45-9,91), p Figura 1). Uree serică [MD: 1,75 mmol/l (IÎ 95% 1,13 până la 2,37), p Figura 2) și excreția urinară de calciu [MD: 25,43 mg/24h (IÎ 95% 13,62 până la 37,24), p 2) din 21 HP controlate randomizat trasee dietetice. |
Pentru fiecare studiu cu conținut ridicat de proteine, pătratul umbrit reprezintă estimarea punctuală a efectului de intervenție. Linia orizontală unește limitele inferioară și superioară ale CI 95% din aceste efecte. Zona pătratului umbrit reflectă greutatea relativă a studiului în metaanaliza respectivă. Diamantul din partea de jos a graficului reprezintă MD combinat cu CI de 95%. HP, bogat în proteine; NP/LP, proteine normale/proteine scăzute.
Pentru fiecare studiu cu conținut ridicat de proteine, pătratul umbrit reprezintă estimarea punctuală a efectului de intervenție. Linia orizontală unește limitele inferioară și superioară ale CI 95% din aceste efecte. Zona pătratului umbrit reflectă greutatea relativă a studiului în metaanaliza respectivă. Diamantul din partea de jos a graficului reprezintă MD combinat cu CI de 95%. HP, bogat în proteine; NP/LP, proteine normale/proteine scăzute.
Analize de sensibilitate
Includerea ECR care investighează numai subiecți fără T2D (18 studii) a confirmat rezultatele sau meta-analiza primară (Tabelul S1). Mai mult, cu excepția pH-ului urinar (doar 1 studiu) și a excreției urinare de calciu (5 studii), principalele rezultate ar putea fi confirmate atunci când sunt incluse doar subiecții obezi (20 de studii) (Tabelul S2). Observații similare ar putea fi făcute pentru studiile pe termen lung (≥ 12 săptămâni, 17 studii) (Tabelul S3). Analiza sensibilității incluzând doar subiecții T2D a dus la observații similare (Tabelul S4). În urma excluderii procesului de către Jenkins și colab. [20] (fiind singurul RCT care nu utilizează proteina animală ca sursă de suplimentări în protocoalele HP), dietele HP au dus la o creștere semnificativ mai pronunțată a acidului uric în comparație cu protocoalele NP/LP.
Bias de publicare
Graficele de pâlnie (în ceea ce privește modificările dimensiunii efectului pentru markerii sănătății rinichilor ca răspuns la dietele HP, respectiv) indică o asimetrie mică până la moderată, sugerând că prejudecata publicării nu poate fi complet exclusă ca factor de influență asupra meta-analizei actuale (Figura S8-S14). Rămâne posibil ca studiile mici care furnizează date neconcludente să nu fi fost publicate sau să nu fi reușit să facă acest lucru.
Heterogenitate
S-a găsit o eterogenitate considerabilă în ceea ce privește ureea serică (I 2 = 88%), pH urinar (I 2 = 95%) și excreția urinară de calciu (I 2 = 90%) (Tabelul 2). S-a presupus că eterogenitatea ridicată ar putea fi explicată prin caracteristici de studiu neuniforme în grupurile cu proteine ridicate, cum ar fi variațiile de vârstă, IMC, lungimea studiului și aportul de proteine. Pentru a obține o perspectivă asupra acestor corelații potențiale, a fost efectuată o meta-regresie cu efecte aleatorii pentru a examina asocierile dintre parametrii grupului HP și NP/LP și modificările GFR, creatininei serice, ureei serice, acidului uric, albuminei urinare și pH-ului urinar, respectiv. O relație doză-răspuns statistic semnificativă ar putea fi detectată între aportul de proteine și creșterea ureei serice (p = 0,023) Nu s-au putut detecta astfel de corelații între alte caracteristici ale studiului și parametrii menționați.
Discuţie
Scopul prezentei meta-analize a fost de a investiga impactul HP vs. Dietele LP/NP privind parametrii funcției renale la subiecții fără o BCR stabilită. Principalele constatări sugerează că subiecții care urmează o dietă HP s-au prezentat cu GFR crescut, uree serică și, respectiv, excreție urinară de calciu. Creșteri suplimentare ale concentrațiilor serice de acid uric ar putea fi observate la acei indivizi care urmează un regim HP, atunci când studiul lui Jenkins și colab. [20] a fost exclus din analiză datorită faptului că a fost singurul studiu care utilizează proteine vegetale exclusiv ca supliment.
Acum aproximativ 30 de ani, Brenner și colab. [24] a exprimat ipoteza că o creștere a GFR și a presiunii glomerulare ar putea provoca disfuncții renale și crește riscul de leziuni renale. Deși această ipoteză nu a putut fi validată și nici respinsă până în prezent, s-ar putea argumenta că consumurile de HP pe termen lung exercită efecte dăunătoare asupra funcției renale, provocând hiperfiltrare renală. În ceea ce privește mecanismul care mediază GFR crescut, Frank și colab. [25] a emis ipoteza că încărcătura de proteine induce un răspuns vasodilatator care duce la hiperemie. Într-o meta-analiză a 14 studii observaționale care au înscris 105.872 de participanți, o GFR> 105 ml/min/1,73 m 2 a fost asociată cu un risc crescut de mortalitate din toate cauzele [26]. Cu toate acestea, autorii acestui studiu au afirmat că concluziile lor ar trebui interpretate conservator. În loc să fie o reacție fiziopatologică, modificările induse de HP în funcția rinichilor, cum ar fi creșterea GFR, ar putea reprezenta, de asemenea, un proces de adaptare fiziologică [27], [28]. Capacitatea rinichiului de a crește nivelul funcțional cu aportul de proteine sugerează o rezervă de funcție renală [29].
Reducerile pH-ului urinar (p = 0,07), observate în această meta-analiză pentru dietele HP, sunt considerate ca un factor de risc independent pentru nefrolitiază [7]. În plus, aportul de HP a crescut excreția urinară de calciu, care este o caracteristică comună la pacienții cu pietre calcaroase [36], [37]. Afectarea homeostaziei calciului poate duce la scăderea densității minerale osoase. Cu toate acestea, datele clinice și epidemiologice nu susțin conceptul că dietele HP exercită efecte dăunătoare asupra sănătății osoase. [1], [38] Mai mult, diferențele observate în prezenta meta-analiză nu par a fi relevante clinic.
Două metaanalize, inclusiv studii observaționale, au arătat că supraponderalitatea, obezitatea și sindromul metabolic cresc riscul bolilor renale cu 40 până la 83% [39], [40]. Având în vedere că aproximativ două treimi din studiile incluse în prezenta meta-analiză înregistrau subiecți obezi, s-ar putea specula că un aport ridicat de proteine va adăuga un alt factor dăunător riscului crescut de disfuncție renală deja stabilit pentru această populație. Conform recomandărilor Asociației Americane a Diabetului, pacienții cu T2D nu ar trebui să se refere la dietele HP ca mijloc de scădere în greutate din cauza efectelor necunoscute pe termen lung ale aporturilor de proteine> 20% din TEC [41].
Limitări
În ceea ce privește validitatea parametrului principal de rezultat GFR, ecuațiile de estimare bazate pe creatinină utilizate în studiile incluse în această analiză sistematică sunt cunoscute ca având unele limitări în ceea ce privește precizia, precum și fiind afectate de variațiile aportului de proteine, care ar putea fi agravată de faptul că populația studiată nu suferea de boli renale cronice manifestate. Astfel, efectele GFR observate în prezenta meta-analiză trebuie interpretate într-un mod conservator, deoarece valorile crescute ale creatininei s-ar traduce într-un GFR estimat mai mic [42]. Un studiu transversal realizat de Inker și colab. a arătat că cistatina C ar putea reprezenta un marker mai util pentru estimarea RFG mai ales atunci când este combinată cu creatinina [43]. Mai mult, o analiză post hoc a studiului „Modificarea dietei și a bolilor renale” (originea eGFR pe baza creatininei serice) a arătat că proteinele din dietă au redus modificarea creatininei, dar nu au afectat semnificativ modificările cistatinei C [44].
În concluzie, dietele HP au fost asociate cu GFR crescut, uree serică, excreție urinară de calciu și concentrații serice de acid uric. Majoritatea acestor modificări ar putea fi interpretate ca un mecanism adaptiv fiziologic indus de dieta HP fără nicio relevanță clinică. Cu toate acestea, având în vedere faptul că BCC subclinică este foarte răspândită și că obezitatea este asociată cu boli de rinichi, programele de reducere a greutății recomandă dietele HP, în special din surse animale, care trebuie tratate cu precauție.
informatii justificative
Figura S1
Instrument de evaluare a riscului de prejudecată.
- Frecvența mesei atât la restaurantele fast-food, cât și la cele relaxate a fost asociată cu corpul ridicat
- Ar putea modul în care trăiesc oamenii înalte să-și afecteze greutatea NHS
- Ar putea cum trăiesc oamenii înalți să le afecteze greutatea NI
- Altitudine mare ar putea vindeca obezitatea ABC News
- Comparație de recenzii pentru rețete de supe pentru arderea grăsimilor; Evaluare