Abstract
fundal
Cistinuria este o tulburare moștenită a transportului renal de aminoacizi care provoacă nefrolitiază recurentă și morbiditate semnificativă la om. Are o incidență de 1 din 7000 la nivel mondial, făcându-l una dintre cele mai frecvente tulburări genetice la om. Am caracterizat fenotipic un model de șoarece de cistinurie de tip A rezultat din eliminarea Slc3a1.
Metode
Knockout de Slc3a1 la nivelurile de ARN și proteine a fost evaluat utilizând PCR cantitativă în timp real și imunofluorescență. Slc3a1 șoarecii knockout au fost plasați pe diete normale sau de crescător și au fost evaluați pentru formarea de pietre de cistină în timp, urmărind analiza cu raze X și dezvoltarea leziunilor renale prin măsurarea biomarkerilor de leziuni. Leziunea renală a fost, de asemenea, evaluată prin analize histologice. Nivelurile de aminoacizi au fost măsurate în sângele șoarecilor folosind cromatografie lichidă de înaltă performanță. Nivelurile de glutation hepatic au fost măsurate folosind un test pe bază de luminiscență.
Rezultate
Am confirmat eliminarea meciului Slc3a1 la nivel de ARN, în timp ce Slc7a9 ARN reprezentând co-transportorul a fost păstrat. După cum era de așteptat, am observat formarea pietrei vezicii urinare în Slc3a1 -/- șoareci. Masculin Slc3a1 -/- șoarecii au prezentat greutăți mai mici comparativ cu Slc3a1 +/+ . Slc3a1 -/- șoarecii care au urmat o dietă regulată au demonstrat creșterea azotului ureic din sânge (BUN) fără creșterea creatininei serice. Cu toate acestea, plasarea animalelor knockout pe o dietă de crescător, care conține o concentrație mai mare de cistină, a dus la dezvoltarea creșterii atât a BUN cât și a creatininei, care indică o boală cronică renală mai severă. Examenul histologic a arătat că aceste efecte dietetice au condus la agravarea obstrucției tubulare a rinichilor și a inflamației interstițiale, precum și la agravarea inflamației vezicii urinare. Cistina este un precursor al moleculei antioxidante glutation, deci am evaluat nivelurile de glutation în ficatul Slc3a1 -/- șoareci. Am găsit niveluri semnificativ reduse atât de glutation, cât și de glutation total la animalele eliminate.
Concluzii
Rezultatele noastre sugerează că dieta poate afecta dezvoltarea și progresia bolii renale cronice la un model animal de cistinurie, care poate avea implicații importante pentru pacienții cu această boală. În plus, glutationul redus îi poate predispune pe cei cu cistinurie la leziuni cauzate de stresul oxidativ.
fundal
Au fost generate modele de șoarece de cistinurie de tip I. Peters și colab. a identificat o mutație cu sens greșit Slc3a1 într-un ecran de mutageneză N-etil-N-nitrozourea (ENU) la șoareci C3HeB/FeJ [8]. Autorii au demonstrat o greutate redusă a rinichilor la bărbații homozigoti în comparație cu bărbații de tip sălbatic și femelele homozigote. În plus, nivelurile de uree plasmatică au fost crescute la bărbații homozigoti de la 13 la 20 de săptămâni în comparație cu animalele de tip sălbatic. Livrozet și colab. a identificat o mutație spontană în Slc3a1 la șoarecii 129SvPasCrl rezultând cistinurie [9]. Funcția renală nu a fost afectată semnificativ la șoarecii mutanți, măsurată prin măsurători ale creatininei serice. Cu toate acestea, au observat macrofage crescute și fibroză interstițială la șoarecii mutanți. Ercolani și colab. a demonstrat obstrucție la ieșirea vezicii urinare la șoareci masculi de cistinurie pe un backround mixt C57Bl/6 și 129/SvJ [10]. A fost raportată strategia genetică pentru generarea acestei linii de șoarece cistinurie [11]; cu toate acestea, am căutat să caracterizăm mai complet această tulpină de șoarece de cistinurie.
Metode
Animale
Slc3a1 -/- și șoareci de tip sălbatic (mascul și femelă) au fost crescuți și întreținuți așa cum s-a descris anterior și conform Comitetului instituțional de îngrijire și utilizare a animalelor din Nashville Tennessee Valley Healthcare System VA și Vanderbilt University Medical Center [10, 11]. Dietele normale și de crescător au fost obținute din Lab Diet (St. Louis, MO), cu 5L0D corespunzător normalului și 5LJ5 crescătorului. Șoarecii au fost adăpostiți la Nashville Tennessee Valley Healthcare System VA. Măsurătorile de greutate și lungime au fost efectuate pe șoareci care au fost crescuți și întreținuți pe chow de crescător. Pentru a măsura lungimea, șoarecii au fost anesteziați cu izofluran și măsurați de la vârful nasului până la vârful cozii. Animalele au fost repartizate aleatoriu în grupuri experimentale. La finalizarea studiului, animalele au fost eutanasiate în conformitate cu Asociația Medicală Veterinară Americană prin gaz CO2 urmat de luxația colului uterin.
PCR în timp real
Țesuturile șoarecilor au fost îndepărtate și imersate în ARNlater (Qiagen, Valancia, CA) pentru studii de expresie a ARNm. ARN-ul a fost extras folosind un kit Qiagen RNeasy. Perechile Primer au fost proiectate folosind software-ul Primer Express (Applied Biosystems, Foster City, CA) și expresia GAPDH a fost utilizată ca control endogen. Nivelurile de expresie ale ARNm ale Slc3a1 și Slc7a9 au fost evaluate prin PCR cantitativă în timp real folosind SYBR verde și un sistem de detectare a secvenței ABI 7900HT (Applied Biosystems). Grundele sunt enumerate în Tabelul 1.
Western blot, imunocolorare și histologie
Au fost preparate extracte de proteine din celule întregi
Imagistica cu raze X
Imaginea prezentată este a unui bărbat de paisprezece săptămâni Slc3a1 -/- șoareci. Pentru a monitoriza formarea pietrei de-a lungul timpului, șoarecii au fost duși la Institutul de Științe Imagistice al Universității Vanderbilt, anesteziați cu izoflouran și oxigen până la imobilizare, apoi au fost plasați într-un aparat cu raze X Faxitron 2000 la setarea 35 pentru un timp de expunere de 4 s.
Măsurători de biomarker și aminoacizi
Pentru măsurătorile BUN și creatinină, sângele a fost colectat într-un tub CB 300 Z microvetă cu activator al cheagurilor (Sarstedt, Newton, NC) prin sângerare submandibulară sub anestezie cu izofluran cu o lancetă de 5,5 mm. Probele au fost coagulate la temperatura camerei timp de> 30 min și centrifugate la 4500 rpm timp de 10-20 min. Serul a fost imediat alicotat și depozitat la - 80 ° C pentru măsurarea azotului uree din sânge de către Laboratorul de patologie comparată al Centrului Medical Vanderbilt University și măsurarea creatininei de către Laboratorul de biomarkeri Core C al Universității Alabama-Birmingham O'Brien Center Core C DOMNIȘOARĂ. Concentrațiile plasmatice de aminoacizi au fost determinate prin HPLC cu fază inversă utilizând o versiune modificată a metodelor Bidlingmeyer și colab. [23].
Măsurători ale glutationului
Nivelurile de glutation au fost măsurate utilizând un test GSH-GLO Glutathione Assay (Promega, Madison, WI) conform instrucțiunilor producătorului. Concentrația proteică a lizatelor hepatice a fost determinată de BCA și concentrațiile normalizate la 400 ng/μl. Lizatele hepatice au fost testate +/− 500 μM TCEP. TCEP reduce orice glutation oxidat prezent în probă. Luminiscența a fost măsurată folosind un cititor de microplăci FLUOStar-Omega.
Rezultate
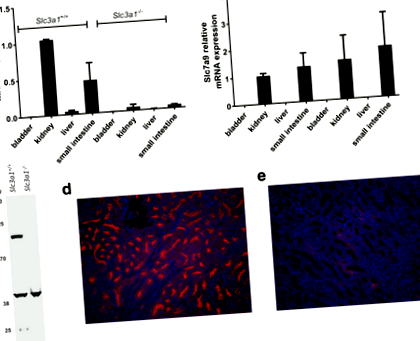
Am confirmat mai întâi eliminarea meciului Slc3a1 folosind RT-PCR pentru a evalua nivelurile de expresie în diferite țesuturi. Cum era de așteptat, Slc3a1 Nivelurile de ARN au fost reduse dramatic în țesuturile în care apare expresia în mod normal, cum ar fi rinichiul și intestinul subțire (Fig. 1a). În plus, așa cum era de așteptat, Slc7a9 Nivelurile de ARN au fost nealterate prin eliminarea Slc3a1 (Fig. 1b). Am folosit apoi Western blot și microscopie imunofluorescentă pentru a evalua pierderea expresiei rBAT în rinichi de Slc3a1 -/- șoareci. Western blot a demonstrat pierderea expresiei rBAT din lizatele renale (Fig. 1c). Microscopia imunofluorescentă pentru rBAT a demonstrat că eliminarea Slc3a1 a dus la pierderea expresiei rBAT în tubii proximali ai Slc3a1 -/- șoareci în comparație cu șoarecii de tip sălbatic (Fig. 1d și e).
Slc3a1 transcrierile și expresia proteinei rBAT se pierd la bărbați Slc3a1 șoareci knockout. Slc3a1 -/- șoarecii demonstrează pierderea Slc3a1 ARN (A) dar păstrarea de Slc7a9 ARN (b) în rinichi și intestinul subțire. Vezica și ficatul sunt furnizate ca martori negativi. Sunt prezentate mediile a două experimente independente realizate în triplicat (medie ± SD). (c) Western blot reprezentativ al rBAT de tip sălbatic și Slc3a1 -/- șoareci. Imunofluorescența a fost utilizată pentru a evalua expresia rBAT în tip sălbatic (d) și masculin Slc3a1 -/- șoareci (e). Animalele knockout demonstrează pierderea expresiei rBAT în tubul proximal
Șoarecii knockout nu au dezvoltat pietre la rinichi, dar au dezvoltat pietre vezicale detectabile prin raze X după cum sa raportat anterior (Fig. 2a) [10]. În concordanță cu observațiile anterioare, am observat diferențe de gen între bărbați și femei Slc3a1 -/- șoareci cu șoareci femele dezvoltând foarte rar pietre vezicale [10]. Nu am observat o rată ridicată de formare a pietrei vezicii urinare la mascul Slc3a1 -/- șoareci pe chow normal (0,31% cistină) (Tabelul 2). Cu toate acestea, când am plasat masculul Slc3a1 -/- șoareci pe crescători (0,36% cistină), am observat o rată mai mare de formare a pietrei vezicii urinare. Comparând procentul de șoareci cu calculii vezicii urinare la 28 de săptămâni, 100% din Slc3a1 -/- șoarecii de pe chow crescător aveau pietre vezicale, în timp ce doar 42% din Slc3a1 -/- șoarecii de pe chow obișnuit au prezentat formarea pietrei vezicii urinare (Fig. 2b). Rata de formare a pietrei vezicii urinare la șoareci pe crescătorul de reproducător este prezentată în Fig. 2c. Aceste rezultate demonstrează că aportul alimentar poate avea un impact major asupra ratei de formare a pietrei în Slc3a1 -/- șoareci.
Masculin Slc3a1 -/- șoarecii demonstrează rate diferite de formare a pietrei vezicii urinare, în funcție de dietă. A Raze X de șoareci cu formare tipică de piatră a vezicii urinare. b 42% dintre șoarecii de pe chow normal aveau pietre vezicale până la 28 de săptămâni, în timp ce 100% dintre șoareci aveau pietre vezicale până la 28 de săptămâni pe chow crescător (N = 12). c Radiografie de Slc3a1 -/- animalele au dezvăluit formarea de piatră a vezicii urinare pe chow de reproducător, așa cum este descrisă de un complot Kaplan-Meier (N = 8)
Am observat acel bărbat Slc3a1 -/- șoarecii au fost în mod constant mai mici în greutate în comparație cu Slc3a1 +/ + șoareci de aceeași vârstă (Fig. 3a, b). Această diferență de greutate nu a fost recapitulată la șoarecii femele. Toți șoarecii au prezentat aceeași lungime de la nas până la tipul cozii lor, indicând un fenotip metabolic general, mai degrabă decât deficiența nutrițională, a contribuit la diferența de greutate a șoarecilor mici crescuți și menținuți pe chow-ul crescătorului (Fig. 3c). Am evaluat nivelurile de aminoacizi din plasmă în Slc3a1 -/- șoareci și i-au comparat cu șoareci de tip sălbatic (Tabelul 3). În concordanță cu greutatea redusă la bărbați Slc3a1 -/- șoareci, am observat un fenotip mai sever cu multiple niveluri de aminoacizi diferite între tipurile sălbatice și animalele knockout. Evaluarea aminoacizilor atât la bărbați, cât și la femei Slc3a1 -/- șoarecii au dezvăluit că ornitina, lizina și taurina trebuie reduse la ambele sexe. Prin urmare, eliminarea rBAT a dus la reducerea ornitinei și a lizinei plasmatice la aceste animale. Cisteina, care formează cisteina atunci când două molecule sunt unite între ele, este metabolizată în taurină [24], care a fost, de asemenea, redusă între sexe. Interesant este că cistina plasmatică a fost redusă doar la bărbați Slc3a1 -/- în ciuda șoarecilor masculi și femele care prezintă cistinurie [11].
Analiza histologică a tipului sălbatic și masculin Slc3a1 -/- rinichi și vezici urinare la vârsta de 10-12 luni. Rinichii șoarecilor cu creatinină crescută (b și d) demonstrează mai multă dilatare tubulară și fibroză în comparație cu șoarecii cu creatinină normală (A și c) fie în mod regulat (A și b) sau crescător chow (c și d). Vezici de tip sălbatic (e), eliminare cu creatinină normală (f), și eliminarea cu creatinină crescută (g) sunt de asemenea afișați șoareci. Knockout-urile demonstrează infiltrat inflamator și cristale de cistină. Panou (g) demonstrează cristale de cistină încorporate în peretele vezicii urinare (săgeți). Se prezintă pete H&E reprezentative din fiecare grup de șoareci
Nivelurile de glutation la bărbați Slc3a1 -/- șoareci la vârsta de 8 săptămâni. Nivelurile reduse (GSH) și oxidate (GSSG) de glutation au fost măsurate în tipul sălbatic și Slc3a1 -/- animale. GSH, GSSG, total și raportul dintre formele reduse la cele oxidate (GSH: GSSG) au fost toate reduse în Slc3a1 -/- șoareci (N = 6 ± SEM)
Discuţie
Tratamentul pentru cistinurie nu sa schimbat dramatic în ultimii 20 de ani, în ciuda unei mai bune înțelegeri a bazei genetice [1]. Modelele de șoarece pentru cistinurie confirmă nu numai baza genetică a bolii, ci oferă și modele pentru testarea și evaluarea noilor terapii [10]. Există gene care afectează formarea de calculi la pacienții cu cistinurie care ar putea fi derivate din analiza pacienților și apoi testate pe modele de șoareci. Există probabil gene care afectează formarea calculilor la pacienții cu cistinurie care ar putea fi derivate din analiza pacienților și apoi testate pe modele de șoareci. Recent, Zee și colab. a demonstrat că acidul α-lipoic previne formarea pietrei de cistină în modelul de șoarece raportat în acest articol [11].
Au fost generate trei modele de șoarece de cistinurie de tip A, inclusiv cel descris aici care a fost generat prin ștergerea exonului 1 [10]. Celelalte modele constau în mutații spontane (E383K) [9] sau mutageneza indusă de ENU (D140G) [8]. Modelul D140G pe un fundal 129S2/SvPasCrl a demonstrat o reducere cu 40% a supraviețuirii cu 15 săptămâni cu creșterea valorii BUN serice, deși nu a existat o creștere a creatininei serice sau a fibrozei renale interstițiale [9]. Posibile diferențe de gen în aceste observații nu au fost comentate, deși pietrele au apărut în principal la bărbați [9]. Modelul E383K de pe fundalul C3HeB/FeJ a arătat BUN seric crescut la șoareci masculi în vârstă de 20 de săptămâni și greutate renală scăzută la șoareci masculi în vârstă de 32-48 săptămâni, fără niciun fenotip observat la șoareci femele [8]. Diferența de gen observată în formarea calculilor între bărbați și femei în contextul cistinuriei a fost observată la pacienți și revizuită în altă parte [27, 28]. Diferența de formare a calculilor nu pare să fie cauzată de diferențele dintre nivelurile de cistină urinară, dar se poate datora agregării diferențiale a cistinei în urina masculină față de cea feminină [27, 29]. Cu toate acestea, studiul nostru demonstrează că CKD apare la bărbații în vârstă Slc3a1 -/- șoareci.
Se știe puțin despre ce factori afectează fenotipul cistinuriei și progresia către CKD. [2] Am constatat că dieta se hrănește cu Slc3a1 -/- șoarecii au avut un efect dramatic asupra ratei de formare a pietrei. Tratamentul obișnuit pentru cistinurie include limitarea aportului dietetic de sodiu și proteine, aportul crescut de lichide, alcalinizarea urinară și, eventual, medicamente tiol și captopril [1]. Un studiu anterior a demonstrat că o dietă săracă în proteine, cu mai multe surse de proteine vegetale, a redus excreția de cistină la pacienții cu cistinurie [30]. Nu am găsit studii privind rolul dietei în formarea de pietre de cistină la modelele de cistinurie la șoareci. Studiile clinice la om asupra efectelor dietei pentru modificarea potențială a cistinuriei umane lipsesc [2]. Studiile viitoare ar putea fi direcționate spre evaluarea modificărilor dietetice într-un mod mai controlat pentru a elimina modificările care ar putea încetini progresia formării de pietre în cistinurie.
Incapacitatea de a recupera cistina din urină modifică probabil metabolismul cistinei la animalul întreg. Knockout de Slc3a1 afectează expresia acestuia nu numai în rinichi, ci și în intestin. Transportorul peptidic intestinal Pept1 (Slc15a1) se crede că permite reabsorbția cistinei și a altor aminoacizi din intestin compensând oarecum pierderea de Slc3a1 în intestin [31, 32]. În prezent, nu se cunoaște modul în care aceasta ar putea contribui la diferența generală de gen în cistinurie și diferențele observate ale nivelurilor de aminoacizi plasmatici.
Concluzii
Am demonstrat că aportul alimentar poate avea un impact asupra severității fenotipului cistinuriei atât în ceea ce privește formarea calculilor, cât și dezvoltarea CKD într-un model de cistinurie la șoarece. Șoarecii masculi au prezentat un fenotip mai sever în ceea ce privește greutatea animalelor și compoziția aminoacizilor din plasmă. Cistinuria a afectat compoziția glutationului din ficat. Studiile viitoare vor evalua în mod sistematic componentele dietetice asupra fenotipului cistinuriei și ce efect are alterarea rezultantă a metabolismului glutationului asupra fiziologiei și fiziopatologiei.
Disponibilitatea datelor și a materialelor
Seturile de date utilizate și/sau analizate în timpul studiului actual sunt disponibile de la autorul corespunzător, la o cerere rezonabilă.
- Corelarea nutriției hiperproteice a BUN la echilibrul de azot - Vizualizare text complet
- Utilizarea lipidelor, nutriția și colita la pacienții cu afecțiuni maligne hematologice - Vizualizare text complet
- Intervenția stilului de viață în ficatul gras (NAFLD) - Vizualizare text complet
- Importanța bacteriilor lactice în alimentele fermentate din Asia Fabrici de celule microbiene Text complet
- Produse lactate în tratamentul rahitismului hipofosfatemic - Vizualizare text complet