Întrebare: Ce mecanisme reglează ketogeneza și moderează impactul acesteia asupra bolii? Ce condiții sunt afectate direct de cetone și/sau o dietă ketogenică?
La pachet: Ketogeneza este reglementată, direct și indirect, de acțiunea insulinei. Dieta ketogenică are beneficii clinice clare pentru anumite afecțiuni rare care implică defecte ale căilor glicolitice. Dovezile preliminare indică, de asemenea, că pot fi benefice pentru pacienții cu cancer, boli neurodegenerative și diferite afecțiuni legate de inflamație.
Această revizuire din 2019 rezumă principalele mecanisme care guvernează ketogeneza și analizează efectele cetozei dietetice asupra stărilor specifice de boală.
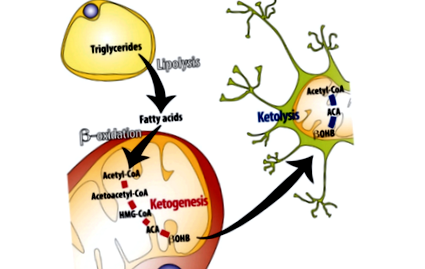
Ketogeneza - adică sinteza corpurilor cetonice în ficat - este determinată în primul rând de o supresie extinsă a nivelului de insulină (1). În primele ore ale unui post sau în timpul inițierii unei diete cu conținut scăzut de carbohidrați, depozitele de glucoză din ficat și mușchi vor fi eliberate în sânge pentru a menține nivelul glicemiei. Odată epuizate aceste depozite, acizii grași sunt eliberați din țesutul adipos. Când acești acizi grași ajung la ficat, suferă o oxidare beta și formează acetil-CoA. Când nivelurile de acetil-CoA devin suficient de ridicate, ficatul începe să producă corpuri cetonice (KB) în cantități semnificative (2). Aceste corpuri cetonice circulante sunt apoi preluate de alte celule și organe prin intermediul transportorului monocarboxilat 1 (MCT1), unde sunt apoi convertite înapoi în acetil-CoA pentru a fi utilizate ca sursă de energie (3).
Figura 1: Rezumatul proceselor cheie care reglementează ketogeneza
Ketogeneza este astfel reglementată în primul rând de disponibilitatea acizilor grași în ficat. Numai prin acest mecanism, ketogeneza este suprimată chiar de o creștere modestă a nivelurilor de insulină, care mută celulele grase de la descompunerea acidului gras și se eliberează către stocarea acizilor grași, reducând fluxul de acizi grași în celulele hepatice (4). Insulina suprimă simultan cetoza prin efecte de reglare directă asupra celulelor hepatice, inclusiv creșterea malonil-CoA, care reduce disponibilitatea unui intermediar ketogenic cheie (acil-CoA) în mitocondriile hepatice, inhibând astfel cetogeneza (5).
Figura 2: Reglarea cetogenezei de către insulină. Săgețile roșii indică procesele care sunt reglate în jos sau oprite în fiecare circumstanță. Insulina, prin efectele sale asupra producției de malonil-CoA, suprimă disponibilitatea acil-CoA în mitocondriile hepatice, care la rândul său suprimă cetogeneza.
Dieta ketogenică (KD) - adică o dietă care induce cetoza, în general prin suprimarea dramatică a aportului de carbohidrați - are utilitate clinică clară și specifică pentru două afecțiuni, ambele caracterizate prin defecte ale căilor glicolitice. Sindromul deficitului GLUT1 (GLUT1 DS) afectează transportul glucozei prin bariera hematoencefalică și duce la niveluri scăzute de glucoză în lichidul cefalorahidian. Simptomele includ convulsii, tulburări de mișcare și disfuncție cognitivă. Dieta ketogenică rezolvă rapid aceste simptome; se recomandă pacienților cu această afecțiune genetică să inițieze o KD cât mai curând posibil după diagnostic pentru a preveni leziunile cerebrale pe termen lung (6). Sindromul de deficit de piruvat-dehidrogenază (PDH-DS) este similar prin faptul că o dietă ketogenică va ameliora simptomele prin eludarea patologiilor legate de căile glicolitice centrale (7). Beneficiile bine documentate ale unei diete ketogenice la pacienții cu convulsii rezistente la medicamente pot apărea prin mecanisme similare (8), deși în aceste cazuri o KD este menținută în general alături de medicamentele antiepileptice.
În aceste condiții și în condiții similare, KD mută metabolismul celular departe de glicoliză. Pe un KD, 90% din energie este derivată din grăsimi și doar 10% din carbohidrați și proteine, reducând atât nevoia, cât și potențialul de glicoliză. Convulsiile, de exemplu, sunt caracterizate printr-o rată glicolitică ridicată; dieta ketogenică suprimă glicoliza și reduce astfel riscul de convulsii (9). KD-urile pot avea, de asemenea, beneficii mai directe și secundare în aceste condiții, prin păstrarea homeostaziei energetice neuronale și a sănătății mitocondriale. Nivelurile de ATP neuronale scăzute cresc excitabilitatea neuronală prin efectele (lipsei) de ATP asupra canalelor de potasiu (10); dietele ketogenice susțin niveluri crescute de ATP celular, în special în contextul disfuncției glicolitice. KD-urile reduc simultan producția de specii reactive de oxigen (ROS) de către mitocondriile celulare și promovează biogeneza mitocondrială în cadrul neuronilor (11). Aceste și alte efecte asupra moleculelor specifice, cum ar fi adenozina și acizii grași individuali, pot explica în continuare beneficiile unei diete ketogenice asupra prevenirii și controlului convulsiilor (12).
În periferie, corpurile cetonice sunt antiinflamatorii datorită inhibării lor a NLRP3 (13). Studiile la animale au furnizat dovezi preliminare care indică faptul că o dietă ketogenică poate preveni sau reduce severitatea afecțiunilor legate direct de inflamație, cum ar fi guta și artrita (14). Aceleași efecte au condus la sugestia că o dietă ketogenică poate gestiona starea inflamatorie cronică, de grad scăzut, asociată bolilor cardiovasculare, reducând astfel riscul bolilor cardiace (15).
Rolul dietei ketogene în tratamentul și prevenirea cancerului a fost discutat pe larg pe CrossFit.com (16). În teorie, o dietă ketogenică exploatează efectul Warburg, privând celulele canceroase dependente de glicoliză de o sursă primară de combustibil fără a afecta celulele sănătoase. Cu toate acestea, cel puțin unele celule canceroase sunt capabile să utilizeze corpuri cetonice drept combustibil, anulând acest efect. Cu toate acestea, dovezile actuale indică o KD îmbunătățește în mod constant calitatea vieții la pacienții cu cancer și, în special, reduce efectele secundare gastro-intestinale și neurologice ale terapiilor existente pentru cancer (17). Utilizarea unei diete ketogenice ca adjuvant pentru chimioterapie, radioterapie și alte tratamente pentru cancer va continua să fie o zonă de explorare.
Figura 3: Mecanisme hipotetice prin care o dietă ketogenică afectează creșterea tumorii
Dovezile timpurii sugerează că o dietă ketogenică (sau creșterea artificială a cetonelor serice prin utilizarea suplimentelor cetonice) poate restabili temporar funcția cognitivă la pacienții aflați în stadiile incipiente ale bolii neurodegenerative (18). Autorii acestei revizuiri susțin că cel puțin unele cazuri de boală Alzheimer sunt de natură metabolică, astfel încât o dietă ketogenică, prin susținerea menținerii pe termen lung a homeostaziei energetice neuronale, poate preveni și chiar inversa neurodegenerarea. Cu toate acestea, există puține date care să susțină această teorie. În mod similar, dovezile preliminare sugerează că o dietă ketogenică poate îmbunătăți simptomele nemotorii la pacienții cu boala Parkinson (19). Având în vedere că aceste simptome sunt slab abordate de actualul standard de îngrijire (L-DOPA), KD este privită ca o terapie adjuvantă promițătoare pentru pacienții cu Parkinson.
KD a fost, de asemenea, propus ca tratament pentru boala hepatică grasă, deoarece restricția de carbohidrați asociată cu o KD duce la eliminarea rapidă a depozitelor de grăsime hepatică (20). În special, utilizarea unui KD pentru a trata NAFLD poate duce la un ciclu virtuos, deoarece un ficat fără grăsimi este capabil să inițieze mai rapid cetoza ca răspuns la supresia insulinei decât un ficat mai gras.
Datele minime, în mare parte extrase de la copii, au sugerat că aderența pe termen lung la o boală de boală poate fi asociată cu un risc crescut de fracturi, calculi renali și întârzierea creșterii (21). Cu toate acestea, aceleași dovezi sugerează că aceste efecte secundare pot fi rezultatul unor diete ketogenice slab construite care duc la deficit de vitamina D și condiții similare și pot să nu fie inerente dietei în sine.
În general, această revizuire oferă dovezi care susțin utilizarea unei BK într-o varietate de afecțiuni inflamatorii, cancere și tulburări neurologice. Cercetările care studiază dieta ketogenică rămân limitate, dar KD rămâne o opțiune promițătoare pentru condițiile în care defectele glicolizei, homeostazia energiei celulare sau inflamația joacă un rol.
- Efectele unei diete ketogenice asupra puterii și puterii
- Descrierea dietei ketogenice în limba spaniolă Descriere a Dieta Ketogénica în Español Epilepsie
- Provocări clinice Dieta ketogenică de siguranță incertă pentru sănătatea inimii MedPage astăzi
- Instructorului de fitness Pavel Tsatsouline îi place CrossFit, explică dieta lui Joe Rogan; Fitness Volt
- Nu începeți o altă dietă până când nu citiți acest lucru; Dă-mi CrossFit