Din Curriculum în Genetică și Biologie Moleculară (A.A.G., S.T.L.), Departamentul de Biostatistică (C.M., T.S., G.K.) și Departamentul de Patologie și Medicină de Laborator (S.T.L.), Universitatea din Carolina de Nord, Chapel Hill.
Din Curriculum în Genetică și Biologie Moleculară (A.A.G., S.T.L.), Departamentul de Biostatistică (C.M., T.S., G.K.) și Departamentul de Patologie și Medicină de Laborator (S.T.L.), Universitatea din Carolina de Nord, Chapel Hill.
Din Curriculum în Genetică și Biologie Moleculară (A.A.G., S.T.L.), Departamentul de Biostatistică (C.M., T.S., G.K.) și Departamentul de Patologie și Medicină de Laborator (S.T.L.), Universitatea din Carolina de Nord, Chapel Hill.
Din Curriculum în Genetică și Biologie Moleculară (A.A.G., S.T.L.), Departamentul de Biostatistică (C.M., T.S., G.K.) și Departamentul de Patologie și Medicină de Laborator (S.T.L.), Universitatea din Carolina de Nord, Chapel Hill.
Din Curriculum în Genetică și Biologie Moleculară (A.A.G., S.T.L.), Departamentul de Biostatistică (C.M., T.S., G.K.) și Departamentul de Patologie și Medicină de Laborator (S.T.L.), Universitatea din Carolina de Nord, Chapel Hill.
Vizualizați cea mai recentă versiune a acestui articol. Versiunile anterioare:
Abstract
Obiectiv- Fibrinogenul crescut este corelat cu ateroscleroza severă, așa cum este definită de apariția evenimentelor ischemice, dar baza mecanicistă a acestei corelații rămâne necunoscută. Pentru a studia această relație, am examinat ateroscleroza spontană și indusă de dietă la șoarecii transgenici cu hiperfibrinogenemie (fibrinogen crescut).
Metode și rezultate— Șoarecii normali și transgenici au fost hrăniți fie cu o dietă aterogenă, fie cu un simplu chow de crescător. Am măsurat nivelurile de fibrinogen plasmatic și am identificat o creștere a fibrinogenului în funcție de vârstă și de dietă. După 8 până la 12 luni, secțiunile aortice au fost pregătite și colorate, iar leziunile care conțin lipide au fost numărate, măsurate și evaluate pentru maturitate. Depozitele umplute cu lipide au apărut spontan într-un număr mic de șoareci de pe chow-ul crescător; leziunile tipice de tip striuri grase au apărut la aproape toate animalele hrănite cu dietă. Analiza morfometrică a arătat că nici numărul, nici mărimea leziunilor nu au fost influențate nici de nivelul fibrinogenului, nici de genotip.
Concluzii - Datele noastre au arătat că nici concentrația fibrinogenului, nici genotipul nu au avut un efect semnificativ statistic asupra inițierii, creșterii inițiale sau progresiei timpurii a leziunilor aterosclerotice.
Este bine cunoscut faptul că fibrinogenul crescut este corelat cu ateroscleroza severă, așa cum este definită de apariția evenimentelor ischemice. Primul studiu major care a raportat această corelație a fost Northwick Park Heart Study, în care, în 1980, Meade și colab. 1 au arătat o asociere semnificativă între decesul cardiovascular și concentrația de fibrinogen, care era independentă de alți factori de risc. De atunci, multe rapoarte au legat niveluri ridicate de fibrinogen cu toate formele de boli cardiovasculare (BCV). Studiile Caerphilly/Speedwell au arătat că fibrinogenul crescut este corelat cu boala cardiacă ischemică. 2 Studiul de la Göteborg a raportat că fibrinogenul este asociat cu infarct miocardic și accident vascular cerebral, boli coronariene și mortalitate totală. 3 Studiul Framingham a arătat că o varietate de BCV trebuie corelate cu fibrinogenul, inclusiv accidentul vascular cerebral, boala coronariană și boala ocluzivă arterială periferică. 4.5 Deoarece mai multe studii au coroborat aceste constatări (a se vedea revizuirea 6), nu există nicio îndoială că fibrinogenul plasmatic crescut este corelat cu BCV.
Mecanismul patologic care leagă hiperfibrinogenemia de un risc crescut de ateroscleroză evidentă din punct de vedere clinic rămâne necunoscut. O ipoteză este sugerată de efectul fibrinogenului asupra celulelor musculare netede (SMC) și celulelor endoteliale, în care fibrinogenul acționează ca o matrice provizorie pentru migrare și în care produsele de degradare a fibrinei (ogenilor) acționează ca mitogeni. 7 Aceste mecanisme sugerează că fibrinogenul crescut afectează puternic 2 dintre celulele implicate în formarea leziunii. În schimb, fibrinogenul crescut poate fi o consecință a aterosclerozei, în măsura în care fibrinogenul este o proteină în fază acută, iar nivelurile sale cresc ca răspuns la boală. Desigur, fibrinogenul crescut poate fi atât o cauză, cât și o consecință a bolii aterosclerotice.
Pentru a oferi un sistem experimental pentru a examina baza mecanicistă pentru conexiunea dintre fibrinogenul crescut și BCV, am generat șoareci transgenici cu hiperfibrinogenemie. În studiul de față, le-am folosit pentru a determina dacă nivelurile crescute de fibrinogen afectează ateroscleroza indusă de dietă la șoareci. Am ales un model indus de dietă pentru a studia inițierea și dezvoltarea timpurie a aterosclerozei, deoarece am anticipat că fibrinogenul crescut va promova patogeneza bolii. Deși leziunile induse de dietă nu progresează către plăci în stadiu târziu, leziunile cu dungi grase în aorta proximală a șoarecilor normali sunt similare cu leziunile foarte timpurii la om. 8 Leziunile din modelul nostru de șoarece au fost examinate pentru modificări de inițiere, sarcină și maturitate care au fost datorate nivelurilor de genotip sau fibrinogen.
Metode
Materiale
Produsele chimice au fost achiziționate de la Sigma Chemical Co., dacă nu se specifică altfel. Medicamentele anestezice au fost achiziționate de la Barber Veterinary Supply. Anticorpul anti-fibrinogen de iepure provenea de la Dako Corp. Materialele pentru prelevarea de sânge, secționarea și colorarea au fost de la Fisher. Chow de reproducător a fost Picolab Mouse Diet 20 (nr. 5058 iradiat) de la Purina-Mills; dieta aterogenă (TD 88051) a fost de la Harlan/Teklad.
Animale transgenice
Toate procedurile care implică șoareci au fost aprobate de Comitetul instituțional de îngrijire și utilizare a animalelor. Șoarecii au fost adăpostiți într-o unitate cu barieră completă în cuști sterilizate. După cum s-a descris anterior, am generat șoareci transgenici prin microinjecția locusului fibrinogenului de șoarece în ovocitele C57BL/6. 9 Transgenul a fost o clonă fagică P1 cu o inserție de 80 kb de ADN genomic de 129 SvEv, incluzând locusul fibrinogenului de 50 kb (α, β și γ) flancat de 5 și 25 kb. Șoarecii transgenici au fost identificați prin reacția în lanț a polimerazei. Am stabilit o linie de fibrinogen transgen pozitiv (FT +), în care concentrațiile plasmatice de fibrinogen au fost aproape de două ori mai mari decât la șoarecii C57BL/6 normali. Aceste animale nu au defecte de fertilitate și nici o boală trombotică și trăiesc o durată normală de viață. 9
Proiectare experimentală
Șoarecii BC au fost hrăniți cu chow de crescător până la eutanasie la 8 luni (șoareci BC8) sau 12 luni (șoareci BC12); Chow de crescător conținea nutrienți standard plus 9% grăsimi și 20% proteine. Șoarecii AD au fost hrăniți cu chow de crescător timp de 4 luni și apoi au fost hrăniți cu o dietă aterogenă până la eutanasie după 4 luni (șoareci AD4, în vârstă de 8 luni) sau 6 luni (șoareci AD6, în vârstă de 10 luni) în dietă; această dietă aterogenă, dezvoltată de Paigen și colab., 8 conținea substanțe nutritive standard plus 15,8% grăsimi, 1,25% colesterol și 0,5% colat de sodiu. Sângele a fost prelevat lunar de la toate animalele, începând cu 2 luni (șoareci BC) sau 4 luni (șoareci AD, cu 1 zi înainte de începerea dietei aterogene).
Analize plasmatice
Animalele au fost postite timp de 4 până la 6 ore și anesteziate cu ketamină/xilazină (0,31 ml/0,11 ml adus la 1 ml în ser fiziologic steril) pe baza greutății (0,1 ml/30 g). Sângele a fost extras din spațiul retro-orbital și centrifugat la 15.000 rpm timp de 15 minute, iar supernatantul plasmatic a fost depozitat la -80 ° C. Nivelurile de fibrinogen au fost determinate de ELISA. 9 Colesterolul total a fost determinat utilizând o modificare a setului de colesterol total Wako CII. Pe scurt, într-o placă cu 96 de godeuri, 100 μL de substrat cromogen/soluție enzimatică au fost amestecate cu 1 μL de probă (în duplicat). După 10 minute la 37 ° C, placa a fost citită la 550 nm. Colesterolul total în miligrame pe decilitru a fost determinat ca densitatea optică medie a probei împărțită la densitatea optică medie a standardului.
Pregătirea și măsurarea secțiunilor aortice
După ce șoarecii au fost anesteziați (vezi Analize plasmatice), inima a fost perfuzată prin ventriculul stâng cu 10 ml de paraformaldehidă proaspătă 4%. 10 Țesutul a fost fixat in situ timp de> 24 de ore. Aortas au fost procesate și evaluate așa cum este descris de Paigen și colab 8 și modificat de Reddick și colab. 10 Pe scurt, inima a fost tăiată într-un plan imediat sub cele 2 atrii, așa cum se arată în Figura 2A. Sinusul superior al inimii/aortului a fost încorporat în compusul OCT, înghețat și secționat în serie (6 până la 8 μm grosime). Secțiunile au fost identificate după locația prezentată în Figura 2A (adică secțiunea 1, 2, 3 sau 4). 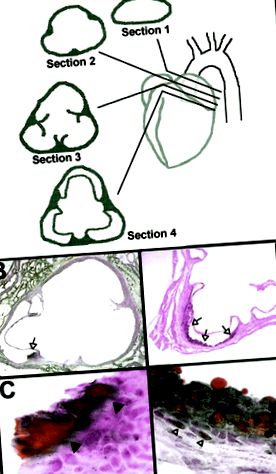
Figura 2. Histologia leziunii. Aortele au fost secționate ca schemate și colorate cu Sudan IV și hematoxilină. A, sinusul aortic secționat într-un plan paralel cu o linie trasată între fundurile ambelor atrii. Secțiunea 1 este din afara inimii. Secțiunea 2 prezintă locurile de fixare a supapelor. Secțiunea 3 prezintă bucăți ale supapelor și ale locurilor de fixare. Secțiunea 4 prezintă supapele/accesoriile complete. B, secțiunea 4 (mărire originală × 2) de la un șoarece FT +/BC, care arată un depozit colorat în Sudan IV (săgeată deschisă). C, Mărire mai mare (mărire inițială × 40) a leziunii prezentate în panoul B. Limita interioară a depozitului lipidic este indicată cu vârfuri de săgeată închise. D, Secțiunea 4 (mărire originală × 4) a unui șoarece FT−/AD care prezintă o leziune cu dungi grase care se extinde de la o cuspidă a valvei la următoarea (săgeți deschise, mărire originală × 4). E, mărire mai mare (mărire inițială × 40) a leziunii prezentate în panoul D. Celulele din spumă (săgeți închise) și SMC încărcate de colesterol (vârfuri de săgeți deschise) sunt clar evidente.
Secțiunile au fost colorate cu Sudan IV (pentru lipide) și hematoxilină prin tehnici standard de colorare. După captarea imaginii la mărirea × 2, zona leziunii a fost măsurată utilizând fie NIH Image (versiunea 1.62), fie Scion Image (versiunea beta 3b). Diapozitivele din secțiunea 4 de la șoarecii AD4 și BC8 selectați au fost imunocolorați cu anticorp fibrinogen anti-uman.
Analize statistice
Ecuațiile de estimare generalizate (GEE) au fost utilizate pentru a acomoda toate punctele de timp în mod individual, în timp ce se ține cont de corelația dintre mouse. Modelele GEE permit evaluarea modelelor în timp, precum și pentru covariabile, cum ar fi colesterolul, fibrinogenul și genotipul.
Rezultate
Proiectare experimentală
Așa cum este descris în Metode, animalele au fost fie menținute pe chow de reproducător (grup BC) pe tot parcursul experimentului, fie hrănite cu o dietă aterogenă (grup AD) începând cu vârsta de 4 luni. Șoarecii BC au servit ca martori pentru grupul AD și ca animale experimentale pentru a evalua aterogeneza spontană. Rezultatele sunt raportate ca genotip/grup de dietă: FT +/BC8 (n = 21) și FT−/BC8 (n = 20), FT +/BC12 (n = 19) și FT−/BC12 (n = 18), FT +/AD4 (n = 20) și FT−/AD4 (n = 20) și FT +/AD6 (n = 15) și FT−/AD6 (n = 12).
Nivelurile de colesterol plasmatic la șoareci pe diete normale și aterogene
Nivelurile de colesterol sunt prezentate în Figura 1A, unde datele din stânga barei verticale au fost obținute de la toți șoarecii, iar datele din dreapta au fost obținute de la șoareci eutanasiați la vârsta de 10 (șoareci AD6) sau 12 (șoareci BC12). Toți șoarecii au început cu niveluri similare de colesterol. Pentru șoarecii BC la 2 luni, nivelul mediu de colesterol a fost de 118 ± 29 mg/dL la șoarecii FT + (cercuri deschise) și 114 ± 21 mg/dL la șoarecii FT− (cercuri umplute). La 8 luni, nivelul mediu de colesterol al șoarecilor BC nu s-a modificat semnificativ pentru niciunul dintre genotipuri: 121 ± 34 mg/dL pentru șoarecii FT + și 123 ± 32 mg/dL pentru șoarecii FT−. Din luna 9 până la eutanasie, nivelul mediu de colesterol la șoarecii BC a crescut constant, cu niveluri finale de 168 ± 28 mg/dL pentru șoarecii FT + și 171 ± 50 pentru șoarecii FT−. Astfel, după 12 luni de reproducere, nivelul colesterolului la toți șoarecii a fost semnificativ crescut față de nivelurile inițiale (P
figura 1. Valorile plasmatice ale colesterolului și fibrinogenului. Colesterolul (A) sau fibrinogenul (B) a fost măsurat lunar, începând cu 2 luni (grup BC) sau 4 luni (grup AD). Bara la 8 luni reprezintă eutanasierea șoarecilor BC8 și AD4. Datele din stânga acestei bare sunt de la toți șoarecii, iar datele din dreapta provin exclusiv de la șoareci BC12 și AD6. Cercurile umplute indică șoareci FT−/BC (n = 38/18, total/BC12); cercuri deschise, șoareci FT +/BC (n = 40/19); pătrate umplute, șoareci FT−/AD (n = 32/12, total/AD6); și pătrate deschise, șoareci FT +/AD (n = 35/15).
Histologia leziunii
La eutanasie, sinusul aortic a fost secționat (Figura 2A) și colorat cu Sudan IV pentru a identifica leziunile care conțin lipide. Așa cum s-a descris anterior, cele mai multe leziuni 8,11,12 au fost găsite în secțiunea 4. Probele reprezentative din secțiunea 4 sunt prezentate în Figura 2B până la 2E. O zonă colorată Sudan IV în aortă de la un șoarece FT +/BC este prezentată la măririle originale × 2 (Figura 2B) și × 40 (Figura 2C). Această leziune nu avea caracteristicile unei urme de grăsime definite de Stary și colab 13, în măsura în care nu a existat nicio acumulare intracelulară de lipide (comparați cu Figura 2E). Aceste depozite lipidice au fost prezente doar la șoareci BC, în aceleași locații (baza valvelor) ca dungi grase la șoareci AD. Odată cu vârsta, mai mulți șoareci au dezvoltat aceste leziuni, iar dimensiunea, dar nu numărul, a leziunilor a crescut. Deși leziunile de această natură nu au fost descrise, le-am marcat ca leziuni la șoarecii BC. Astfel de leziuni pot fi asociate cu dieta bogată a crescătorilor.
O zonă colorată în Sudan IV în aorta unui șoarece FT−/AD6 este prezentată la măririle originale × 4 (Figura 2D) și × 40 (Figura 2E). Spre deosebire de leziunile BC, această leziune avea caracteristicile unei dungi grase, incluzând celule rotunde de spumă în intima (săgeți închise din Figura 2E) și SMC cu depozite de colesterol citoplasmatic (vârfuri de săgeți deschise în Figura 2E). Toate leziunile la animalele AD au fost dungi clasice de grăsime, deși niciuna nu avea capace fibroase. Aceasta implică faptul că nivelurile crescute de fibrinogen nu au modificat dezvoltarea sau progresia leziunilor induse de dietă.
În plus față de petele Sudan IV, probele de secțiunea 4 de la șoareci BC8 și AD4 au fost imunoclorați cu un anticorp policlonal la fibrinogen uman. Deși colorarea unei secțiuni analoage 4 dintr-un șoarece apoE nul 10 a demonstrat fibrino-antigene în leziunile mai avansate, nu am detectat fibrino-antigene nici în depunerile lipidice, nici în leziunile cu dungi grase (datele nu sunt prezentate).
Analiza morfometrică
Am examinat secțiuni de la 79 de șoareci și am marcat toate zonele colorate în Sudan IV ca leziuni. Majoritatea celor 36 de șoareci hrăniți numai cu crescători (13 din 19 șoareci BC8 și 10 din 17 șoareci BC12) nu au avut leziuni. Cu o excepție, ceilalți șoareci BC au avut doar o leziune, întotdeauna în secțiunea 4. Excepția, un șoarece FT−/BC8, a avut 3 leziuni în secțiunea 4. Numărul mediu de leziuni per șoarece BC, inclusiv șoarecii fără leziuni, este prezentate în Tabelul 1; acest număr a fost întotdeauna
TABEL 1. Numărul și aria leziunii, luând în considerare toate animalele experimentale
TABELUL 2. Numărul și aria leziunii, luând în considerare numai animalele cu leziuni
Pentru fiecare șoarece, zona leziunii a fost determinată ca suma suprafețelor fiecărei leziuni separate în micrometri pătrate. Valorile medii pentru toți șoarecii sunt prezentate în Tabelul 1, iar valorile medii pentru doar șoarecii cu leziuni sunt prezentate în Tabelul 2. Evaluarea tuturor animalelor ne-a permis evaluarea sarcinii globale a leziunilor pe baza suprafeței acoperite, în timp ce evaluarea doar șoarecii cu leziuni au furnizat informații cu privire la calitatea leziunilor în sine. Pentru șoarecii hrăniți cu crescători, 4 dintre cei 6 șoareci BC8 și 4 dintre cei 7 șoareci BC12 au avut suprafețe de leziune totale de 3 μm 2, cea mai mică suprafață fiind de 1,1 × 10 3 μm 2. Șoarecii rămași aveau zone de leziune totale> 3 × 10 3 μm 2, cea mai mare suprafață totală fiind de 1,0 × 10 4 μm 2. Zona de leziune la șoarecii hrăniți cu o dietă aterogenă a fost de aproximativ 10 ori mai mare. Secțiunea 4 din 21 din 24 șoareci AD4 cu leziuni au avut o suprafață totală a leziunii de 4 μm 2 (cea mai mică suprafață a leziunii a fost 0,5 × 10 3 μm 2); 3 șoareci aveau zone de leziune totale> 3 × 10 4 μm 2 (cele mai mari fiind 4 × 10 4 μm 2). După 6 luni de dietă aterogenă, zonele de leziune au fost mai mari: 6 din 14 șoareci AD6 aveau zone de leziune 4 μm 2 și 8 din 14 șoareci AD6 aveau zone de leziune> 3 × 10 4 μm 2 .
RANCOVA a fost aplicat celor 3 modele discutate în Metode. Aceste analize au fost efectuate de două ori, cu utilizarea fie a tuturor animalelor din populația experimentală, fie a acelor animale care aveau leziuni prezente. Analiza întregii populații de animale experimentale oferă o indicație a impactului fibrinogenului asupra inițierii sau localizării leziunilor în curs de dezvoltare. Prin evaluarea numai a animalelor diferite de zero, analiza datelor ilustrează în continuare efectele fibrinogenului asupra zonei leziunii, numărului leziunii sau maturității leziunii. Includem datele din ambele analize (tabelele 1 și 2), deoarece diferențele dintre aceste numere evidențiază impactul includerii sau nu a șoarecilor fără leziuni. Aceste analize colective sugerează că nici genotipul, nici valorile medii ale fibrinogenului nu au influențat nici suprafața totală (intervalul de P= 0,097 până la 0,980) sau numărul (intervalul de P= 0,102 până la 0,941) ale leziunilor din secțiunea 4 a șoarecilor BC sau secțiunilor 2 până la 4 ale șoarecilor AD. Aceste date nu arată în mod clar nicio diferență semnificativă între numărul sau aria leziunii și nivelul de genotip sau fibrinogen.
Discuţie
Astfel, datele noastre indică faptul că în modelul nostru de șoarece, fibrinogenul nu a avut nici un rol în inducerea, sarcina sau progresia leziunilor aterosclerotice timpurii. Deși studiul de față a examinat doar ateroscleroza timpurie, această concluzie pare să fie incompatibilă cu un număr mare de rapoarte epidemiologice privind bolile umane. Aceste rapoarte au constatat că hiperfibrinogenemia este asociată cu ateroscleroza crescută în toate etapele și în toate părțile arborelui vascular (coronarian, carotid și periferic). 6 Rezultatele noastre sunt mai consistente cu cele ale lui Xiao și colab., 14 care au constatat că deficitul de fibrinogen nu a modificat dezvoltarea leziunilor aterosclerotice într-un model de șoarece. Prin împerecherea șoarecilor nul fibrinogen cu șoareci apoE nul, au fost capabili să examineze influența deficitului de fibrinogen asupra dezvoltării aterosclerozei avansate. Rezultatele lor au arătat că la șoarecii apoE nul, fibrinogenul nu a fost necesar pentru dezvoltarea bolii aterosclerotice avansate și nici deficiența de fibrinogen nu a avut un impact asupra formării leziunii, dimensiunii sau morfologiei. Aceste studii combinate la șoareci sugerează că fibrinogenul crescut la om poate fi un răspuns la boală, dar nu poate modifica direct creșterea și dezvoltarea leziunii aterosclerotice.
Primit la 5 septembrie 2002; revizuire acceptată la 25 septembrie 2002.
Această lucrare a fost susținută de grantul Institutului Național de Sănătate HL-52706. Mulțumim lui Shin Ja Kim pentru pregătirea secțiunilor înghețate și dr. Robert Bagnell pentru asistență la microscopie. De asemenea, mulțumim doctorilor Virginia Godfrey și Nobuyo Maeda pentru sfaturi pe parcursul acestei lucrări și pentru lectura critică a manuscrisului.
- Efectele Momordica charantia asupra rezistenței la insulină și a obezității viscerale la șoareci pe o dietă bogată în grăsimi
- Efectele β - Conținut de glucan și perle de orz în dietă - Șoareci obezi induși - Aoe - 2017 - Cereale
- Efectele preadipocitelor derivate de la șoareci hrăniți cu o dietă bogată în grăsimi asupra potențialului angiogen al
- Efectele stresului mental cronic și ale dietei aterogene asupra mediului inflamator imunitar în
- Fructoza și efectele toxice ale zahărului - Diet Doctor
