Abstract
fundal
Infuzia de dexmedetomidină îmbunătățește oxigenarea și mecanica pulmonară la pacienții cu boală pulmonară obstructivă cronică; cu toate acestea, efectul său la pacienții cu boli pulmonare restrictive nu a fost încă aprofundat investigat. Scopul acestei lucrări a fost de a evalua efectele perfuziei de dexmedetomidină asupra oxigenării și mecanicii pulmonare la pacienții obezi morbid cu boli pulmonare restrictive.
Metode
Patruzeci și doi de pacienți cu obezitate morbidă programați pentru intervenții chirurgicale bariatrice au fost incluși în studiu. Pacienții au fost randomizați pentru a primi fie perfuzie de dexmedetomidină la o doză în bolus de 1 mcg/Kg urmată de perfuzie la 1 mcg/Kg/oră timp de 90 min (grup Dexmedetomidină), fie perfuzie salină normală (grup control). Ambele grupuri au fost comparate în ceea ce privește: oxigenarea 2/fracția de oxigen inspirat (FiO2)>, complianța pulmonară, spațiul mort, presiunea platoului, tensiunea arterială și ritmul cardiac.
Rezultate
Grupul cu dexmedetomidină a prezentat o îmbunătățire semnificativă a raportului PaO2/FiO2 și o complianță pulmonară mai mare comparativ cu grupul martor până la sfârșitul perfuziei cu medicamente. Grupul cu dexmedetomidină a demonstrat scăderea spațiului mort, a presiunii platoului, a tensiunii arteriale și a ritmului cardiac, comparativ cu grupul de control până la sfârșitul perfuziei cu medicamente.
Concluzie
O perfuzie de dexmedetomidină de 90 de minute a dus la o îmbunătățire moderată a oxigenării și a mecanicii pulmonare la pacienții obezi morbid cu boală pulmonară restrictivă.
Înregistrarea procesului
clinictrials.gov: NCT02843698 la 20 iulie 2016.
fundal
Dexmedetomidina este un agonist selectiv α - 2 cu diferite utilizări clinice atât în anestezie, cât și în unitatea de terapie intensivă. Pe lângă efectele sale sedative și cardiovasculare, dexmedetomidina are efecte respiratorii favorabile la animale [1, 2] și la anumite grupuri de pacienți la oameni. Efectele dexmedetomidinei asupra oxigenării și mecanicii pulmonare au fost investigate în bolile pulmonare obstructive. Dexmedetomidina a scăzut spațiul mort și a îmbunătățit atât complianța pulmonară, cât și oxigenarea la pacienții cu boală pulmonară obstructivă cronică (BPOC) supuși unei intervenții chirurgicale pentru cancerul pulmonar [3].
În cazul bolilor pulmonare restrictive, efectul posibil al dexmedetomidinei nu a fost bine investigat la om. Într-un model animal de obezitate experimentală, administrarea dexmedetomidinei a arătat caracteristici morfologice și funcționale pulmonare mai bune comparativ cu propofolul [4]; astfel, am emis ipoteza că un efect similar ar putea fi prezent la oameni. Pacienții cu obezitate morbidă se caracterizează prin prevalența ridicată a bolilor pulmonare restrictive [5]; astfel, am investigat efectele perfuziei de dexmedetomidină asupra oxigenării (raportul P/F), precum și a mecanicii pulmonare (complianță și spațiu mort) într-un grup selectat de pacienți obezi morbid cu boli pulmonare restrictive, pentru a afla posibilele beneficii ale acestui medicament asupra acestei populații.
Metode
Un studiu randomizat dublu-orb controlat a fost realizat în spitalul universitar din Cairo după aprobarea revizuirii consiliului instituțional (N - 12-2016) la 24 decembrie 2016. Studiul a fost înregistrat la sistemul de registre clinic.trials.gov la 20 iulie 2016 (NCT02843698). Un consimțământ informat scris a fost obținut de la participanți înainte de recrutare. Pacienții au fost randomizați în funcție de un generator de numere aleatorii online. Ascunderea a fost realizată folosind plicuri opace sigilate.
Studiul a inclus 42 de pacienți obezi morbid cu boli pulmonare restrictive [6]. Anestezia a fost indusă de propofol (2 mg/Kg LBW) și fentanil (2 μg/Kg LBW). După inducerea anesteziei, tubul endotraheal a fost introdus ajutat de rocuroniu (0,5 mg/Kg LBW). Anestezia a fost menținută de izofluran (1-1,5%) și rocuroniu (0,1 mg/Kg/40 min) la FiO2 de 40%. Paracetamol intravenos (2 g) și Ketorolac (40 mg) au fost administrate înainte de sfârșitul intervenției chirurgicale.
Pacienții au fost ventilați mecanic folosind aparatul de anestezie Maquet (Flow-i). Managementul nostru ventilator a inclus: ventilație controlată de volum, volum mare mare (6-8 ml/Kg LBW), presiune expiratorie pozitivă finală (PEEP) 8-10 mmH2O și frecvență respiratorie adoptată pentru a menține CO2 mare-final între 30 și 35 mmHg [ 7]. Nu au fost utilizate manevre de recrutare la pacienții noștri.
Pacienții au fost alocați aleatoriu în studiul nostru dublu-orb folosind secvența generată de computer în două grupuri: 1- grupul cu dexmedetomidină (n = 21): a primit dexmedetomidină (Precedex, Hospira, Lake forest, IL, SUA) într-o doză de (1μg/Kg LBW) bolus la 15 minute după intubația endotraheală, urmată de 0,5 μg/Kg/oră perfuzie continuă timp de 90 min. 2- Grup de control (n = 21): a primit 1 ml soluție salină normală urmată de perfuzie salină normală continuă timp de 90 min. Studiul medicamentos a fost pregătit și rata de perfuzie a fost calculată de un asistent de cercetare pentru a asigura orbirea investigatorului.
La sfârșitul operației, izofluranul a fost întrerupt, blocul neuromuscular rezidual a fost inversat folosind neostigmină (0,05 mg/kg) și atropină (0,02 mg/kg), apoi pacientul a fost extubat. În unitatea de îngrijire postanestezică (PACU), pacientul a fost monitorizat de monitoare de bază (pulsoximetrie, monitor neinvaziv de tensiune arterială și ECG). Pacienții cu saturație de oxigen mai mică de 88% pe mască de oxigen de 6 l au fost admiși la secția de terapie intensivă.
Conformitatea pulmonară dinamică a fost calculată folosind aparatul de anestezie Maquet ca: volum mareic ((presiunea maximă a căilor respiratorii - PEEP). Complianța statică a plămânilor a fost calculată ca: Volumul mareic ((presiunea platoului - PEEP). Presiunea platoului a fost calculată prin creșterea pauzei de inspirație finală la 30-40%. Spațiul mort fiziologic a fost calculat prin ecuația Hardman și Aitkenhead [8]: Vd/Vt = 1,14 (PaCO2 - EtCO2)/PaaCO2-0,005.
Rezultatul primar
Oxigenarea până la sfârșitul perfuziei de medicament din studiu (evaluată prin raportul P/F: PaO2/Fracția de oxigen inspirat).
Rezultate secundare
Oxigenarea intraoperatorie, complianța pulmonară (statică și dinamică), spațiul mort (Vd/VT) și PaCO2 (5 minute după intubația și poziționarea endotraheală, la 45 de minute și la 90 de minute după începerea perfuziei cu medicament).
Frecvența cardiacă, tensiunea arterială sistolică (SBP), tensiunea arterială diastolică (DBP) și presiunea căilor respiratorii din platou (la momentul inițial, apoi la fiecare 15 minute timp de 2 ore).
Date demografice (vârstă - sex - IMC - fumat - comorbidități), date operatorii (timp chirurgical - lichide intraoperatorii - pierderi de sânge), necesitatea UTI postoperatorie, necesitatea ventilației mecanice postoperatorii, complicații postoperatorii și scala de sedare Pasero opioid indusă [9].
Modificarea fiecărui raport P/F și a conformității pulmonare dinamice (ratio Raport P/F: raport P/F până la sfârșitul perfuziei de studiu - raport P/F la momentul inițial, Δ conformitate: complianță pulmonară dinamică până la sfârșit perfuziei medicamentului din studiu - complianță pulmonară dinamică la momentul inițial)
Δ spațiu mort (%): spațiu mort până la sfârșitul perfuziei de medicament din studiu - spațiu mort la momentul inițial/spațiu mort până la sfârșitul perfuziei de medicament din studiu%).
Calculul dimensiunii eșantionului
Într-un studiu pilot pe 10 pacienți, am raportat un raport P/F intraoperator de 310 ± 32 la pacienții cu obezitate morbidă supuși operațiilor bariatrice. Folosind software-ul MedCalc versiunea 14.10.2 (MedCalc Sofware bvba, Ostend, Belgia), am calculat o dimensiune conservativă a eșantionului care ar putea detecta o diferență de 10% în raportul P/F (adică 31) între cele două grupuri de studiu. Un număr minim de 36 de pacienți (18 pacienți pe grup) a fost calculat pentru a avea o putere de studiu de 80% și o eroare alfa de 0,05. Numărul a fost crescut la 41 de pacienți (21 de pacienți pe grup) pentru a compensa eventualele abandonuri.
analize statistice
Pachetul statistic pentru software-ul de științe sociale (SPSS), versiunea 15 pentru Microsoft Windows (SPSS inc., Chicago, iL, SUA) a fost utilizat pentru analiza datelor. Datele categorice (incidența complicațiilor și comorbidităților) au fost prezentate ca frecvență (%) și analizate prin testul chi pătrat. Datele continue au fost verificate pentru normalitate folosind testul Shapiro-Wilk și au fost prezentate ca medie (deviație standard) sau mediană (interval intercuartil), după caz. Datele continue (raportul PF, complianța, spațiul mort, vârsta, pierderea de sânge etc.) au fost analizate folosind testul t nepereche sau Mann Whitney după caz. Măsurile repetate (tensiunea arterială, ritmul cardiac, presiunea platoului) au fost analizate folosind analiza varianței (ANOVA) pentru măsuri repetate cu comparații perechi post-hoc folosind testul Boneferroni. A P valoarea mai mică de 0,05 a fost considerată semnificativă statistic.
Rezultate
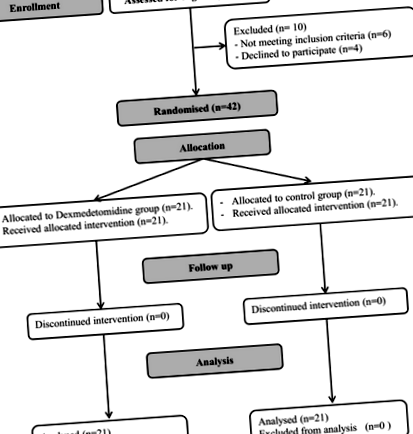
Patruzeci și doi de pacienți au fost disponibili pentru analiza finală (Fig. 1). Datele demografice și caracteristicile de bază au fost comparabile între ambele grupuri de studiu (Tabelul 1). Funcțiile pulmonare preoperatorii au fost, de asemenea, comparabile între cele două grupuri de studiu (Tabelul 1). La 90 de minute, s-a înregistrat o îmbunătățire semnificativă atât a raportului P/F, cât și a complianței pulmonare în cadrul grupului cu dexmedetomidină, comparativ cu citirea inițială. Ratio Raportul P/F a fost semnificativ mai mare în grupul cu dexmedetomidină comparativ cu grupul de control P = 0,046) (Tabelul 2).
Diagrama recrutării pacienților
Comparativ cu grupul de control, grupul cu dexmedetomidină a prezentat o complianță pulmonară dinamică mai mare la ambele 45 min 2O - 1 Vs 34,6 (5) mL cmH2O - 1, P = 0,004> și 90 min 2O - 1 Vs 34,5 (6) mL cmH2O - 1, P - 1 versus - 1 (4) mL cmH2O - 1, P = 0 - 1 Vs 45 (11) mL cmH2O - 1, P = 0,01>; în timp ce ambele grupuri au prezentat complianță statică pulmonară comparabilă în alte momente (Tabelul 2).
Spațiul mort a crescut semnificativ în grupul de control la 45 min și 90 min comparativ cu linia de bază; în timp ce spațiul mort a scăzut în grupul cu dexmedetomidină la 90 de minute comparativ cu măsurarea inițială și cu grupul martor (Tabelul 2). Space spațiul mort (%) a fost semnificativ mai mic în grupul cu Dexmedetomidină comparativ cu grupul de control P = 0,01> (Tabelul 2). Presiunea platoului a fost mai mică în grupul cu dexmedetomidină, comparativ cu grupul martor la majoritatea măsurătorilor (Fig. 2).
Presiunea platoului. * denotă semnificație între ambele grupuri
Atât SBP cât și DBP au fost mai mici în grupul cu dexmedetomidină, comparativ cu grupul de control și comparativ cu linia de bază în majoritatea măsurătorilor (Fig. 3). Frecvența cardiacă a fost, de asemenea, mai mică în grupul cu Dexmedetomidină, comparativ cu grupul martor la 15 min și cu valoarea inițială la 60, 75, 90 și 105 min (Fig. 4).
Tensiunea arterială sistolică și diastolică. * denotă semnificație între ambele grupuri, † denotă semnificație comparativ cu citirea inițială în grupul dexmedetomidină
Ritm cardiac. * denotă semnificație între ambele grupuri, † denotă semnificație comparativ cu citirea inițială în cadrul grupului cu dexmedetomidină
Discuţie
Infuzia cu dexmedetomidină a îmbunătățit oxigenarea și mecanica pulmonară la pacienții obezi morbid cu boli pulmonare restrictive. Grupul cu dexmedetomidină a prezentat un raport P/F mai mare, o conformitate mai mare, un spațiu mort mai scăzut și o presiune mai mică a platoului, comparativ cu grupul de control.
Atunci când este utilizată ca agent sedativ, dexmedetomidina a dus la o mai bună sincronizare pacient-ventilator [15] și mai multe ore libere de ventilator [16] la adulții bolnavi critici. Dexmedetomidina scurtase procesul de înțărcare la copiii bolnavi critici [17]. Dexmedetomidina a îmbunătățit oxigenarea și mecanica pulmonară în timpul OLV în chirurgia toracică [10, 12] și la pacienții cu BPOC supuși unei intervenții chirurgicale cu cancer pulmonar [3]. Dexmedetomidina a avut un efect protector împotriva leziunilor pulmonare independente în timpul OLV [13]. Dexmedetomidina a îmbunătățit oxigenarea alveolară atunci când este utilizată pentru inducerea anesteziei la copii cu tetralogia Fallot [18]. În bolile restrictive ale plămânilor, datele disponibile au fost extrase din studiile pe animale. Comparativ cu Propofol, administrarea dexmedetomidinei a dus la caracteristici pulmonare mai bune la șobolani cu obezitate experimentală [4]. Dexmedetomidina a avut un efect protector al șobolanilor cu leziuni pulmonare induse de lipopolizaharide [14, 19]. Din câte știm, acest studiu este primul care a investigat efectul dexmedetomidinei asupra oxigenării și mecanicii pulmonare la pacienții cu boli pulmonare restrictive.
Conform caracteristicilor inițiale, toți pacienții noștri au prezentat un model izolat de boală pulmonară restrictivă fără dovada unui model obstructiv. Astfel, descoperirile noastre declară un efect relativ nou al perfuziei de dexmedetomidină asupra mecanicii respiratorii la populația pacienților obezi morbid cu boli pulmonare restrictive. Acest efect nu a fost raportat anterior la oameni. Efectele favorabile pentru dexmedetomidină asupra oxigenării și mecanicii pulmonare la pacienții noștri au fost moderate; am raportat o îmbunătățire de aproape 10% a raportului P/F după perfuzia de dexmedetomidină de 90 de minute. Lee și colab. a raportat o îmbunătățire similară a oxigenării și mecanicii pulmonare la pacienții cu BPOC supuși unei intervenții chirurgicale cu cancer pulmonar [3]. Durata mai lungă (și/sau dozele mai mari) ar putea duce la rezultate mai semnificative. Mai mult, această îmbunătățire moderată ar putea avea o valoare mai mare la pacienții cu stare respiratorie compromisă în sala de operație și unitatea de terapie intensivă. Cu toate acestea, această ipoteză trebuie confirmată prin studii controlate randomizate.
Doar cinci dintre pacienții noștri (12%) au prezentat hipoxie postoperatorie în PACU care a avut nevoie de internare în UCI. Deși nu a existat nicio diferență semnificativă între ambele grupuri de studiu în ceea ce privește necesitatea postoperatorie de terapie intensivă, nu am putut generaliza această constatare deoarece studiul nostru nu a fost suficient de puternic pentru a o judeca.
Limitări de studiu
Studiul nostru a avut unele limitări. În primul rând: am folosit o singură doză de dexmedetomidină timp de 90 de minute. Acest lucru se datorează faptului că am considerat studiul nostru ca un studiu exploratoriu pentru efectul dexmedetomidinei la această populație. Pe baza rezultatelor noastre, recomandăm mai multe studii pentru a investiga dacă aceste efecte pot diferi cu doze diferite și cu o durată mai mare de perfuzie. În al doilea rând: utilizarea ecuației Hardman și Aitkenhead pentru calcularea spațiului mort fiziologic; aceasta deoarece capnografia volumetrică nu era disponibilă în unitatea noastră. În al treilea rând: nu am folosit manevre de recrutare pulmonară; aceasta s-a bazat pe ceea ce Defresne și colab. raportase la pacienții cu obezitate morbidă în timpul intervenției chirurgicale de bypass gastric laparoscopic [20].
Concluzie
O perfuzie de dexmedetomidină de 90 de minute a dus la o îmbunătățire moderată a oxigenării și a mecanicii pulmonare la pacienții obezi morbid cu boală pulmonară restrictivă.
- Dificultăți în gestionarea tuberculozei ganglionare Gupta P R - Lung India
- Efectele frontierelor unei diete de patru săptămâni cu doze mari de oxid de zinc, suplimentate cu Escherichia comensală
- Efectele frontierelor dietelor bogate în fructoză asupra semnalizării apetitului central și a funcției cognitive
- Efectele secundare ale diflucanului cresc riscul de avort spontan, studiul defectelor congenitale cardiace
- Observarea directă a activității fizice și a comportamentelor dietetice într-un mediu structurat Efecte