Termeni asociați:
- Boala Crohn
- Colită ulcerativă
- Enterită
- Boala inflamatorie a intestinului
- Colangita sclerozantă primară
- Colita
- Intestinul subtire
- Ileum
- Hamster
Descărcați în format PDF
Despre această pagină
Boli bacteriene și fungice
fundal
Ileita proliferativă este o boală infecțioasă gravă a hamsterilor și de obicei duce la morbiditate și mortalitate ridicate. Boala se caracterizează clinic prin diaree la hamsterii înțărcați și patologic prin leziuni proliferative segmentare ale epiteliului ileonului terminal. Boala, ileita proliferativă, a fost, de asemenea, denumită enterită regională, ileită terminală, adenocarcinom intestinal enzootic, hiperplazie ileală atipică, enterită de hamster și „coadă umedă”. Toate sinonimele de mai sus descriu același sindrom de boală, care va fi denumit ileită proliferativă în acest capitol. Termenul „coadă umedă” a fost folosit, în special în industria animalelor de companie, pentru a desemna această boală. Cu toate acestea, acest aspect clinic descriptiv poate fi cauzat de mai multe afecțiuni care pot provoca diaree; și, astfel, utilizarea termenului poate duce la confuzie. Literatura despre ileita proliferativă a fost revizuită de mai mulți autori (Cooper și Gebhart, 1998; Frisk, 1987; Frisk și Wagner, 1977b; Jacoby și Johnson, 1981; Lawson și Gebhart, 2000).
Primul focar major de ileită proliferativă înregistrat în literatură a fost în 1958 (Friedman, 1965). Boala naturală la hamsteri a fost raportată doar din America de Nord (Jasni și colab., 1994b). Căutarea agentului etiologic al ileitei proliferative a hamsterilor a inclus multe studii diagnostice și experimentale. În trecut, speculațiile cu privire la cauza leziunilor hiperplazice caracteristice includeau bacterii (Amend și colab., 1976; Booth și Cheville, 1967; Friedman, 1965; Frisk și colab., 1981; Jacoby și Johnson, 1981; Jacoby și colab. ., 1975; La Regina și Lonigro, 1982; Lentsch și colab., 1982; Wagner și colab., 1973), viruși (Tomita și Jonas, 1968) și nutriție (Goldman și colab., 1972). O analiză a studiilor timpurii referitoare la căutarea agentului cauzal a fost făcută de Frisk (1987). Din anii 1980, cercetările privind ileita proliferativă s-au concentrat aproape exclusiv pe identificarea organismului intracitoplasmatic observat în celulele epiteliale ileale afectate. Identificarea acestui organism a fost foarte dificilă din cauza incapacității sale de a fi propagat pe medii artificiale. Acest organism a fost în cele din urmă caracterizat și numit Lawsonia intracellularis (McOrist și colab., 1995).
S-a demonstrat că mai multe organisme intestinale acționează ca oportuniste la hamsterii cu ileită proliferativă, inclusiv Campylobacter jejuni (Lentsch și colab., 1982), Escherichia coli enteropatogenă (Frisk și colab., 1978), Chlamydia trachomatis (Fox și colab., 1993), Cryptosporidium sp. (Davis și Jenkins, 1986) și paraziți protozoare (Boothe și Cheville, 1967; Jackson și Wagner, 1970; Sheffield și Beveridge, 1962). Agenții bacterieni și paraziți enumerați mai sus nu sunt prezenți în mod constant în toate cazurile de ileită proliferativă și pot fi observați sau izolați de hamsteri fără leziuni proliferative. De asemenea, leziunile tipice ale ileitei proliferative pot fi produse experimental fără prezența acestor agenți (Amend și colab., 1976; Johnson și Jacoby, 1978; Stills, 1991).
Intestin și mezenter pediatric
Marilyn J. Siegel, Edward Y. Lee, în Ultrasunete clinice (ediția a treia), 2011
Ileita terminală acută
Ileita terminală acută poate fi cauzată de Yersinia enterocolitica, Campylobacter jejuni, Salmonella tifus și sindromul Behçet, deși pot produce de obicei o gastroenterită ușoară. În ileita terminală acută, durerea abdominală poate imita apendicita. 58 Ileonul distal și colonul sunt locurile comune de implicare.
Îngroșarea pereților intestinului subțire
Boala Crohn este cea mai frecventă boală inflamatorie intestinală la copii.
Constatările bolii Crohn sunt o structură tubulară parțial compresibilă, ne-orbitoare, pe vederi cu ax lung și aspectul ochi de taur pe vederi cu ax scurt.
Descoperirile ileitei terminale acute sunt un perete îngroșat sărac, peristaltism diminuat și ganglioni limfatici mezenterici măriți.
Constatările hemoragiei peretelui intestinal sunt îngroșarea pereților cu ecotextură variabilă în funcție de vârsta hematomului.
Hematoamele acute sunt mai reflective decât hematoamele cronice.
Grosimea peretelui intestinului în bolile inflamatorii și hemoragice este
La pacienții care prezintă simptome care imită apendicita, ecografia poate sugera diagnosticul ileitei acute acute nebănuite. 58.59 Rezultatele ecografice sunt similare cu cele ale bolii Crohn, incluzând un perete îngroșat sărac, peristaltism diminuat și ganglioni limfatici mezenterici măriți. Nodurile au de obicei un diametru cuprins între 7 și 21 mm și sunt sărace în ecou, cu un centru foarte reflectorizant. 59 Doppler color arată un flux crescut în mucoasa inflamată. 54,55 Un diagnostic specific al bolii infecțioase sau inflamatorii a intestinului necesită cultura scaunului sau prelevarea de probe de țesut.
Prezentare generală a histopatologiei colitei ulcerative și a bolii Crohn
Trăsături neobișnuite ale colitei ulcerative
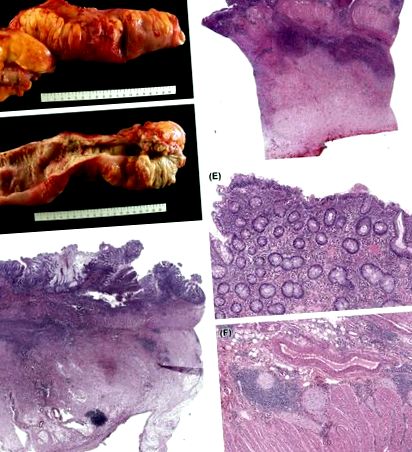
Figura 5.5. Caracteristici macroscopice și microscopice ale bolii Crohn. (A) Examenul macroscopic relevă un segment intestinal strict cu înveliș de grăsime; (B) specimenul nu este întins la deschidere; (C) imaginile microscopice din acest specimen de rezecție dezvăluie un proces inflamator care implică toată grosimea colonului; Vederile cu putere mai mare (D - F) dezvăluie ulcerul fisural și abcesul mural (D), colita cronică activă (E) și plexita neuronală (F).
(A și B) Imagine oferită de dl. Robin M. Foss.
Ulceratia fisuratoare si inflamatia transmurala: Deși UC este de obicei superficială, cu inflamație limitată la mucoasă, specimenele de rezecție din cazurile cu boli severe pot prezenta inflamații care se extind dincolo de mucoasă. De exemplu, ulcerația de fisurare superficială, definită ca o fisură verticală asemănătoare cuțitului căptușită de țesutul de granulație care se extinde în aspectul superficial (jumătatea interioară) a muscularis propria, este considerată a fi o caracteristică a CD. Cu toate acestea, prezența sa singură la pacienții cu colită difuză severă nu ar trebui să determine un diagnostic de CD. 21 Inflamația transmurală poate fi găsită la pacienții cu UC fulminantă, fie într-o formă neagregată și cu grosime completă cu un model celular mixt, fie un model transmural de agregate limfocitare în regiunile cu ulcerație severă. 22
Implicarea tractului GI superior în UC: Aproximativ 4% dintre copiii cu UC prezintă constatări GI superioare, mai frecvent inflamații, eroziuni și ulcerații la nivelul stomacului și, rareori, ulcerații la nivelul duodenului și esofagului. 13 În general, cele mai frecvente constatări ale GI superioare în UC includ gastrită focală, inflamație gastrică bazală mixtă, plasmocitoză gastrică superficială și duodenită cronică difuză, iar aceasta din urmă poate prezice pouchita. 23 Gastrita intensificată focal, o colecție de limfocite T, histiocite și/sau granulocite care implică una sau doar câteva glande gastrice, este o constatare frecventă în CD. 24 Cu toate acestea, Ushiku și colab. au constatat că până la 30% dintre pacienții pediatrici cu UC pot avea gastrită focal îmbunătățită și că mai multe gropi sau glande gastrice tind să fie implicate de inflamație în UC decât în DC. 25
Infecție suprapusă asupra UC: Pacienții cu UC pot prezenta simptome agravante care pot fi atribuite în totalitate sau complet lipsite de o exacerbare a IBD. De exemplu, pacienții cu UC pot avea colită asociată cu Clostridium difficile sau o infecție citomegalovirală (CMV) suprapusă, care face simptomele bolii refractare la tratamentul medical. Terapia antivirală poate aduce beneficii unui subgrup de pacienți cu UC care sunt refractari la corticosteroizi. Astfel, incluziunile CMV ar trebui excluse în mod activ la biopsiile intestinale luate de la pacienții cu IBD. Într-un studiu, cinci sau mai multe celule pozitive cu imunohistochimie CMV (IHC) pe secțiune de biopsie au indicat un risc mai mare de colectomie. 27 De asemenea, este demn de remarcat faptul că CMV IHC poate fi o metodologie excelentă pentru detectarea CMV în materialul de biopsie GI atunci când histologia este echivocă.
- Hipuricemia - o prezentare generală Subiecte ScienceDirect
- Circulația hiperdinamică - o prezentare generală Subiecte ScienceDirect
- Ciuperci medicinale - o prezentare generală Subiecte ScienceDirect
- Leukoencefalopatia - o privire de ansamblu asupra subiectelor ScienceDirect
- Jejunoileostomia - o prezentare generală a subiectelor ScienceDirect