Când Michelle Obama a lansat-o Let’s Move! campanie împotriva obezității la copii în 2010, a venit pe baza datelor care arată că 36% din S.U.A. adulții și 17% dintre copiii și adolescenții din SUA erau obezi (1). Riscurile asociate sănătății subliniate de dna. Echipa lui Obama a reflectat consensul Centrelor pentru Controlul și Prevenirea Bolilor, care a evidențiat o multitudine de rezultate adverse, de la cancer la artrită și la boala coronariană. Printre aceste mesaje de sănătate publică, consecințele neuropsihiatrice ale obezității s-au concentrat în mod restrâns asupra bolilor cerebrovasculare, cum ar fi accidentul vascular cerebral, și consecințele psihologice ale stigmatizării. Cu toate acestea, studii la scară largă care arată o asociere între obezitate, diabet și demență indică faptul că creierul este afectat mai larg (2,3).
Conexiunea demență-obezitate-diabet face parte dintr-o poveste în evoluție care ne obligă să reexaminăm o conceptualizare de lungă durată a minții și a corpului ca fiind separate. Când René Descartes a scris faimos despre dualismul minte-corp în secolul al XVII-lea, el reformula idei care erau vechi chiar și pentru el. Acum se înțelege că cunoașterea, afectul, memoria și alte procese mentale sunt manifestări ale funcției creierului. Deși neuroștiința contemporană a demontat în mare măsură dihotomia lui Descartes, dualismul creier-corp continuă să existe, dovadă fiind sistemele de îngrijire a sănătății practic separate, dedicate sănătății mintale și fizice.
Acest lucru are implicații importante pentru modul în care abordăm tulburările fizice și mentale aparent disparate, dificil de tratat. Relația dintre diabet și demență este exemplul perfect. Aplicarea unui etos al dualismului creier-corp la această problemă sugerează că depinde de interniști și endocrinologi să abordeze obezitatea și diabetul, în timp ce psihiatrii și neurologii se ocupă de tulburările neurocognitive. Cu toate acestea, o înțelegere științifică a acestor tulburări sugerează că descompunerea acestor silozuri poate duce la descoperiri patologice și terapeutice importante.
Deci, cum contribuie obezitatea sau diabetul la o creștere cu 50% a riscului de demență? Care este legătura dintre greutate, metabolism și sănătatea creierului? O legătură cheie poate fi impactul inflamației și al stresului oxidativ asupra creierului. Zeci de ani de studiu asupra unei game largi de boli, inclusiv cancer și boli de inimă, au demonstrat că inflamația și stresul oxidativ joacă un rol major în patologia umană. Multe dintre aceleași procese care afectează arterele coronare și organele viscerale au un impact asupra creierului. Inflamația duce la activarea microgliei și a astrocitelor. Acest lucru determină eliberarea citokinelor și a oxidanților reactivi, ducând în cele din urmă la disfuncții neuronale sau la moarte. În mod critic, acest proces poate declanșa un ciclu vicios: neuronii pe moarte pot provoca mai multe inflamații, creând astfel o cascadă de neurodegenerare (4).
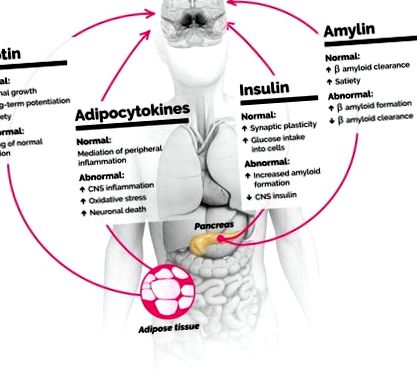
Atât diabetul, cât și obezitatea cresc inflamația sistematic. Până nu demult, se credea că bariera hematoencefalică (BBB) protejează creierul de astfel de efecte sistemice. Acum știm că creierul este afectat semnificativ de starea inflamatorie a obezității/diabetului prin mai multe căi. În primul rând, mulți dintre mediatorii inflamatori sistemici - citokinele, de exemplu - traversează BBB în anumite condiții. În al doilea rând, mediatorii metabolici eliberați de țesutul adipos și de pancreas - leptina, insulina și amilina - au roluri suplimentare importante în medierea inflamației sistemului nervos central (SNC) și reglarea sănătății neuronale. Analizarea unora dintre detaliile a ceea ce se întâmplă exact cu creierul în diabet și obezitate (Figura 1) poate oferi noi ținte pentru tratamentele cu demență.
Mediatorii metabolici și inflamatori eliberați de țesutul adipos și de pancreas au impact asupra creierului atât în sănătate, cât și în boală. Diabetul și obezitatea pot contribui la demență prin intermediul acestor mediatori. SNC, sistemul nervos central.
Deși adesea considerat inert, acum ne dăm seama că grăsimea în sine poate juca un rol major în reglarea sănătății cognitive. Țesutul adipos servește o serie de funcții neuroendocrine. Una dintre cele mai importante funcții este producerea și eliberarea unei game de polipeptide numite adipokine. Acestea au o gamă largă de efecte, de la modularea metabolismului (prin leptină), medierea coagulării sângelui (prin inhibitori de activare a plasminogenului) și reglarea căii inflamatorii (inclusiv prin interleukine și factori de necroză tumorală) (5). La persoanele sănătoase din punct de vedere metabolic, secreția de adipokine este adaptată nevoilor fiziologice. Cu toate acestea, în obezitate, mediul adipokinic intră într-o stare uneori cunoscută sub numele de adiposopatie, în care citokinele inflamatorii, cum ar fi interleukina-6, sunt secretate la niveluri superioare, iar mediatorii metabolici, cum ar fi leptina, încetează să funcționeze corect.
Cercetările arată că modificările patologice ale adiposopatiei au efecte majore asupra creierului. Inflamația periferică perturbă BBB și poate împiedica plasticitatea sinaptică și neurogeneza hipocampului; citokinele precum interleukina-6 pot duce la scăderea volumului de substanță cenușie hipocampală (5). Interesant este faptul că predominanța descoperirilor hipocampice la începutul evoluției bolii Alzheimer poate fi legată de sensibilitatea sa la întreruperile din BBB (6). Deoarece inflamația dăunează structurilor responsabile de învățare, memorie și cunoaștere, efectele neurocognitive pozitive ale leptinei sunt diminuate.
Leptina este cunoscută mai ales pentru reglarea sațietății și a aportului de energie. Cu toate acestea, promovează și creșterea axonală și îmbunătățește potențarea pe termen lung prin modularea funcției N-metil-D-aspartat. Aceste caracteristici sugerează importanța sa în memorie și învățare. Stările de obezitate sunt asociate cu rezistența la leptină. Rezistența la efectele leptinei nu se limitează la capacitatea sa de a regla alimentația - poate, de asemenea, să plictisească rolul leptinei în îmbunătățirea cognitivă (7).
La fel ca în cazul țesutului adipos, peptidele pancreatice au, de asemenea, roluri importante în creier. În timp ce insulina este cunoscută mai ales pentru rolul său în aportul celular de glucoză, cercetările privind rolul său în cunoaștere capătă impuls. Receptorii insulinei sunt implicați în învățare și memorie, cu concentrații mari de receptori în cortex și hipocamp. În plus, insulina (și factorul de creștere asemănător insulinei 1) acționează ca factori neurotrofici care promovează plasticitatea sinaptică (4).
În diabetul de tip 2, corpul devine rezistent la insulină, forțând pancreasul să producă cantități din ce în ce mai mari de insulină pentru a promova absorbția glucozei de către celule. Așa cum este cazul leptinei, rezistența sistemică la insulină estompează efectele procognitive ale insulinei în creier: rezistența la insulină este asociată cu o fluență verbală scăzută, un volum scăzut de substanță cenușie în lobii temporali și tulburări de memorie declarative (4). Mai mult, transportul insulinei în creier poate fi subregulat de rezistența la insulină periferică și acest lucru poate afecta metabolismul glucozei în SNC, poate contribui la stresul oxidativ și poate inhiba efectele neurotrofice ale insulinei. În același timp, deoarece cantitățile absolute de insulină sunt din ce în ce mai mari (deși efectul este mai mic), hiperinsulinemia duce la formarea de plăci amiloid-β periferice și centrale similare celor observate în neuropatologia bolii Alzheimer și a altor tulburări neurodegenerative. Aceste plăci pot activa inflamația în SNC, ducând la moarte neuronală suplimentară și la formarea plăcii (4).
O altă piesă a poveștii poate proveni din amilină, un hormon produs în principal de pancreas. La fel ca leptina, amilina funcționează pentru a regla metabolismul energetic prin scăderea aportului de energie/creșterea sațietății. În acest număr al Psihiatriei biologice, Reiner și colab. (8) explorați cum este mediat acest efect. Un studiu separat din 2014 a arătat că în rândul persoanelor în vârstă, amilina plasmatică este corelată pozitiv cu sănătatea cognitivă, chiar și după controlul altor factori de risc metabolici, cum ar fi diabetul și hiperlipidemia (9). În plus, descoperirile preliminare sugerează că amilina ar putea concura cu proteinele patologice amiloid-β pentru situsurile de legare a receptorilor și chiar ar ajuta la eliminarea amiloidului SNC (10). Aceste date sugerează că neregularizarea amilinei, așa cum se observă la obezitate și diabet, ar putea contribui la acumularea de plăci β-amiloid (și inflamație ulterioară și moarte neuronală) observate în boala Alzheimer.
Mulțumiri
Acest comentariu a fost produs în colaborare cu Inițiativa Națională a Curriculumului în Neuroștiințe. Această lucrare a fost susținută de Institutul Național de Sănătate nr. R25 MH10107602S1 și R25 MH086466 07S1 (către MRA, în rolul ei de copreședinte al Inițiativei Curriculumului Național în Neuroștiințe).
Mulțumim Dr. David Ross pentru contribuțiile sale ca editor al inițiativei Curriculum National Neuroscience și Amanda Wang pentru rolul său în dezvoltarea figurii.
- Îmbunătățirea recomandărilor dietetice pentru pacienții cu diabet de tip 2 și obezitate într-o endocrinologie
- Mediul matern și ciclul transgenerațional de obezitate și diabet Diabet
- Specialist în hipoglicemie - Modesto, CA Gopika Gangupantula, MD, FAAFP, BC-ADM Diabet și obezitate
- Hipertensiunea, obezitatea escaladează pierderea memoriei la persoanele cu risc de boală Alzheimer
- Este apa dvs. responsabilă pentru obezitate și diabet Monarch Manor