K E A Lundin
1 Departamentul de Medicină, Rikshospitalet, Oslo, Norvegia
E M Nielsen
2 LIIPAT, Institutul de Patologie, Rikshospitalet și Universitatea din Oslo, Oslo, Norvegia
H G Scott
3 Departamentul de patologie, Rikshospitalet, Oslo, Norvegia
E M Løberg
4 Departamentul de patologie, Spitalul Universitar Ullevaal, Oslo, Norvegia
A Gjøen
5 Departamentul de Medicină, Spitalul Universitar Ullevaal, Oslo, Norvegia
J Bratlie
6 Institutul de Cercetări Medicale, Rikshospitalet și Universitatea din Oslo, Oslo, Norvegia
În Scar
7 Departamentul de Medicină, Spitalul Lovisenberg, Oslo, Norvegia
E Mendez
8 Unidad de Analisis Estructural Proteinas, Centro Nacional de Biotechnologica, CSIC, Madrid, Spania
Un Løvik
1 Departamentul de Medicină, Rikshospitalet, Oslo, Norvegia
K Kett
1 Departamentul de Medicină, Rikshospitalet, Oslo, Norvegia
Abstract
Tratamentul bolii celiace (CD) sa bazat pe excluderea dietetică a proteinelor din grâu, orz, secară și ovăz. Excluderea ovăzului s-a bazat pe experimente de hrănire timpurie, dar este cu siguranță posibil ca produsele din ovăz utilizate în unele dintre aceste studii să fie contaminate de alte cereale. Există, totuși, mai multe motive pentru a include ovăzul în dieta pacienților cu CD. Ovăzul poate crește gustul dietei și ar servi ca o sursă valoroasă de fibre într-o dietă care este, în general, deficitară în fibre.
Posibilul efect nociv al ovăzului a fost revizuit recent. Într-un studiu amplu, 92 de pacienți cu CD au fost randomizați la o dietă standard fără gluten sau la o dietă similară cu ovăz. Mucoasa intestinului subțire nu a fost afectată de ovăz, iar normalizarea serologică nu a fost întârziată. 2 Unsprezece pacienți s-au retras în timpul studiului. Pacienții au fost reevaluați după cinci ani. 3 Din 35 de pacienți din grupul original cu ovăz, 23 mâncau încă ovăz. Nu s-a arătat niciun efect nociv al ovăzului. Într-un studiu mai mic pe 10 pacienți cu CD, ovăzul a fost, de asemenea, bine tolerat. 4, 5 Un studiu suedez în care au fost urmăriți 20 de pacienți cu CD tratați timp de doi ani a arătat că tolerează cantități mari de ovăz (100 g/zi). 6 Cinci pacienți s-au retras din studiu. Au fost raportate și studii care sugerează că ovăzul este sigur pentru pacienții cu dermatită herpetiformă. 7, 8 Au fost solicitate studii clinice suplimentare.
PACIENTI ȘI METODE
Testarea purității ovăzului
O serie de produse comerciale cu ovăz au fost testate pentru contaminarea grâului printr-un kit de imunoanaliză legată de enzime (ELISA) care detectează wheat-gliadina de grâu (Ridascreen; Food Diagnostics, Oslo, Norvegia). Metoda a fost dezvoltată de Skerritt și Hill. 9 Trusa ELISA identifică, de asemenea, secara și, într-o măsură mult mai mică, orz și ovăz. Unele probe de ovăz au fost, de asemenea, testate prin western blot, spectrometrie de masă și ELISA, așa cum este descris în altă parte. 10-12 Un total de 120 de probe de ovăz de la producătorul ales pentru provocarea noastră clinică au fost, de asemenea, testate cu un kit similar (BioKits; Tepnel, Manchester, Marea Britanie) la Institutul Veterinar, Oslo, Norvegia (rezumat în limba engleză: http: // www.snt.no/dokumentasjon/rapporter/snt_rapporter/200202.html). Acest kit folosește același anticorp monoclonal ca și kitul Ridascreen, dar a fost produs de un alt producător.
Provocare clinică
Nouăsprezece pacienți adulți cu CD (doi bărbați) au participat la studiu. Toți fuseseră diagnosticați cu CD pe bază de atrofie viloasă duodenală, urmată de îmbunătățiri clinice și histologice pe o dietă standard fără gluten. Toți au avut o biopsie de control efectuată la o urmărire clinică în ultimele 12 luni înainte de provocarea clinică. Ora biopsiei de pre-provocare este prezentată în tabelul 2 ▶. Înainte de a începe să consume ovăz, voluntarii s-au supus unui test standard de respirație 13 C-d-xiloză. Simptomele gastrointestinale și aportul de alimente au fost măsurate înainte, în timpul provocării și după sfârșitul studiului la 12 săptămâni. Aportul zilnic de ovăz a fost de 50 g. În ultima zi a perioadei de provocare, s-a efectuat un nou test de respirație 13 C-d-xiloză și o gastroduodenoscopie folosind un obiectiv Olympus GIF-T140 și s-au obținut biopsii cu forceps jumbo. Biopsiile au fost punctate în conformitate cu criteriile propuse de Marsh și modificate de Oberhuber și colegi. 13 anticorpi IgA antigliadin (AGA), anticorpi antiendomisium (EMA) și ulterior și transglutaminază antitissue (tTG) au fost analizați într-un laborator de rutină (Fürst’s Laboratorium, Oslo, Norvegia). Studiul a fost aprobat de comitetul de etică regional. Toți participanții au dat consimțământ scris în cunoștință de cauză.
masa 2
Scorul de mlaștină și nivelurile de IFN-γ înainte și după provocarea cu ovăz
| Pacientul nr | GFD (y) | Prebiopsie (luni) | Scorul de mlaștină (înainte) | IFN-γ (înainte) | Scorul de mlaștină (după) | IFN-γ (după) |
| 1 | 2 | −12 | 0 | 3 | 0 | 3 |
| 2 | 14 | −12 | 1 | 3 | 0 | 3 |
| 3 | 15 | −10 | 0 | 3 | 0 | 3 |
| 4 | 5 | −5 | 3a | 6,5 × 10 4 | 1 | 8,2 × 10 4 |
| 5 | 3 | −6 | 1 | 3 | 3a | 6,0 × 10 4 |
| 6 | 2 | −12 | 0 | 3 | 0 | 3 |
| 7 | 5 | −12 | 0 | 3 | 0 | 3 |
| 8 | 2 | −5 | 0 | 3 | ND | ND |
| 9 | 2 | −2 | 1 | 3 | 1 | 4,3 × 10 4 |
| 10 | 3 | −12 | 3a | 3 | 1 | 3 |
| 11 | 11 | −10 | 1 | ND | 1 | 3 |
| 12 | 3 | −10 | 0 | 3 | 0 | 3 |
| 13 | 2 | −11 | 0 | 3 | 0 | 6,6 × 10 4 |
| 14 | 2 | −12 | 3a | 3 | 3a | 1,3 × 10 5 |
| 15 | 2 | −5 | 1 | 3 | 1 | 3 |
| 16 | 30 | −12 | 0 | 3 | 0 | 3 |
| 17 | 3 | −11 | 0 | 3 | 0 | 3 |
| 18 | 11 | −12 | 0 | 3 | 0 | 3 |
| 19 | 17 | −2 | 0 | 3 | 0 | 3 |
IFN-γ, transcrieri specifice interferonului γ per µg ARN; GFD, dietă fără gluten; ND, nu a fost detectat.
analiza ARNm
Biopsiile au fost înghețate la noptieră în N2 lichid, iar ARN-ul a fost izolat și transcris invers (RT) așa cum s-a descris în altă parte. 14 A fost efectuată o reacție în lanț specifică a polimerazei (PCR) pentru interferon gamma (IFN-γ). Acele probe care au fost pozitive în RT-PCR standard au fost supuse PCR cantitativ. 14
REZULTATE
Puritatea ovăzului
Raport de caz
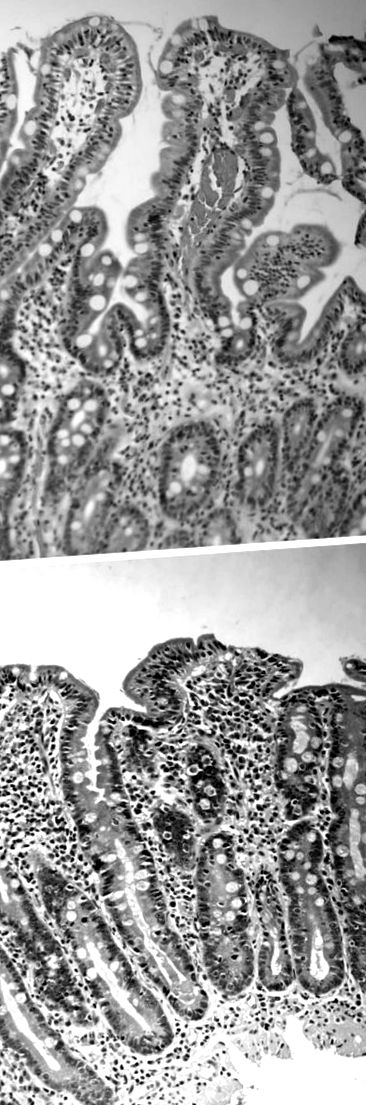
Morfologia intestinului subțire al pacientei nr. 5 din tabelul 2 ▶ înainte (A, leziunea Marsh 1) și după (B, leziunea Marsh 3B) ea consumase ovăz. Colorare hematoxilin-eozină, mărire originală 200 ×.
Urmăriți după 1,5 ani
Pacienților li s-a permis să mănânce ovăz pur după voia lor, după provocarea studiului. După 1,5 ani, 15 pacienți au fost de acord să se întoarcă pentru urmărire, inclusiv gastroduodenoscopie. Dintre acești 15 pacienți, 12 au consumat în mod regulat ovăz, deși de obicei mai puțin de 50 g/zi. Histologia intestinului subțire a fost încă satisfăcătoare (Marsh tip 0 sau Marsh tip 1). Toți au avut serologie normală și și-au exprimat satisfacția cu privire la adăugarea ovăzului în dieta lor. Doi pacienți cu consum de ovăz (nr. 1 și 15 din tabelul 2 ▶) care au fost negativi pentru IFN-γ mARN după perioada de provocare de 12 săptămâni au prezentat un semnal pozitiv la urmărire. Nivelul nu a fost cantitativ, dar nu a fost asociat cu deteriorarea mucoasei.
DISCUŢIE
Aici am arătat că ovăzul cu cel mult o contaminare neglijabilă cu alte cereale este disponibil comercial în Norvegia. Aceste ovăz au fost bine tolerate de majoritatea celor 19 pacienți cu CD tratați într-un studiu provocator. Cu toate acestea, am găsit un pacient cu CD care era intolerant la ovăz.
O problemă importantă cu privire la prezentul studiu se referă la puritatea ovăzului utilizat. Am ales să testăm puritatea ovăzului utilizat în studiu folosind un kit ELISA disponibil comercial. Trusa de testare folosește un anticorp împotriva ω-gliadinei. Acest test detectează grâul și secara, dar într-o măsură mai mică orz. Producătorul ovăzului selectat pentru utilizare în prezentul studiu a luat mai multe măsuri de precauție pentru a evita contaminarea ovăzului cu alte cereale. A fost liniștitor faptul că testarea unui număr mare de 150 de probe nu a reușit să producă un test pozitiv. Având în vedere rezultatul neașteptat al provocării clinice, am testat unele dintre probe cu proceduri mai avansate din punct de vedere tehnic. Am constatat apoi că unul dintre sacii de ovăz era contaminat în partea de sus a sacului, dar nu și în partea de jos. Important, două probe din ovăzul consumat de pacientul nostru cu intoleranță la ovăz s-au dovedit a fi ovăz pur. Luate împreună, este probabil ca ovăzul utilizat în prezentul studiu să fie suficient de pur și să respecte limitele sugerate de limita standard revizuită a Codex de 20 ppm pentru alimentele fără gluten în mod natural. 16
Unele aspecte ale provocării clinice ar trebui discutate. Am ales să provocăm pacienții timp de 12 săptămâni, deoarece această perioadă este comparabilă cu alte studii și era de așteptat să fie suficientă pentru detectarea unui răspuns dăunător. Pentru un singur pacient evident intolerant, timpul de provocare a fost în mod clar suficient. Ea a dezvoltat modificări ale mucoasei și dermatită în timpul provocării. Dermatita seamănă clinic cu dermatita herpetiformă, dar o singură biopsie nu a demonstrat depozitele de IgA tipice acestei boli. Cu toate acestea, chiar dacă un depozit tipic de IgA este un diagnostic de dermatită herpetiformă17, este uneori necesar să se obțină biopsii repetate și chiar pot exista cazuri adevărate negative. 18 Cu toate acestea, dermatita a fost în timp direct legată de consumul de ovăz și a scăzut în decurs de 3-4 luni după retragerea ovăzului. Un punct slab al prezentului studiu este că a trecut un timp între biopsia de pre-provocare și provocarea reală. Acest lucru poate să nu fie optim, dar am considerat că este puțin probabil ca acești pacienți adulți bine tratați să dezvolte modificări ale mucoasei în timpul perioadei.
Rezultatele noastre sunt în contradicție cu studiile clinice raportate anterior. 1-6 Am observat că introducerea ovăzului a dus la modificări ale obiceiurilor intestinale și unele disconfort abdominal pentru mai mulți dintre pacienți. Este posibil ca această experiență să fi fost remarcată anterior, dar este importantă la fel. Poate fi folosit pentru a-i liniști pe celiaci începând cu ovăz că această experiență pare a fi normală și va trece probabil. Diferența majoră este că unul dintre pacienți a fost intolerant la ovăz. Acest lucru nu a fost raportat anterior. Mai mult, dacă se ia în considerare numărul total de pacienți din studiile clinice de provocare, intoleranța la ovăz pare a fi un eveniment rar.
După prezentul studiu de provocare, am întâlnit mai mulți pacienți care erau clinic intoleranți la ovăz (dermatită, dureri abdominale și reacții generale de tip anafilactoid). Nimeni nu a fost dispus să ingereze din nou ovăz. Astfel, considerăm că intoleranța la ovăz în CD este o entitate probabilă.
Deși nu este pe deplin înțeles în această etapă, este totuși interesant de observat că unii dintre pacienți au avut niveluri pozitive de mARN pentru IFN-γ, dar nu au anomalii histologice corespunzătoare. Considerăm IFN-γ ca un semn al activării celulelor T, dar este posibil să nu fie direct responsabil pentru atrofia vilozitată observată în CD. 19 Relevanța acestei constatări este limitată de faptul că un grup de control al pacienților cu CD care au fost abstinenți de la ovăz nu au fost incluși în studiul nostru de provocare. Cu toate acestea, am raportat anterior descoperiri care arată că celiacele bine tratate nu exprimă de obicei IFN-γ mARN în mucoasa intestinului subțire. 14, 15
Datele actuale susțin ideea că majoritatea pacienților cu CD tolerează ovăzul în dieta lor. Contaminarea ovăzului comercial cu alte cereale este o problemă, iar celiacii ar trebui să selecteze ovăzul de la producătorii care se dedică producției de ovăz fără astfel de contaminanți. Cu toate acestea, constatarea că chiar ovăzul pur poate induce atrofie viloză și dermatită la un pacient cu CD creează o anumită îngrijorare.
Mulțumiri
Mulțumim personalului asistent medical de la unitățile de endoscopie de la Rikshospitalet și Ullevaal sykehus, și personalului tehnic de la LIIPAT și Institutului de Imunologie, de la Rikshospitalet, pentru asistență neprețuită. Studiul a primit sprijin de la Regal, Fondul medical Freia Chocolate Fabric, Medinnova, Astra, Asociația Norvegiană pentru Boli Celiace și fonduri EXTRA de la Fundația Norvegiană pentru Sănătate și Reabilitare. Îi mulțumim dr. Andrew S Louka pentru citirea critică a manuscrisului.
- Articolul de revizuire a leziunilor hepatice induse de medicamente în contextul bolii hepatice grase nealcoolice - a
- Ovăz - Celiac UK
- Nutrienți Număr special Tulburări legate de gluten Boala celiacă și dincolo
- Ovăz, muesli, All Bran Cereale sănătoase pentru micul dejun
- Vacanța mea de top fără gluten - Lacul Garda, Italia - Pensiunea Celiac