Încercări volumul 20, Număr articol: 384 (2019) Citați acest articol
Abstract
fundal
Cancerul gastric este a treia cea mai frecventă cauză de decese cauzate de cancer și are a cincea cea mai mare incidență la nivel mondial, în special în Asia de Est, Europa Centrală și de Est și America de Sud. În prezent, chirurgia este singurul tratament curativ pentru cancerul gastric; cu toate acestea, există o tendință în creștere către gastrectomia radicală laparoscopică. Hrănirea timpurie pe cale orală (EOF) s-a dovedit a beneficia de rezultatele clinice în comparație cu gastrectomia deschisă în condiții de recuperare îmbunătățită după operație. Există o lipsă de linii directoare și dovezi pentru siguranța și fezabilitatea EOF la pacienții supuși gastrectomiei radicale laparoscopice. Astfel, se justifică un studiu prospectiv randomizat.
Metode/proiectare
Studiul EOF după gastrectomie radicală laparoscopică totală (SOFTLY) este un studiu controlat randomizat cu un singur centru, cu braț paralel, cu non-inferioritate, care va înscrie 200 de pacienți care sunt diagnosticați patologic cu cancer gastric și sunt supuși gastrectomiei radicale laparoscopice. Obiectivul principal, incidența scurgerii anastomotice, se bazează pe 1,9% în grupul de control din studiul CLASA-01. Pacienții vor fi randomizați (1: 1) în două grupuri: grupul EOF va primi o dietă lichidă limpede în ziua 1 post-operatorie (POD1), iar grupul de hrănire orală întârziată (DOF) va primi o dietă lichidă limpede după ziua operativă 4 (POD4). Vor fi înregistrate caracteristicile demografice și patologice. Aportul nutrițional total și oral, datele generale, proteinele serice totale, albumina serică, glicemia și temperatura vor fi înregistrate înainte de operație și în momentul spitalizării. Evenimentele adverse vor fi, de asemenea, înregistrate. Apariția fistulelor postoperatorii, inclusiv scurgerea anastomotică, va fi înregistrată ca principal eveniment advers postoperator sever și va reprezenta obiectivul primar.
Discuţie
Siguranța și fezabilitatea EOF după gastrectomie nu au fost stabilite. Studiul SOFTLY va fi primul studiu controlat randomizat care implică gastrectomie radicală laparoscopică totală, în care grupul EOF (POD1) va fi comparat cu grupul DOF (POD4). Rezultatele studiului SOFTLY vor furniza date despre siguranța și fezabilitatea EOF după gastrectomia radicală laparoscopică totală.
Înregistrarea procesului
Registrul de studii clinice din China, ChiCTR-IOR-15007660. Înregistrat la 28 decembrie 2015. Studiul are aprobare etică și instituțională completă.
fundal
Raportul mondial privind cancerul din 2014, publicat de OMS [1, 2], a indicat că cancerul gastric a fost al cincilea cel mai frecvent malign (951.600 de cazuri; 6,8% din total) și a treia cauză principală a deceselor provocate de cancer în 2012 la nivel mondial (723.100 de decese; 8,8% din total). Rezecția gastrică este principala abordare terapeutică prin care se prelungește supraviețuirea pacienților cu cancer gastric [3].
S-a raportat că aproximativ 30% dintre pacienții cu cancer sunt subnutriți, dintre care majoritatea sunt pacienți cu cancer gastro-intestinal superior [4]. În 1980, Eastern Cooperative Oncology Group (ECOG) a raportat că prevalența malnutriției la pacienții cu cancer gastric a fost de până la 87% [5].
Boala în sine și tratamentul medicamentos, precum și efectul intervenției chirurgicale asupra tractului gastro-intestinal și a sistemului metabolic, sunt toți potențialii factori care contribuie la malnutriția postoperatorie, care ar putea duce la infecții postoperatorii, prelungind durata de ședere postoperatorie ( LOS) și crește morbiditatea și mortalitatea [6,7,8].
Sprijinul nutrițional este crucial după o intervenție chirurgicală gastrică. Datorită protecției locului anastomotic și a ileusului potențial tranzitoriu [9], este de rutină o perioadă de post cu nutriție parenterală numai după o intervenție chirurgicală gastrică până când funcția intestinului este detectabilă clinic [10]. Cu toate acestea, nutriția parenterală ca singură cale nutrițională are dezavantaje nutriționale și imunologice mai mari decât suportul nutrițional enteral [11, 12].
Ghidurile Societății Europene pentru Nutriție Parenterală și Enterală (ESPEN) și Recuperare Îmbunătățită după Chirurgie recomandă inițierea timpurie a aportului normal de hrană sau a hranei enterale după o intervenție chirurgicală gastrointestinală (grad A) și hrănirea tubului enteral (de exemplu, un cateter cu ac jejunostomie sau sonda nasojejunală) când administrarea orală nu este posibilă. Sunt disponibile date limitate cu privire la aportul oral imediat la pacienții cu anastomoze supuse gastrectomiei [13, 14]. Hrănirea orală timpurie (EOF) ca cale nutrițională naturală după o intervenție chirurgicală gastrică a fost recent raportată în studiile randomizate controlate (ECA) și o meta-analiză, iar hrănirea orală întârziată servește drept control [15,16,17,18,19].
Aceste studii au arătat o îmbunătățire cu EOF direct după o intervenție chirurgicală gastrică; în mod specific, recuperarea funcției intestinului a fost mai rapidă, LOS post-operatorie a fost mai scurtă, iar ratele de complicații chirurgicale și generale au fost mai mici. Puține studii au evaluat EOF la pacienții cu cancer gastric supuși gastrectomiei radicale laparoscopice, inclusiv gastrectomii totale și subtotale [15,16,17,18].
Studiile anterioare [15,16,17] privind EOF după gastrectomie deschisă ne-au condus la ipoteza că pacienții cu cancer gastric supuși gastrectomiilor radicale total laparoscopice tratați cu EOF au rate de scurgere anastomotice similare sau mai mici, mai puține complicații și o recuperare mai rapidă în comparație cu hrănire orală întârziată. Unele dovezi indică faptul că EOF ca parte a recuperării timpurii după intervenția chirurgicală (ERAS) este fezabilă și sigură după o intervenție chirurgicală de cancer gastric [15, 20] și este asociată cu o spitalizare mai scurtă și timp până la trecerea gazelor. Procedura chirurgicală și reconstrucția digestivă sunt principalele diferențe între gastrectomia radicală deschisă și laparoscopică [21] (în special gastrectomia radicală laparoscopică totală (TLRG)). În studiul actual, pacienții cu cancer gastric din grupul EOF vor începe o dietă lichidă limpede în ziua postoperatorie (POD) 1, în timp ce pacienții din grupul de hrănire orală întârziată (DOF) vor începe o dietă lichidă limpede pe POD4; ambele grupuri nu vor avea limite de volum. Vor fi incluși numai pacienții supuși gastrectomiei total laparoscopice. Prin urmare, am proiectat un RCT de siguranță și fezabilitate pentru a verifica ipoteza. Rezultatele pot servi drept bază pentru studiul ulterior al EOF după TLRG.
Obiectivul studiului actual este de a evalua dacă EOF după TLRG va crește sau nu rata de scurgere anastomotică în comparație cu DOF. Încercăm să stabilim dacă o dietă lichidă clară pe POD1 crește sau nu rata de scurgere anastomotică sau poate duce la o mai bună recuperare funcțională după TLRG comparativ cu hrănirea orală cu POD4. Proiectarea studiului va determina siguranța și fezabilitatea EOF după gastrectomia radicală laparoscopică și va furniza dovezi suplimentare ale liniilor directoare ERAS după TLRG.
Metode/proiectare
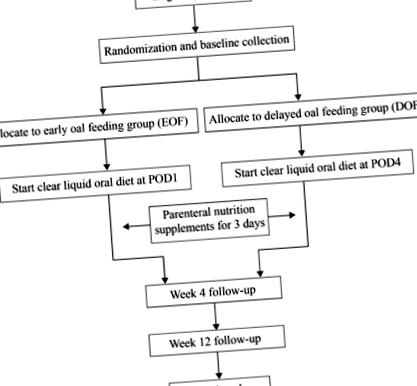
SOFTLY este un ECC cu non-inferioritate, cu un singur centru, cu braț paralel, în care 200 de pacienți vor fi repartizați aleatoriu în una din cele două perioade diferite de hrănire orală postoperatorie care vor fi inițiate după TLRG. Diagrama fluxului de încercare este prezentată în Fig. 1.
Diagrama fluxului de proiectare a studiului
Procesul SOFTLY va testa ipoteza că EOF, care va fi inițiat pe POD1, nu este inferior DOF pe POD4 pentru pacienții supuși TLRG în ceea ce privește rata de scurgere anastomotică.
O listă completă de verificare a articolelor conform SPIRIT 2013 [22] este furnizată în fișierul suplimentar 1.
Aprobarea etică
Procedurile de studiu și formularul de consimțământ informat au fost aprobate de Comitetul de Etică independent al spitalului Xijing din provincia Shaanxi, China. Informațiile despre orice evenimente adverse (AE) vor fi raportate comitetului de etică până la atingerea unei situații stabile. Comitetul de etică are datoria de a evalua periodic progresul acestui proces.
Procedura de randomizare
Participanții care îndeplinesc criteriile de eligibilitate vor fi repartizați aleatoriu fie grupului EOF, fie grupului DOF cu un raport 1: 1. Secvența de randomizare a fost generată de un biostatistician care nu este implicat în acest studiu cu software-ul SAS versiunea 9.2 (SAS Institute, Cary, NC, SUA). Lista de randomizare a fost sigilată în plicuri opace numerotate secvențial, care au fost depozitate într-un dulap cu dublu blocare. Randomizarea este implementată de un asistent de cercetare care nu este implicat în recrutare. După alocarea aleatorie, plicurile vor fi stocate din nou separat. Deoarece participanții nu pot fi orbiți de intervenție sau clinicienii responsabili de îngrijirea pacientului, vor fi orbi doar colectarea și analiza datelor [23]. Figura 1 prezintă diagrama de încercare.
Selecția participanților
Criteriile de includere sunt următoarele: 1) intervalul de vârstă, 18-65 ani; 2) diagnosticul de cancer gastric și eligibil pentru gastrectomie radicală laparoscopică; 3) fără chimioterapie, radioterapie și terapie țintită înainte de operație; 4) screeningul riscului nutrițional 2002 (NRS2002) ≤ 5; și 5) să ofere consimțământul informat.
Criteriile de excludere sunt următoarele: 1) cancer concomitent; 2) cancer gastric restant; 3) complicații (sângerare, perforație sau obstrucție); 4) chirurgie de urgență.
Protocoale de tratament
Acesta este un RCT de confirmare, cu un singur site, de non-inferioritate pentru a evalua siguranța și fezabilitatea EOF după TLRG comparativ cu DOF.
Toți pacienții eligibili cu cancer gastric vor fi repartizați aleatoriu într-un raport de alocare 1: 1 grupului EOF sau DOF. Participanții la ambele grupuri vor fi supuși unor proceduri peri-operatorii similare, cu excepția orelor de început ale hrănirii orale diferite. Toate datele studiului vor fi stocate într-un fișier Excel 2007, care va fi monitorizat de o asistentă care nu este implicată în acest studiu.
Proceduri perioperatorii
Înainte de operație, se vor efectua gastroscopii, biopsii endoscopice și tomografii computerizate pentru a confirma dimensiunea și localizarea tumorii, iar pacienții cu metastaze organice vor fi excluși pe baza evaluării de către doi patologi experimentați. Se vor respecta liniile directoare ERAS și toți participanții vor primi educație preoperatorie, analgezie preventivă și multimodală, ambulare precoce și gastrectomie radicală laparoscopică ca parte a tratamentului peri-operator.
Gastrectomii laparoscopice radicale vor fi efectuate de aceleași echipe chirurgicale experimentate, care au efectuat această procedură cu un număr anual de aproximativ 100 de pacienți cu cancer gastric. Anastomoza principală va fi finalizată laparoscopic, iar incizia abdominală va fi de 1000 ml de la POD3-6, așa cum este tolerată, în timp ce participanții randomizați la grupul DOF (grupul de control) vor primi același conținut de hrănire orală descris mai sus în timpul acestui studiu pe POD4. ). Singura diferență între brațele de intervenție și de control va fi timpul de începere a alimentării orale după operație. Astfel, grupul DOF va ține post timp de 3 zile și va primi 50-500 ml dintr-o injecție de glucoză de 10% pe POD4 și> 1000 ml de suspensie nutritivă enterală pe POD6.
Intervenția a fost planificată pentru POD6. Un nutriționist va supraveghea hrănirea orală în timpul procesului, folosind principiul dietetic al consumului mai mic și mai frecvent, în funcție de toleranța individuală. Aportul caloric adecvat va fi calculat folosind formula Harris-Benedict (25-35 kcal/kg/zi). Un investigator va fi desemnat să înregistreze datele de observare clinică.
Doar atunci când intestinul este intolerant (nu poate îndeplini 60% din cerințele zilnice pentru POD4) sau există suspiciunea unei scurgeri anastomotice, se va lua în considerare nutriția parenterală totală. Criteriile de descărcare de gestiune sunt definite ca menținerea temperaturii normale timp de 3 zile, ambulație și capacitatea de a tolera lichidele orale ad libitum.
Colectarea și programarea datelor
După semnarea consimțământului informat, datele de bază, cum ar fi vârsta, sexul, indicele de masă corporală (IMC) și complicațiile, vor fi colectate de un asistent de cercetare clinică. Datele de laborator (proteina serică totală, albumina serică și glicemia) vor fi, de asemenea, testate preoperator și în timpul spitalizării pentru a monitoriza starea nutrițională a pacienților. Un operator specificat va înregistra detaliile procedurilor chirurgicale, cum ar fi abordarea operatorie, localizarea tumorii, metastaza ganglionilor limfatici și stadiul TNM patologic.
De la POD1-6, datele de observație clinică (scurgeri anastomotice, timpul primului flatus și defecație, scorul durerii NRS, șederea spitalică postoperatorie și complicațiile) vor fi, de asemenea, înregistrate zilnic pentru a evalua recuperarea postoperatorie de către un investigator. Clinicienii vor fi responsabili pentru îngrijirea pacienților și nu vor fi implicați în colectarea datelor.
Informațiile de contact și adresa pacienților vor fi confirmate înainte de externare. Două vizite de urmărire vor fi efectuate în ambulatoriu sau telefonic la 4 și 12 săptămâni după externare, concentrându-se pe toleranța dietei și orice disconfort. Detaliile programului sunt prezentate în Fig. 2.
Conținut pentru programul de înscriere, intervenții și evaluări
Obiective de studiu
Obiectivul principal va fi procentul de incidență a scurgerilor anastomotice după TLRG. Vom determina dacă EOF la POD1 este sau nu non-inferior în ceea ce privește apariția fistulelor post-operatorii, inclusiv scurgeri anastomotice. Scurgerea anastomotică va fi definită ca defalcarea conexiunii și scurgerea ulterioară a fluidului sistemului digestiv de la o anastomoză chirurgicală a structurilor sistemului digestiv. Dacă se suspectează clinic o scurgere anastomotică post-operatorie, se va efectua o radiografie a tractului digestiv pentru a diagnostica scurgerea. De obicei, un drenaj abdominal suficient este cel mai eficient tratament.
Obiectivele secundare sunt recuperarea postoperatorie și starea nutrițională, după cum urmează: (1) complicații postoperatorii (n) la 30 de zile conform clasificării Clavien Dindo, care includ infecție incizională, abces abdominal, hemoragie intraperitoneală, sângerare anastomotică, postoperator obstrucție intestinală, pancreatită, complicații pulmonare și alte complicații ale organelor; (2) ora primului flatus și a defecației (zi); (3) durata șederii postoperatorii (zi); și (4) costurile de spitalizare (yuani).
Estimarea mărimii eșantionului
Pe baza datelor din studiul CLASS-01 [21], rata de scurgere anastomotică în acest studiu este definită ca 1,9%, iar ECA anterioare care implică gastrectomie deschisă au concluzionat că nu au existat diferențe semnificative între EOF și hrănirea orală tradițională în ceea ce privește riscul de scurgeri anastomotice [19, 24]. Pentru a verifica dacă EOF nu este inferior în raport cu rata de scurgere anastomotică după gastrectomia radicală laparoscopică, am proiectat un test de non-inferioritate cu o marjă de non-inferioritate de 5% (α = 0,05, β = 0,20 și o putere de 80 %). Având în vedere atât considerații clinice, cât și statistice, cum ar fi intoleranța la nutrienții enterali, prin urmare, nu vor fi necesari mai puțin de 160 de participanți (80 de participanți în fiecare grup). Având în vedere abandonul și retragerile de 20% înainte de finalizarea procesului, am decis să recrutăm un total de 200 de participanți (100 de participanți în fiecare grup) [21].
analize statistice
Principiul intenției de a trata va fi aplicat în toate analizele cu o rată presupusă de abandon. Variabilele continue distribuite în mod normal vor fi descrise ca medii cu SD-urile corespunzătoare, iar variabilele categoric ne-distribuite în mod normal vor fi descrise ca mediane cu intervalul corespunzător sau procente și frecvențe. Datele continue distribuite în mod normal sau non-normal vor fi comparate de către Student t-testul sau testul Mann - Whitney U și testul chi-pătrat și testul exact al lui Fisher vor fi utilizate pentru a compara variabilele categorice, după cum se indică. Cu excepția rezultatului primar, vor fi, de asemenea, comparate rezultatele secundare, cum ar fi complicațiile postoperatorii, timpul primului flatus și defecația și durata postoperatorie a șederii. Factorii potențiali de risc pentru intoleranță la EOF și complicații post-operatorii vor fi identificați utilizând o analiză multivariantă. Un statistician orb va analiza toate datele folosind un sistem cu două fețe P valoare
Discuţie
Factori precum postul, doar nutriția parenterală, răspunsul la stres după o intervenție chirurgicală gastro-intestinală și utilizarea perioperatorie a antibioticelor pot duce la inhibarea salivei și a secreției de lichid gastrointestinal, afectează motilitatea gastro-intestinală și funcția de barieră a mucoasei intestinale și pot perturba microbiomul intestinal. Utilizarea unei strategii nil-by-mouth aplicată în mod tradițional este adesea adoptată deoarece EOF ar putea duce la o fistulă a tractului digestiv sau obstrucție intestinală secundară din cauza presiunii intestinale crescute [10, 25]; cu toate acestea, nu există dovezi care să susțină această teorie. În ciuda lipsei datelor solide, liniile directoare ESPEN și ERAS după gastrectomie recomandă inițierea timpurie a aportului oral ca cale preferată pentru nutriție.
În ultimii ani, EOF ca cale nutrițională în conformitate cu nevoile fiziologice după gastrectomia deschisă s-a dovedit a fi asociat cu o reducere a spitalului, fără a îmbunătăți rata de scurgere anastomotică. Sunt disponibile date limitate pentru gastrectomia radicală laparoscopică.
Studiul propus se bazează pe cercetări în urma gastrectomiei deschise pentru a evalua siguranța și fezabilitatea EOF după gastrectomia radicală laparoscopică. Sub îndrumarea ERAS, dacă EOF va duce sau nu la beneficii semnificative va fi, de asemenea, evaluat comparativ cu DOF.
Dacă EOF după gastrectomia radicală laparoscopică se dovedește a fi la fel de sigură ca DOF, vor fi efectuate studii suplimentare multicentrice. Efectele conținutului și aportului alimentar de EOF asupra beneficiilor postoperatorii ar trebui explorate într-un studiu corolar, încercând să desemneze EOF ca un nou tratament nutrițional după gastrectomie.
Starea procesului
Înscrierea la acest studiu este în curs la momentul depunerii manuscrisului. În prezent, procesul a recrutat deja 102 pacienți.
- Terapia de rehidratare orală și hrănirea înlocuiesc nutriția parenterală totală cu o vinetă clinică
- Consumul de sare și alimente sărate și riscul ulterior de cancer gastric la bărbații japonezi de vârstă mijlocie
- Prevenirea cancerului de stomac (gastric)
- Înregistrarea unei diete a pacientului pe parcursul radical al radioterapiei pentru cancerul de prostată folosind o dietă
- Mirul induce apoptoza și inhibă proliferarea și migrația celulelor canceroase gastrice