1 Rush University College of Nursing, 600 S. Paulina Street, Suite 1080, Chicago, IL 60612, SUA
2 Rush University Medical Center, 1725 W. Harrison Street, Chicago, IL 60612, SUA
3 Secțiunea de gastroenterologie și nutriție, Rush University Medical Center, 1725 W. Harrison Street, Chicago, IL 60612, SUA
4 North Park University School of Nursing, 3225 W. Foster Avenue, Chicago, IL 60625, SUA
5 Asistență medicală pentru comunitate, sisteme și sănătate mintală, Rush University College of Nursing, 600 S. Paulina Street, Suite 1080, Chicago, IL 60612, SUA
6 Facultate de practică, Rush University College of Nursing, 600 S. Paulina Street, Suite 1080, Chicago, IL 60612, SUA
Abstract
fundal. Sunt disponibile câteva suplimente alimentare sigure și eficiente pentru a favoriza pierderea în greutate. Am evaluat siguranța și eficacitatea glucomananului, un supliment de fibre solubile în apă, pentru obținerea pierderii în greutate la persoanele supraponderale și cu obezitate moderată care consumă diete auto-selectate. Metode. Participanții au fost repartizați aleatoriu să ia 1,33 grame de glucomannan sau capsule placebo cu aspect identic, cu 236,6 ml (8 uncii) de apă cu o oră înainte de micul dejun, prânz și cină timp de 8 săptămâni. Rezultatul principal al eficacității a fost modificarea greutății corporale după 8 săptămâni. Alte rezultate ale eficacității au fost modificările compoziției corpului, foamea/plenitudinea și concentrațiile de lipide și glucoză. Rezultatele de siguranță au inclus simptome gastro-intestinale/toleranță și enzime hepatice serice și niveluri de creatinină. Rezultate. Un total de 53 de participanți (18-65 de ani; IMC 25-35 kg/m 2) au fost înscriși și randomizați. Cele două grupuri nu au diferit în ceea ce privește caracteristicile de bază și respectarea suplimentului de studiu. La 8 săptămâni, nu a existat nicio diferență semnificativă între grupurile de glucomanan și placebo în ceea ce privește pierderea în greutate (
, resp.) sau alte rezultate ale eficacității sau în oricare dintre rezultatele siguranței. Concluzii. Suplimentele de glucomannan administrate pe parcursul a 8 săptămâni au fost bine tolerate, dar nu au favorizat pierderea în greutate sau nu au modificat semnificativ compoziția corpului, foamea/plenitudinea sau parametrii lipidelor și glucozei. Acest proces este înregistrat cu NCT00613600.
1. Introducere
Excesul de greutate și obezitatea sunt extrem de dificil de inversat. În ciuda utilizării pe scară largă a strategiilor convenționale de management - diete cu conținut scăzut de calorii, activitate fizică, intervenții comportamentale și agenți farmacologici - prevalența supraponderalității și a obezității continuă să crească în SUA. Se estimează că 65% din totalul adulților din SUA au fost supraponderali sau obezi în perioada 2007-2008 [1]. Excesul de greutate și obezitatea cresc riscul de comorbidități precum diabetul și ateroscleroza și sunt asociate cu o calitate a vieții redusă și cu speranța de viață [2, 3]. În mod clar, sunt necesare abordări alternative. O abordare alternativă potențial promițătoare este glucomananul, un supliment alimentar larg promovat și utilizat pentru proprietățile sale de slăbire. În ciuda utilizării sale pe scară largă, siguranța și eficacitatea glucomananului nu au fost studiate în mod adecvat.
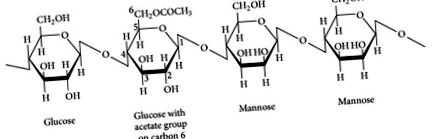
Glucomananul este o fibră dietetică solubilă în apă, fermentabilă, extrasă din tubercul sau rădăcina elamului de elefant, cunoscută și sub numele de konjac (Coniac Amorphophallus sau Amorphophallus rivieri). Glucomannanul constă dintr-un lanț polizaharidic de beta-D-glucoză și beta-D-manoză cu grupări acetil atașate într-un raport molar de 1: 1,6 cu legături beta 1-4 (vezi Figura 1) [4-6]. Deoarece amilaza salivară și pancreatică umană nu poate împărți legăturile beta 1, 4, glucomananul trece relativ neschimbat în colon, unde este fermentat puternic de bacteriile colonice. Are o greutate moleculară ridicată (în medie: 1.000.000 de daltoni) și poate absorbi până la 50 de ori greutatea sa în apă, făcându-l una dintre cele mai vâscoase fibre dietetice cunoscute [6]. Prin urmare, glucomananul se administrează în doze mai mici decât alte tipuri de suplimente de fibre.
Se crede că mecanismele care mediază efectele de reducere a greutății glucomananului sunt similare cu cele ale altor fibre fermentabile solubile în apă. Cu densitatea sa redusă de energie și proprietățile voluminoase, glucomananul pare să promoveze pierderea în greutate prin deplasarea energiei altor substanțe nutritive și producerea de sațietate și saturație, deoarece absoarbe apa și se extinde în tractul gastro-intestinal. În plus, glucomananul pare să reducă colesterolul total și nivelul de colesterol al lipoproteinelor cu densitate mică (LDL) prin stimularea excreției fecale a colesterolului și a acizilor biliari și scăderea absorbției intestinale a colesterolului [7-9]. De asemenea, glucomananul poate îmbunătăți parametrii glicemici prin inhibarea poftei de mâncare și încetinirea absorbției intestinale datorită vâscozității crescute [10-13]. Glucomananul este în general bine tolerat și are un profil de siguranță favorabil.
Glucomananul a fost asociat cu reduceri ale greutății corporale și ale lipidelor plasmatice și ale nivelului de glucoză la adulți în câteva studii clinice [14-19]. Dar aceste studii au fost limitate de modele slabe, dimensiuni reduse ale eșantionului, diagnostice eterogene, formulări variabile și doze de glucomanan și durata scurtă de urmărire [20]. Spre deosebire de aceste studii, am folosit un design randomizat, dublu-orb, controlat cu placebo, pentru a evalua siguranța și eficacitatea a 3,99 g/zi de capsule de glucomanan într-un eșantion de 53 de adulți sănătoși supraponderali și cu obezitate moderată care consumă diete auto-selectate și menținerea nivelurilor obișnuite de activitate fizică în timpul unei perioade de studiu de 8 săptămâni.
2. Materiale și metode
2.1. Populația de studiu
Pe baza unui studiu anterior controlat cu placebo al glucomananului [18], am planificat să recrutăm 50 de participanți și să îi urmărim timp de 8 săptămâni pentru a avea 80% putere pentru a detecta în mod adecvat modificările în greutate și alte variabile metabolice.
2.2. Design de studiu
Indivizii eligibili care au consimțit să participe la studiu au fost repartizați aleatoriu să primească capsule care conțin glucomanan sau un placebo potrivit, umplut cu celuloză microcristalină inactivă. Un generator de numere aleatorii a fost utilizat pentru a crea o secvență de randomizare; cutii conținând aprovizionarea cu capsule a fiecărui participant au fost ambalate conform acestei secvențe. Atât capsulele de glucomannan, cât și cele placebo au fost preparate de o farmacie externă, care nu a avut alt rol în studiu. Pentru a se asigura că suplimentul de glucomannan utilizat în perioada de studiu îndeplinește standardele de control al calității, a fost achiziționat din același lot și o probă a fost trimisă la ConsumerLab.com pentru analize compoziționale și de puritate, care indicau compoziția și puritatea adecvate. Nici participanții, nici anchetatorii nu au fost conștienți de sarcinile de tratament.
Participanții au fost instruiți să ia două capsule de 666 mg (1,33 g) glucomanan sau placebo cu 236,6 ml (8 oz.) De apă cu o oră înainte de micul dejun, prânz și cină timp de 8 săptămâni (pentru un total de 3,99 g/zi). De asemenea, au fost încurajați să-și mențină aportul alimentar actual și nivelurile de activitate fizică. Participanții la studiu s-au întors la 2 săptămâni și 8 săptămâni pentru a returna orice supliment de studiu neutilizat sau placebo din vizita anterioară, pentru a primi o nouă sursă de supliment de studiu sau placebo pentru restul de 6 săptămâni, pentru a raporta efectele secundare și pentru a extrage sânge.
Toate datele au fost colectate de personalul de cercetare din studiu și încărcate în baza de date TeleForm (scanare electronică) de către un asistent de cercetare. Studiul a fost aprobat de comisia de revizuire instituțională a site-ului. Toți participanții au acordat consimțământul informat în scris înainte de înscriere. Un comitet independent de monitorizare a datelor și siguranței a monitorizat procesul și a analizat rezultatele intermediare.
2.3. Rezultatul primar
Rezultatul principal al eficacității a fost pierderea în greutate de la momentul inițial la 2 săptămâni și 8 săptămâni după randomizare. Greutatea corporală a fost măsurată la cel mai apropiat 1/10 kg folosind o cântare electronică calibrată, participanții purtând haine ușoare fără pantofi [21].
2.4. Rezultate secundare
Rezultatele secundare de eficacitate au inclus modificări ale compoziției corpului (circumferința taliei/șoldului, grăsimii corporale și a masei lipsite de grăsime), foametei și plenitudinii, precum și parametrii lipidelor și glicemiei în repaus alimentar. Circumferința taliei și șoldului a fost determinată folosind proceduri standardizate [22], iar grăsimea corporală și masa fără grăsime au fost măsurate folosind Tanita Ultimate Scale (Tanita Corp., Tokyo, Japonia). Senzațiile subiective de foame și plenitudine au fost evaluate utilizând scale analogice vizuale (VAS) standardizate de 100 mm [23]. Scara foamei era ancorată de cuvintele „Deloc flămând” și „Extrem de flămând”, iar scara de plinătate era ancorată de „Deloc plin” și „Extrem de plin”. Participanții au fost rugați să facă o marcă verticală peste linia corespunzătoare sentimentelor lor în ultimele patru ore din ziua vizitei lor programate la clinică (total = trei zile în perioada de studiu de 8 săptămâni). Pentru a înscrie scale, distanța în mm de la 0 pentru fiecare scară a fost măsurată cu o riglă. Probele de sânge venos periferic în post au fost obținute pentru nivelurile de glucoză și lipide. Un panou lipidic standard a fost utilizat pentru a cuantifica trigliceridele, colesterolul total și colesterolul HDL; Nivelurile de colesterol LDL au fost calculate folosind ecuația Friedewald.
Principalele rezultate ale siguranței au fost simptomele gastro-intestinale și tolerabilitatea și evaluarea de laborator a funcției hepatice și renale. Simptomele și toleranța gastro-intestinale au fost determinate prin întrebarea participanților despre dificultăți la înghițire, distensie abdominală, diaree, eructații și alte simptome legate de gastro-intestinale folosind metode standard de interogare nedirecționată, inclusiv când au început simptomele și dacă se credea că acestea sunt legate de suplimentul de studiu. Enzimele hepatice au fost considerate crescute cu un nivel de aspartat aminotransferază> 275 u/L și/sau o alanină transferază> 250 u/L; pentru creatinina serică, un nivel> 4,5 mg/dL a fost considerat crescut.
Alte măsuri au inclus aportul alimentar, activitatea fizică, respectarea suplimentelor și percepțiile de credibilitate/speranță ale tratamentului studiat. Pentru a evalua modificările pe parcursul perioadei de studiu de 8 săptămâni, aportul alimentar a fost măsurat utilizând înregistrări alimentare de 3 zile completate la momentul inițial, 2 săptămâni și 8 săptămâni și analizate folosind software-ul de analiză a datelor clinice NutriBase (http://www.nutribase.com /). Chestionarul internațional de activitate fizică (IPAQ) [24] a fost administrat la momentul inițial, 2 săptămâni și 8 săptămâni pentru a caracteriza orice modificări ale nivelului obișnuit de activitate în timpul perioadei de studiu care ar putea afecta rezultatele studiului. Complianța suplimentului a fost măsurată prin numărarea capsulelor și raportarea de sine a procentului de capsule luate. Conformitatea calculată a fost definită ca procentul de doze prescrise luate de la momentul inițial pe parcursul perioadei de studiu de 8 săptămâni. Deoarece diferențele dintre percepțiile participanților cu privire la credibilitatea raționamentului tratamentului și speranța lor ar putea confunda rezultatele, am administrat chestionarul privind credibilitatea/speranța (CEQ) participanților din ambele grupuri în primele și ultimele zile ale tratamentului [25].
2.5. Analize statistice
Toate analizele statistice au fost efectuate cu SPSS 16.0 (Chicago, IL). Au fost utilizate statistici descriptive pentru a caracteriza eșantionul. Datele nominale au fost analizate prin utilizarea testului chi-pătrat, în timp ce datele continue au fost analizate prin utilizarea analizelor de corelație Pearson, eșantion independent
-teste și analiza unică a varianței. Datele sunt prezentate ca medie ± SD. A fost determinat un nivel de semnificație de 0,05 a priori.
3. Rezultate
3.1. Populația de studiu
Figura 2 prezintă screening-ul, înscrierea și urmărirea participanților la studiu. Dintre cei 124 de adulți selectați, un total de 53 au îndeplinit criteriile de eligibilitate și au fost înscriși în studiu. Douăzeci și șase de participanți au fost repartizați aleatoriu în grupul cu glucomanan și douăzeci și șapte de participanți la grupul placebo. Nu au existat diferențe semnificative între cele două grupuri în ceea ce privește ratele de întrerupere. Trei participanți din fiecare grup au fost fie pierduți pentru urmărire, fie au întrerupt studiul din motive personale, rezultând un eșantion final de 47 de participanți.
Caracteristicile demografice și clinice inițiale au fost similare între cele două grupuri (Tabelul 1). Participanții au fost preponderent de sex feminin (
85%), au reprezentat un amestec de grupuri rasiale și etnice și au avut o vârstă medie de 40,6 ani. Pentru cei 47 de participanți care au finalizat studiul, conformitatea calculată a fost de 81,3% ± 4,5% în grupul cu glucomanan și 82,7% ± 5% în grupul placebo.
- Cunoașterea nutrițională este asociată cu o scădere mai mare în greutate la obezi și supraponderali cu venituri mici
- Efortul fiziologic în testele de fitness submaximale prezice pierderea în greutate la bărbații supraponderali și obezi
- Siguranța și eficacitatea Ledipasvir Sofosbuvir la adulți cu infecție cronică cu VHC - Vizualizare text complet
- Un border collie sever obez începe o călătorie de slăbire, spune salvarea câinilor Winnipeg - Winnipeg
- Studiul antrenorului de sănătate AI îmbunătățește pierderea în greutate în rândul persoanelor obeze