Rosa Burgos
Endocrinologie și nutriție
Unitatea de sprijin nutrițional
Spitalul Universitar Vall d'Hebron
Pag. Vall d'Hebron 117-127
08035, Barcelona, Spania
obiective de invatare
- Să știe despre intervenția nutrițională la pacienții care suferă de scleroză multiplă sau boala Parkinson;
- Să cunoască problemele luării deciziilor clinice în momentul/siguranța/eficacitatea hrănirii tubului gastrostomiei endoscopice percutanate (PEG) la pacienții cu scleroză laterală amiotrofică (SLA);
- Să înțeleagă provocarea clinică a stabilirii și menținerii hrănirii tubului la pacienții neurologici cu demență avansată;
- Să cunoască implicațiile etice, legale și morale ale sprijinului nutrițional la pacienții cu tulburări neurodegenerative cu demență progresivă.
Cuprins
- Introducere
- Suport nutrițional în condiții neurologice cronice 2.1 Scleroza multiplă 2.2 Boala Parkinson 2.3 Boala neuromusculară (inclusiv scleroza laterală amiotrofică)
- Hrănirea enterală: considerații la pacienții cu tulburări neurologice cronice
- Alimentarea cu tub/plasarea PEG în tulburările neurodegenerative
- Considerații etice: hrănirea tubului în tulburările neurodegenerative cu demență avansată
- rezumat
- Caz clinic
- Test de autoevaluare
- Referințe
Mesaje cheie
- Pacienții cu boli neurologice cronice sunt expuși riscului de malnutriție, cu disfagie cea mai frecventă preocupare în ceea ce privește evaluarea și tratamentul;
- Pacienții cu scleroză laterală amiotrofică generează cele mai frecvente dileme cu privire la momentul/eficacitatea și securitatea plasării PEG;
- Nu există date robuste disponibile care să susțină hrănirea tubului în fața hrănirii orale în demența terminală avansată;
- Pacienții cu demență avansată nu sunt de obicei considerați candidați adecvați pentru hrănirea artificială prin tuburi PEG;
- Din punct de vedere juridic și etic, sprijinul nutrițional specializat ar trebui considerat a fi o terapie medicală;
- Directivele avansate ajută la rezolvarea conflictelor legate de tratamentele dorite.
1. Introducere
2. Suport nutrițional în condiții neurologice cronice
2.1 Scleroza multiplă
Managementul nutriției
Excesul de greutate și obezitatea pot apărea, de asemenea, inițial din cauza mobilității reduse, a corticosteroizilor, a medicamentelor antidepresive și a obiceiurilor dietetice nesănătoase (utilizarea alimentelor grase, a băuturilor cu zahăr etc.). (4).
Odată cu creșterea handicapului, pierderea în greutate, malnutriția și cașexia sunt frecvente. Deși incidența malnutriției la pacienții cu SM nu a fost determinată, aceasta poate afecta negativ funcția organelor, puterea musculară și funcția imună, agravând astfel simptomele SM (6). Posibilele cauze ale malnutriției sunt rezumate în tabelul 1. Gestionarea dietetică a pierderii în greutate depinde de identificarea sursei problemei.
Disfagia este un simptom al SM cronice progresive. Incidența raportată variază între 3 și 43%, în funcție de metoda utilizată pentru evaluarea dificultății de înghițire (7-10). Este adesea însoțită de dificultăți de vorbire. Caracteristicile disfagiei includ tuse și sufocare în timpul meselor, infecții toracice frecvente și pierderea în greutate. Evaluarea capacității de a înghiți poate fi clinică inițial, dar aceasta ar trebui să fie urmată de fluoroscopie video sau de evaluare endoscopică fibreoptică a deglutiției. Tipul intervenției nutriționale depinde de gradul de dificultate și variază între dietele de consistență modificate și nutriția artificială exclusivă dacă riscul de aspirație este foarte mare.
Dacă pierderea în greutate progresează în ciuda intervenției orale sau dacă disfagia nu poate fi tratată în condiții de siguranță prin modificări dietetice, ar trebui luată în considerare nutriția enterală prin intermediul unui PEG. Hrănirea tubului enteral poate îmbunătăți starea nutrițională, reduce riscul de pneumonie prin aspirație, reduce riscul de apare la răni și menține echilibrul fluidelor, precum și permite o anumită administrare orală continuă. Cu toate acestea, înainte de a începe tratamentul, argumentele pro și contra nutriției artificiale ar trebui discutate pe deplin cu pacientul și familia.
2.2 Boala Parkinson
2.3 Boli neuromusculare (scleroză laterală amiotrofică)
Problemele cheie pentru managementul nutrițional în scleroza laterală amiotrofică includ (19, 20):
- Suplimentarea energiei
- Diagnosticul/tratamentul disfagiei
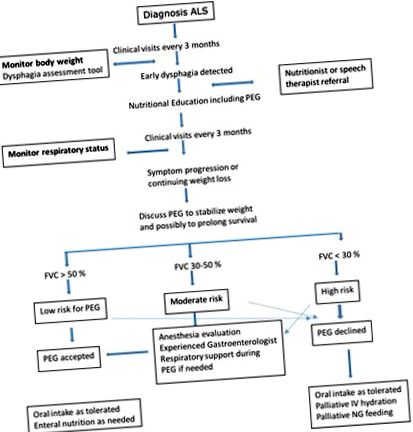
- Momentul/siguranța/eficacitatea plasării tubului PEG.
Diagnosticul și tratamentul disfagiei
Disfagia la pacienții cu SLA este foarte răspândită și poate fi simptomul inițial în SLA cu debut bulbar. În formele avansate ale bolii, prevalența disfagiei poate fi aproape de 100%. Pentru mai multe detalii despre diagnosticul de disfagie, consultați modulul 25.1.
3. Considerații privind hrănirea enterală la pacienții cu tulburări neurologice cronice
Mai multe întrebări trebuie abordate atunci când se ia în considerare nutriția enterală a pacienților cu boli neurologice cronice (23):
- Nivelul de conștiință al pacientului
- Poate pacientul să protejeze căile respiratorii de episoadele de reflux gastro-esofagian?
- Care este capacitatea pacientului de a înghiți lichide, lichide îngroșate și alimente moi și solide?
- Pacientul prezintă un risc crescut de aspirare a secrețiilor orofaringiene?
- Nevoia de acces enteral va fi pe termen scurt sau lung?
- Care sunt cerințele nutritive ale pacienților cu afecțiuni specifice (cum ar fi SLA)?
- Există o diferență între hrănirea gastrică și cea jejunală la această populație?
- Care sunt dorințele pacientului și ale familiei în ceea ce privește tratamentul nutrițional?
4. Alimentarea tubului/plasarea PEG în tulburările neurodegenerative
- Comportamente selective (refuză să mănânce o gamă largă de alimente). Aceste tulburări necesită modificări ale dietei.
- Comportamente active (rezistență la hrănire, cu reflexe defensive).
- Dispraxie orală și tulburări de atenție.
- Disfagie orofaringiană (pierderea coordonării musculare în timpul masticării și înghițirii, care poate duce la probleme repetate de înghițire și sufocare).
În cursul clinic al demenței avansate, prevalența tulburărilor alimentare este foarte mare, la fel ca și mortalitatea generală legată de problemele alimentare.
Recent, au fost publicate liniile directoare ESPEN privind nutriția în demență (27). În orientări, sunt identificate diferitele probleme nutriționale care decurg din diferite stadii ale bolii (masa 2).
| masa 2 Probleme nutriționale de-a lungul etapelor demenței | |||||||||||||||||||
| Problemă nutrițională | Stadiul demenței |
| Disfuncție olfactivă și gustativă | Etapele preclinice și timpurii |
| Deficit de atenție | Ușor până la moderat |
| Deficite de funcție executivă (cumpărături, pregătirea mâncării) | Ușor până la moderat |
| Capacitate de decizie afectată (încetinirea alegerii alimentelor, aport redus) | Ușor până la moderat |
| Dispraxia (tulburări de coordonare, pierderea abilităților alimentare) | De la moderat la sever |
| Agnosia (Pierderea capacității de a recunoaște obiecte sau de a înțelege semnificația obiectelor, ceea ce înseamnă că alimentele nu pot fi distinse de cele non-alimentare și că ustensilele de mâncare nu sunt recunoscute ca ceea ce sunt) | De la moderat la sever |
| Probleme de comportament | De la moderat la sever |
| Disfagia orofaringiană | De la moderat la sever |
| Refuzul de a mânca |
Orientări practice pentru diagnosticul și gestionarea pierderii în greutate în AD (28)
- O dietă variată și echilibrată și o activitate fizică zilnică ar trebui recomandate fiecărui pacient cu AD pentru a preveni pierderea în greutate.
- Căutați cauze reversibile din punct de vedere medical sau socio-ambiental ale pierderii în greutate (inclusiv medicamente și, în special, inhibitori ai acetil colinesterazei în primele săptămâni de la debutul tratamentului).
- Profesioniștii din domeniul sănătății și îngrijitorii de familie ar trebui să urmeze o instruire centrată pe detectarea riscului nutrițional și pe alimentele/dieta acestor pacienți.
- Planificarea meselor (mâncăruri îmbogățite, fracționate, cu degete).
- A face pacientul să bea în mod regulat în timpul zilei. Prevenirea deshidratării face parte din managementul pacienților cu AD. Băuturile hrănitoare sunt recomandate în special.
Recent, în Ghidul ESPEN pentru nutriție în demență (27), au fost publicate mai multe recomandări:
5. Considerații etice referitoare la alimentarea cu tuburi la pacienții cu tulburări neurodegenerative cu demență avansată
6. Rezumat
7. Caz clinic
DS, un bărbat de 78 de ani a fost diagnosticat cu boala Parkinson (PD) în urmă cu 6 ani.
El a fost diabetic de tip 2 în ultimii 24 de ani. Inițial a fost administrat cu dietă, dar acum este tratat cu insulină din cauza nefropatiei diabetice incipiente (proteinurie). Simptomele PD au progresat în timp, iar pacientul a devenit incapabil să meargă și a dezvoltat dischinezie severă, cu episoade de akinezie post-prandială/rigiditate mai frecvent în ciuda tratamentului farmacologic.
Înălțime: 1,70 m și greutate 57 kg. IMC 19 kg/m 2 .
Un clinician a recomandat o dietă săracă în proteine.
DS a inițiat dieta cu conținut scăzut de proteine, cu o singură porție mică de proteine animale la cină (aproximativ 20 g proteine / zi).
Q1. Este adecvată această abordare dietetică?
DS a slăbit după 2 săptămâni de dietă. Controlul său glicemic se agravase.
Nu s-a observat nicio diferență în frecvența și durata episoadelor de akinezie. S-a recomandat oprirea dietei cu conținut scăzut de proteine. El a primit sfaturi pentru a redistribui proteinele dietetice pe tot parcursul zilei, evitând alimentele bogate în proteine în momentul levodopei sale pentru PD.
Doi ani mai târziu, avea nevoie de internare în spital din cauza unei infecții respiratorii. La momentul respectiv, s-a observat o progresie a PD, cu disfagie moderată.
Q2. Care sunt cele mai bune metode de confirmare a disfagiei în acest context? Q3. Care este acum cea mai bună cale pentru susținerea nutrițională?
În timpul spitalizării gastropareza a devenit evidentă, presupusă secundar diabetului și terapiei medicamentoase. În ciuda tratamentului procinetic și a EN continuă asistată cu pompă, a apărut pneumonie prin aspirație, asociată cu volume reziduale gastrice intractabil de mari.
Q4. Care este acum cea mai bună abordare nutrițională?
- Eficacitatea terapeutică a suportului nutrițional prin gastrostomie endoscopică percutană în mod critic
- Valoare nutrițională a mandarinei la 100g - Dietă și fitness astăzi
- Compoziția nutrițională a ciupercilor sălbatice comestibile selectate din Sicilia (sudul Italiei)
- Compoziția nutrițională a ciupercilor sălbatice comestibile selectate din Sicilia (sudul Italiei)
- Beneficiile nutriționale ale părinților din ouă
- Deținuții ex-Gitmo de la Pentagon se îndreaptă spre terorism în creștere
- Dezvăluit DVD-urile de antrenament ale celebrităților care chiar te vor face să te potrivești - cu Vicky de Geordie Shore
- Efectul acut al indicelui glicemic al mesei și al încărcăturii glicemice asupra răspunsurilor la glucoză din sânge și insulină în
- PU-ERH TEA Evaluări ale utilizatorilor pentru eficacitate, efecte secundare, siguranță și interacțiuni - WebMD
- 5 moduri simple de a evita plata taxelor pentru bagaje în exces la aeroport! Numai bagaje de mână - Călătorii,