Mark I. Evans, MD
Președinte, Departamentul de Obstetrică și Ginecologie, Universitatea MCP Hahneman, Philadelphia, Pennsylvania (Vol. 3, Cap. 83, 114)
The-Hung Bui, MD
Director, Programul de diagnostic fetal, Spitalul Karolinksa, Departamentul de Medicină Moleculară, Unități de genetică clinică, Stockholm, Suedia
(Vol 3, Cap 114)
Yuval Yaron, MD
Director, Unitatea de diagnostic genetic prenatal, Tel Aviv Sourasky Medical Center, Tel Aviv, Israel (Vol 3, Cap 114)
Depistarea tulburărilor genetice devine o parte din ce în ce mai mare a îngrijirilor obstetricale. În ciuda faptului că ginecologii folosesc abordări comparabile pentru cancerul de col uterin de zeci de ani, a existat întotdeauna o preocupare de bază în rândul oficialilor din sănătatea publică că extrapolarea la tulburări obstetric/fetale ar fi gestionată greșit. Aproape trei decenii de utilizare cu succes a alfa-fetoproteinei (AFP) și acum mai mulți markeri nu au atenuat aceste preocupări.
Identificarea persoanelor cu boli implică, de obicei, teste sau proceduri efectuate pe persoane despre care se crede că prezintă un risc crescut. Cu toate acestea, doar o mică parte din populația generală are suficient risc pentru a justifica efectuarea acestor teste. Pentru tulburările genetice, există adesea subgrupuri de populație despre care se știe că prezintă un risc deosebit de mare, fie că este vorba despre vârsta maternă avansată și sindromul Down, moștenirea africană și boala cu celule secera, moștenirea evreiască Ashkenazi și boala Tay-Sachs sau nenumărate altele. Pentru unele dintre aceste tulburări, deși riscul pentru o anumită persoană din categoria de risc ridicat este mai mare decât în categoria de risc scăzut, dacă categoria de risc ridicat este suficient de mică, majoritatea persoanelor afectate pot proveni dintr-o categorie de risc scăzut . 2 În special odată cu apariția tehnologiilor moleculare și a proiectului genomului uman, avem acum capacitatea de a căuta mii de tulburări potențiale la orice individ care ar putea fi total asimptomatic.
Fundamentul screeningului pentru orice proces de boală necesită o înțelegere fundamentală a diferențelor dintre testele de diagnostic și testele de screening. Testele de diagnostic sunt concepute pentru a oferi un răspuns definitiv la întrebarea are pacientul această problemă specială? Sunt în general teste complexe și necesită în mod obișnuit analize și interpretări sofisticate. Ele tind să fie scumpe și, de obicei, sunt efectuate numai la pacienții despre care se crede că sunt „expuși riscului”. În schimb, testele de screening sunt administrate pacienților sănătoși și adesea întregii populații relevante. Ar trebui să fie ieftine, ușor de utilizat și interpretabile de toată lumea; funcția lor este de a ajuta la definirea cine, în rândul grupului cu risc scăzut, este cu adevărat la risc ridicat. Rezultatele testelor de screening nu sunt prin definiție patognomonice pentru boală. Tot ce fac este să definească cine are nevoie de teste suplimentare. În ceea ce privește bolile genetice, întrebați un pacient „câți ani aveți?” nu este altceva decât un test de screening ieftin. Folosind vârsta maternă de 35 ca limită, 20% până la 30% din anomaliile cromozomiale, cum ar fi sindromul Down, pot fi detectate, deoarece acesta este procentul care apare la femeile mai mari de 35 de ani și cărora, în Statele Unite, li se oferă teste invazive pe această bază.
Încercările de a rafina sensibilitatea și specificitatea screening-ului cromozomial și de a reduce costurile globale ale programelor de screening în sine au fost centrul eforturilor mai recente. 1,2 Scopul este de a reduce nevoia de teste invazive costisitoare care urmează unui screening pozitiv și, deși nu este menționat în mod obișnuit, de a reduce costul îngrijirii nou-născuților anormali care, în urma screeningului, ar putea fi detectați și sarcina întreruptă dorințele părinților. 3.4 Lucrările care înconjoară un astfel de screening și reducerea incidenței defectelor congenitale se încadrează în patru categorii:
- Utilizarea acidului folic preconceptual și precoce pentru a reduce incidența defectelor tubului neural
- Utilizarea markerilor biochimici și ultrasunete în al doilea trimestru pentru a crește detectarea sindromului Down
- Extinderea markerilor biochimici în primul trimestru pentru a permite screening-ul la vârste gestaționale anterioare
- Dezvoltarea caracteristicilor biofizice-ultrasonice ale structurii fetale în primul și al doilea trimestru.
Defecte ale tubului neural
În anii 1970, Brock și Sutcliffe 5 au descris mai întâi utilizarea AFP în lichidul amniotic și mai târziu în serul matern 6 pentru detectarea prenatală a defectelor tubului neural. Screeningul prenatal de rutină a fost acceptat în Regatul Unit de la mijlocul anilor 1970 și în Statele Unite de la mijlocul anilor 1980. Evaluarea impactului unui astfel de screening a arătat că rata natalității copiilor cu defecte ale tubului neural a scăzut de la 1,3 la 1000 nașteri în 1970 la 0,6 la 1000 nașteri în 1989. 7 În unele secțiuni ale Statelor Unite, cum ar fi sud-estul, care a avut rate mai mari decât media, declinul a fost și mai dramatic.
Au fost observate mai multe modificări ale caracteristicilor epidemiologice ale defectelor tubului neural: (1) Proporția cazurilor de spina bifida a crescut. (2) Proporția defectelor tubului neural combinate cu alte defecte fără legătură (adică sindroame) a crescut. (3) Incidența la populația albă a scăzut față de incidența din alte rase. (4) Incidența defectelor izolate ale tubului neural la femei a scăzut. Toate constatările menționate anterior sunt în concordanță cu utilizarea crescută a screening-ului seric al AFP matern, în special la populația albă. Un studiu similar realizat în Australia de Sud de Chan și colegii 8 din 1966 până în 1991 a constatat că prevalența generală a defectelor tubului neural (inclusiv cazurile diagnosticate prenatal) nu a variat între cei doi ani. Cu toate acestea, a existat o reducere de 84% a nașterilor, de la 2,29 la 1000 în 1966 la 0,35 la 1000 în 1991. Scăderea a fost de 96% pentru anencefalie și de 82% pentru spina bifida. Aproximativ 85% din defectele deschise și închise au fost detectate înainte de 28 de săptămâni de gestație prin AFP sau ultrasunete. De asemenea, proporția întreruperilor în cazurile detectate prenatal a crescut constant, de la o medie de aproximativ 20% în 1980 la mai mult de 80% în 1991.
S-a apreciat mult timp că există variații rasiale, geografice și etnice în incidența defectelor tubului neural și că pacienții prezintă un risc crescut în funcție de alte afecțiuni medicale. Se știe că diabeticii prezintă un risc crescut de defecte ale tubului neural, la fel ca și femeile care iau medicamente antiepileptice. 9 În schimb, un studiu din 1992 a concluzionat că pacienții supuși inducției ovulației nu au rate mai mari decât defectele de tub neural decât cele de fond. 10
O întrebare importantă a fost asocierea acidului folic, deficiența acestuia și incidența defectelor tubului neural. Studiile experimentale, clinice și embriologice au investigat rolul vitaminelor ca factor cauzal. O atenție specială s-a concentrat asupra vitaminei B esențiale, acidul folic, care servește ca donator de metil implicat în sinteza acidului nucleic, metabolismul purinei-pirimidinei și sinteza proteinelor. 11 Din cauza nevoilor crescute de acid folic în timpul sarcinii, femeile însărcinate sunt deosebit de predispuse să dezvolte deficiențe relative. Alte influențe posibile includ dieta insuficientă; hemodiluția fiziologică a sarcinii; clearance-ul plasmatic crescut; și tulburări genetice care ar putea afecta producția, transportul și metabolismul. 12
De-a lungul anilor 1990, au existat numeroase studii care au încercat să suplimenteze acidul folic la femeile cu risc crescut de defecte ale tubului neural care, în general, au arătat o scădere a riscului de recurență pentru astfel de femei care au avut deja un copil afectat. SUA. Administrația pentru alimente și medicamente a mandatat, începând din 1998, suplimentarea cu acid folic a pâinii și a boabelor. Grupul nostru a arătat o scădere dramatică a proporției valorilor ridicate ale AFP serice materne în Statele Unite după introducerea suplimentării de rutină a pâinii și a boabelor. 22 Un alt studiu publicat a arătat o scădere cu 20% a defectelor tubului neural pe baza datelor certificabile. 23 Mai mulți alții au confirmat, de asemenea, o scădere remarcabilă a incidenței. 24
Depistarea anomaliilor cromozomiale
În 1984, Merkatz și colegii săi 25 au publicat pentru prima dată asocierea AFP cu ser matern scăzut cu un risc crescut de anomalii ale cromozomilor, în special sindromul Down. În anii următori, a existat o acceptare treptată a asocierii și a înțeles că sindromul Down nu este singura afecțiune aneuploidă asociată cu AFP serică scăzută maternă. Trisomia 18 are valori AFP chiar mai mici. 26
Adoptarea unui screening la scară largă cu AFP serică maternă a dublat efectiv detectarea potențială a anomaliilor cromozomiale în populație. Chiar și cu o populație de reproducere îmbătrânită, doar 25% până la 30% dintre sugarii cu sindrom Down sunt născuți de femei cu vârsta peste 35 de ani (Fig. 1). Adăugarea unui program de screening AFP seric matern bine coordonat poate detecta aproximativ 30% din 80% din cazurile care se nasc la femei mai mici de 35 de ani. Mecanica screeningului biochimic (adică cu ajustări pentru vârsta gestațională, rasă, diabetic statutul, starea de gestație multiplă și greutatea maternă și ajustările printr-o bază de date diferită sau factori de corecție pentru rasa maternă) au fost publicate anterior și nu sunt repetate aici. 27
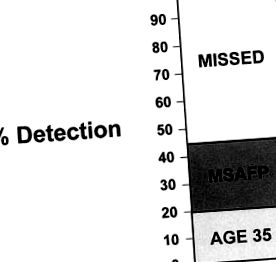
În 1988, Wald și asociații 28 au sugerat că o combinație de parametri incluzând AFP, β-gonadotropină cronică umană (β-HCG) și estriol neconjugat ar putea crește semnificativ frecvența de detectare a sindromului Down la aproximativ 60% din total (Fig. 2 ). Studii multiple au confirmat eficacitatea crescută a screening-ului cu markeri multipli, spre deosebire de AFP singură în detectarea anomaliilor cromozomiale, în special a sindromului Down. 29,30,31,32,33,34
FIG. 2. Detectarea prin screening dublu și triplu. Testarea concomitentă a nivelurilor de gonadotropină corionică umană și de estriol îmbunătățește rata de screening alfa-fetoproteinei la aproximativ 60%. MSAFP, alfa-fetoproteină serică maternă.
În ciuda datelor și recomandărilor copleșitoare din partea organizațiilor naționale, cum ar fi Colegiul American de Obstetrică și Ginecologie, care a oferit screening cu markeri multipli, aproape 20% dintre pacienții din Statele Unite care au screening încă au AFP singuri. 35 Există un acord esențial universal că dintre cei trei parametri comuni utilizați, AFP, β-HCG și estriol neconjugat, că dacă s-ar putea alege doar unul dintre cele de mai sus, că β-HCG este cel mai bun. Există o legătură virtuală pentru locul al doilea în eficacitate între AFP și estriol neconjugat. Deoarece AFP este deja utilizat în America de Nord și o mare parte din Europa de Vest pentru detectarea defectelor tubului neural, totuși, singura întrebare rămasă reală este dacă adăugarea de estriol neconjugat ca al treilea parametru este rentabilă.
Evans și colegii 37 au investigat multe dintre „dogmele” celor 3 decenii de screening biochimic și au constatat că multe dintre acestea nu mai sunt valabile. Credem că variația largă a rezultatelor raportate din întreaga lume se datorează în mare parte diferențelor subtile și uneori nu atât de subtile în metodele de laborator. 37 Argumentele amare despre screeningul dublu versus triplul sunt, parțial, răspunse de faptul că există o variabilitate mult mai largă a măsurătorilor estriolului decât alți parametri. O astfel de variație ajută la explicarea de ce laboratoarele au o experiență atât de divergentă cu estriolul. Când metodele sunt standardizate, o mare parte din variabilitate dispare și permite o comparație „mere versus mere”, spre deosebire de comparația „mere versus portocale”. În mod similar, o mare parte a variației raportate în literatură dispare, de asemenea, odată cu standardizarea, iar factorul de corecție diabetic devine inutil, luând în considerare corect faptul că pacienții diabetici au o greutate maternă mai mare. 39,40
Multe articole din ultimii ani s-au uitat la diferiții constituenți din regimul marker, cele mai importante fiind promovate fiind utilizate în al doilea trimestru de β-HCG liber, spre deosebire de β-HCG intact. Wald și Hackshaw 41 au raportat în 1993 că utilizarea β-HCG liberă în comparație cu β-HCG totală ar crește frecvența de detectare cu aproximativ 4% pentru o anumită rată fals pozitivă utilizată împreună cu vârsta maternă, AFP și estriol neconjugat. Alte studii au sugerat că, în special la vârste gestaționale anterioare (de exemplu, 14 și 15 săptămâni), β-HCG liber poate avea o sensibilitate și o specificitate mai bune decât molecula intactă.
Un alt marker promițător a fost căutarea celulelor fetale în circulația maternă. Studiile din anii 1990 au sugerat că izolarea și analiza celulelor fetale pot deveni practice și utile ca test de screening. 42,43,44 Starea actuală urmează în esență 2 decenii de diferite porniri și opriri care, alternativ, au arătat promițătoare și frustrante, deoarece Hertzenberg și colegii săi 45 au arătat pentru prima dată detectarea și îmbogățirea prin sortarea celulelor fluorescente activate. O mare parte a activității din ultimele 2 decenii s-a concentrat pe modalități de îmbunătățire a eficacității metodelor de detectare axate în primul rând pe necesitatea creșterii îmbogățirii celulelor fetale din circulația sanguină maternă a cărei prevalență a fost estimată la aproximativ 1 din 10 milioane de celule . 46,47,48
O altă zonă a aplicabilității potențiale a celulelor fetale în sângele matern este pentru izolarea diagnosticului molecular al tulburărilor mendeliene. Lo și asociații 50 au putut determina starea Rh fetală la femeile despre care se știe că sunt sensibilizate și căsătorite cu bărbați heterozigoți. Geifman-Holtzman și colegii 51 au determinat statutul Rh fetal folosind reacția în lanț a polimerazei celule roșii din sânge nucleate fetale sortate din sângele matern. Următorii câțiva ani vor determina în cele din urmă cât de reușită este sortarea celulelor fetale ca test de screening. S-a sperat inițial că ar putea fi un test de diagnostic și să înlocuiască nevoia de teste invazive; cu toate acestea, încă din această scriere, cariotipurile fetale nu pot fi obținute din celule izolate și doar fluorescență in situ sunt posibile rezultate legate de hibridizare. Deși este bun ca un test de screening pentru aneuploidie, experiențele noastre arată că aproximativ o treime din cariotipurile anormale observate în programele de diagnostic prenatal nu sunt cele care ar fi detectate de sondele standard pentru cromozomii 13, 18, 21, X și Y. 52 Până și dacă nu pot fi obținute cariotipuri complete, celulele fetale nu vor înlocui testele invazive, dar pot fi un plus important în armamentariul tehnologiilor de screening.
Multe studii au sugerat inhibina dimerică A ca un marker excelent care poate crește sensibilitatea cu 3% până la 7% pentru o anumită rată ecran-pozitivă. 53 Unii au sugerat screening-ul cvadruplu. Există, de asemenea, paradigme care includ parametri diferiți în momente diferite combinate. Deși datele preliminare sugerează o sensibilitate ridicată cu specificitate îmbunătățită, ascunderea rezultatelor de la pacienți până la o lună este problematică din punct de vedere etic în opinia noastră. Fără îndoială, există multiple abordări ale screeningului și nu va exista o abordare standard uniformă.
O altă abordare în doi pași a fost așa-numitul test integrat. 54 Aceasta este o combinație de sânge în primul trimestru și ultrasunete. Rezultatele nu sunt comunicate pacientului, care așteaptă apoi rezultatele de sânge din al doilea trimestru înainte de a se face o evaluare a riscului. Datele preliminare sugerează o rată fals-pozitivă redusă pentru o sensibilitate comparabilă, dar compromisul este necesitatea ca pacienții să aștepte 6 săptămâni pentru a începe finalizarea procesului de screening. Pentru pacienții cărora nu le pasă în mod deosebit de rezultate, întârzierea poate fi bună, dar mulți pacienți consideră că această întârziere este intolerabilă.
Deși screening-ul s-a concentrat în general pe trisomia 21, datele noastre și cele ale altora au arătat întotdeauna un model variat de anomalii detectate prin screening. 55 Un tipar diferit de niveluri analitice a fost observat în trisomia 18. Valorile AFP, β-HCG și estriol neconjugat par a fi scăzute. 56 Aceste valori scăzute sugerează o fiziopatologie diferită de cea a sindromului Down. În sindromul Down, AFP scăzut și estriol neconjugat și β-HCG ridicat pot fi explicate ca reflectând imaturitate inadecvată sau dismaturitate a fătului (adică toate valorile sunt în concordanță cu o vârstă gestațională mai mică). În trisomia 18, această explicație nu funcționează. Am arătat anterior că există diferite modele de întârziere a creșterii intrauterine direcționate genomic în diferite aneuploidii, dar modul în care acest lucru se traduce prin markeri serici nu este clar. Cu toate acestea, unele rapoarte au arătat că un algoritm poate fi utilizat pentru a identifica cele mai multe cazuri de trisomie 18, în timp ce se adaugă aproximativ 0,75% populației care i se oferă amniocenteză.
Dintre toți markerii serici materni evaluați, proteina plasmatică asociată sarcinii A (PAPP-A) și β-hCG liber au apărut ca fiind cei mai predictivi dintre toți ca potențiali markeri pentru screeningul sindromului Down în primul trimestru. 57,58,59,60,61 Canick și Kellner 61 au analizat screening-ul sindromului Down în primul trimestru (8-13 săptămâni gestaționale) cu analiți serici materni. PAPP-A și β-HCG liber s-au remarcat printre cei mai promițători markeri. Ei au estimat că performanța screeningului sindromului Down al acestor analiți în combinație cu vârsta maternă este o rată de detectare de 60% cu o rată fals pozitivă de 5%. Acest lucru este similar cu performanța de screening a screening-ului dublu al doilea trimestru, dar mai puțin eficient decât screening-ul triplu sau cvadruplu din al doilea trimestru. Canick și Kellner 61 au ajuns la concluzia că screening-ul în primul trimestru numai cu markeri serici nu poate fi recomandat decât în cazurile în care screeningul în al doilea trimestru nu poate fi efectuat.
Test integrat (screening în primul trimestru și al doilea trimestru)
Demonstrația conform căreia screening-ul biochimic cu markeri multipli ar detecta majoritatea fetușilor cu anomalii cromozomiale, cum ar fi sindromul Down, a declanșat dezbateri politice și etice în America de Nord și Europa. Haddow și colegii 69 au arătat că la femeile cu vârsta peste 35 de ani, aproape 90% din fetușii cu sindrom Down pot fi detectați, reducând în același timp numărul amniocentezei cu poate jumătate sau mai mult. Din punct de vedere pur al sănătății publice și al perspectivelor matematice, refuzul accesului la femeile mai mari de 35 de ani ale căror ecrane biochimice nu îndeplinesc un nivel de risc suficient de ridicat pentru a justifica cheltuielile de resurse ar putea părea adecvat. Cu toate acestea, o astfel de abordare ar necesita o reorientare a filosofiei și o înlăturare a autonomiei pacientului asupra acestor probleme. Cu toate acestea, atunci când autonomia și dolarul public intră în conflict, este rezonabil să ne așteptăm la dezacorduri cu privire la utilizarea adecvată a acestor resurse.
Czeizel 24 a rezumat datele despre ce proporție de anomalii congenitale ar putea fi detectate și prevenite. Czeizel credea că aproximativ 51 din 73 de tipuri de anomalii congenitale (70%) ar putea fi evaluate. Prevalența nașterii tuturor anomaliilor congenitale ar putea fi redusă de la aproximativ 65 la 26 la 1000; 39 la 1000 sau 60% sunt prevenite. Deși multe anomalii congenitale pot fi prevenite, ele nu reprezintă o singură categorie patologică și nu există o strategie unică pentru prevenirea lor care să fie adecvată.
- Variațiile în volumul cerealelor afectează cantitatea selectată și consumată la micul dejun
- Jurnalul Obezității Deschise - Volumul 2
- OMS EMRO Picior plat printre armata saudită recrutează prevalența și factorii de risc Volumul 12, numărul
- Mănâncarea volumului
- Volumul 22 Numărul 5 Acarologie sistematică și aplicată
