Termeni asociați:
- Ingineria energetică
- Litiu
- Baterii litiu-ion
- Pila de combustibil microbiană
- Grafit
- Anod
- Carbon activat
- Lianți
- Anod inert
- Cola de petrol
Descărcați în format PDF
Despre această pagină
Carboni derivati din carbune
PETER G. STANSBERRY,. ALFRED H. STILLER, în Carbon Materials for Advanced Technologies, 1999
1 4 Fabricarea grafitului și anodului
Anodii de carbon industriali și grafitii artificiali nu sunt un singur material, ci sunt mai degrabă membri ai unei largi familii de carbon pur pur. Din fericire, grafitii artificiali pot fi adaptați pentru a varia foarte mult în ceea ce privește rezistența, densitatea, conductivitatea, structura porilor și dezvoltarea cristalină. Aceste atribute contribuie la aplicabilitatea lor pe scară largă. Caracteristicile specifice sunt conferite produsului finit prin controlul selectării materialelor precursoare și a metodei de prelucrare [19]
Procesele pentru fabricarea anodilor de carbon și a electrozilor de grafit sunt foarte similare și, în unele cazuri, se suprapun. Materiile prime de bază sunt cocsul calcinat (cocs de umplutură) și pasul de gudron de cărbune. În mod convențional, procesul începe prin măcinarea și dimensionarea cocsului de petrol calcinat la diferite dimensiuni pentru recombinare în proporții dictate de utilizarea finală; grafitul fin, grafitii cu densitate mare necesită particule de cocs de dimensiuni micronice, în timp ce particulele de cocs pentru anodi pot avea dimensiuni de centimetri. Coca-cola metalurgică și cărbunele antracit pot fi utilizate ca materiale de umplutură, dar introducerea lor crește nivelul de contaminare de către metale, precum și reduce conductivitatea. Coca-cola de gudron de cărbune este, de asemenea, acceptabilă și este utilizată în țările cu resurse de petrol limitate, dar accesibile. Amestecul de cocs este apoi adăugat la un pas de liant topit și amestecat pentru a permite pasului să ude suprafața de cocs. În funcție de porozitatea cocsului și a altor variabile, aproximativ o parte a pasului de liant este combinată cu trei părți de cocs în fiecare lot de amestecare. Se menține o temperatură suficientă astfel încât amestecul să fie plastic pentru modelare fie prin turnare, fie prin extrudare. Obiectele modelate sunt răcite pentru a întări liantul pentru manipulare, depozitare și eventuală prelucrare ulterioară.
Coacerea este următorul pas. La alegerea cuptorului adecvat, flexibilitatea funcționării și controlul temperaturii sunt considerente cheie. Un cuptor obișnuit de coacere este cuptorul în groapă, în care articolele formate sunt strânse cu grijă. Materialul de ambalare alcătuit din particule fine de cocs (briză) sau nisip este plasat în jurul stocului verde pentru a preveni lăsarea și distorsiunea și pentru a oferi un mediu poros pentru eliberarea substanțelor volatile. Ciclul de ardere este atent monitorizat pentru a se încălzi de la 2 la 10 ° C pe oră până la aproximativ 1000 ° C, durând adesea câteva săptămâni până la finalizare. Pe măsură ce temperatura crește, liantul suferă piroliză și fuzionează cocsul într-o masă solidă. După răcire, materialul de ambalare este îndepărtat și articolele coapte examinate pentru defecte, finisate și utilizate ca anodi de carbon
În unele aplicații articolul coapte ar fi tratat termic în continuare (grafitizare). În timpul grafitizării, stocul este poziționat în cuptorul de grafitizare și acoperit cu material de ambalare. Sunt utilizate două modele de stivuire. În cuptorul Acheson stocul este aranjat în coloane verticale care sunt transversale față de axa cuptorului, cu ambalaj de cocs între fiecare coloană. Ambalajul funcționează ca un rezistor. În procesul Castner, stocul este plasat în rânduri paralele cu axa cuptorului, cu stocul atingându-se unul de altul cap la cap. În acest caz, stocul este rezistența.
Grafitizarea se realizează prin trecerea unui curent electric prin fiecare pat. O încălzire rezistivă considerabilă are loc atunci când sunt posibile temperaturi care depășesc 3000 ° C. Parametrii normali ai procesului utilizează rate de încălzire între 30 și 70 ° C pe oră până la 2500 ° C. Timpul total la temperatură depinde de mărimea artefactului. Mai erau necesare câteva zile pentru a răci cuptorul înainte de despachetare.
În timpul tratamentului la temperaturi ridicate, carbonul suferă modificări dramatice ale proprietăților. Cele mai importante efecte sunt rearanjarea moleculară a carbonului amorf într-o structură grafică mai ordonată. În consecință, acele caracteristici asociate cu grafit, inclusiv cristalinitate ridicată, coeficient scăzut de expansiune termică, rezistență electrică scăzută, conductivitate termică ridicată și rezistență la șoc termic sunt transmise.
Aplicații ale materialelor carbon avansate la bateria secundară litiu-ion
Morinobu Endo, Yoong Ahm Kim și Carbon Alloys, 2003
1. Introducere
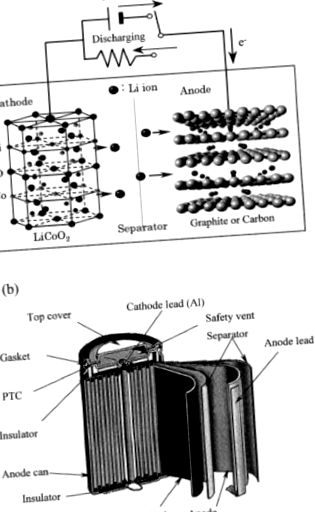
În bateriile reîncărcabile Li-ion, bazate pe conceptul de balansoar sau cocoș navetă, ionii de litiu se deplasează ușor înainte și înapoi între gazdele de intercalație ale catodului și anodului. Astfel, bateriile secundare litiu-ion constau dintr-un anod carbonic și un oxid de metal de tranziție cu litiu, cum ar fi LiCoO2, LiNiO2 și LiMn2O4 ca catod, așa cum se arată în Fig. 1 a. Anodul pe folia de Cu și catodul pe folia de Al sunt formate în forme spiralate sau pliate, care dau un tip cilindric US18650 (18 mm diametru și 650 mm înălțime, Fig. 1b) și celule prismatice. Între acești doi electrozi, este plasat un separator polimeric poros de poliolefină cu aproximativ 25 μm grosime, realizat din polietilenă (PE) și polipropilenă (PP) (Fig. 1b) [16, 17]. Figura 2 prezintă fotografii SEM ale anodilor în care se formează foi de carbon pe ambele părți ale unui cablu din folie de cupru. Electrolitul este un lichid organic, cum ar fi PC, EC + DEC sau un polimer de tip gel dezvoltat recent, stabil sub tensiuni ridicate. O sare de litiu precum LiClO4, LiBF4 și LiPF6 este dizolvată în electrolit.
FIG. 1. (a) Mecanismul de încărcare/descărcare a bateriei secundare Li-ion; (b) celulă cilindrică.
FIG. 2. Fotografii SEM ale foilor de anod de carbon formate pe ambele părți ale unui plumb cu folie de Cu.
O capacitate teoretică de stocare a litiului unui anod de grafit pentru o baterie secundară Li-ion ar putea fi de 372 mAh g -1 și să corespundă etapei I GIC LiC6. Reacțiile totale de încărcare/descărcare și reacția anodică bazate pe intercalarea Li și intercalarea sunt după cum urmează [18]:
Pe de altă parte, au fost raportate carboni dezordinați cu capacități de stocare a litiului care depășesc capacitatea teoretică. Acest fenomen este încă dificil de explicat prin mecanismul de formare a GIC menționat mai sus și sunt necesare noi explicații.
Tehnologii de stocare a energiei
Fayaz Hussain,. M. Hasanuzzaman, în Energie pentru dezvoltare durabilă, 2020
6.2.1.2 Baterie cu litiu oxid de cobalt
În aceste baterii cu litiu oxid de cobalt (LiCoO 2) se utilizează un catod oxid de cobalt și un anod carbon grafit. FIG. 6.3 arată ilustrația schematică a unei baterii litiu-ion. Anodul (grafit) și catodul (LiCoO2) sunt separați de un electrolit lichid neapos (Xia, Luo și Xie, 2012). Utilizarea acestor baterii în aplicații precum laptopuri, camere digitale și telefoane este o alegere potrivită datorită energiei specifice ridicate, deoarece acestea pot fi operate între 3 și 4,2 V. Aceste baterii pot rezista la cicluri de încărcare-descărcare de până la 1000 înainte de scăderea semnificativă a performanței lor. Densitatea energiei bateriei este de minimum 150 și maximă de 200 Wh/kg. Cu toate acestea, celulele speciale pot ajunge până la o densitate de energie specifică de 240 Wh/kg. Astfel, există câteva dezavantaje principale ale acestor baterii, cum ar fi capacitățile specifice de alimentare limitate, durata scurtă de viață și stabilitatea termică scăzută care pot provoca supraîncălzirea acestor baterii.
Figura 6.3. Ilustrația schematică a unei baterii litiu-ion. Anodul (grafit) și catodul (LiCoO2) sunt separați de un electrolit lichid neapos (Xia și colab., 2012).
PROPRIETĂȚI TERMICE DE DESCĂRCARE DE GAZ-ARC FĂRĂ GRAVITATE MĂSURATĂ ÎN AVION JET ȘI APLICAȚIA SA LA PRODUCȚIA DE NANOUBURI
3.3 Observarea TEM a SWNT-urilor
SWNT-urile sunt produse prin utilizarea amestecului de catalizatori anod de carbon. Funinginea de carbon produsă în partea superioară a reactorului este colectată și amestecată bine. O parte din probă este sonicată în alcool și aruncată într-un suport de plasă de cupru.
Această probă este observată de un TEM (JEOL Co., 200 kV). Figurile 4 (a) și (b) prezintă fotografiile TEM sub gravitația G = 0. Figurile 4 (c) și (d) prezintă rezultatele sub G = 1 g0. Se recunoaște că există SWNT-uri, particule de carbon și de metal de tip amorf. Deși este dificil de verificat tot eșantionul, se poate sublinia că densitatea SWNT-urilor sub G = 0 este mai mare decât cea sub G = 1 g0.
FIG. 4 . Fotografii TEM tipice ale SWNTS sub G = 0 (a), (b) și G = 1g0 (c), (d).
Din fotografiile TEM, se numără numărul SWNT-urilor dintr-un flux și se măsoară numărul distribuției SWNT-urilor. Figura 5 prezintă graficele cu bare ale distribuțiilor pentru cele două cazuri de gravitație. Se confirmă faptul că pachete mai grase de SWNT tind să fie produse în condiții fără gravitație.
FIG. 5 . Număr de distribuție SWNTs într-un flux pentru cele două condiții de gravitație.
Distribuția diametrului SWNT-urilor este, de asemenea, măsurată din fotografiile TEM și prezentate în Fig. 6. De asemenea, se confirmă faptul că SWNT-urile mai grase tind să fie produse în condiții fără gravitație. Diametrul principal al SWNTS sub G = 0 este de aproximativ 1,5 nm, ceea ce este în concordanță cu rezultatele măsurării modurilor de respirație ale spectrului Raman.
FIG. 6 . Distribuția în diametru a SWNT-urilor pentru cele două condiții de gravitație.
Analiza lianților de gudron de cărbune pentru electrozi
B Consum de anod
Există un acord general că dezintegrarea suprafeței anodilor de carbon în timpul electrolizei sărurilor topite este influențată de oxidarea preferențială a cocsului liant. Această așa-numită tendință de praf se manifestă ca un consum excesiv, exprimat ca procent din cel corespunzător formării dioxidului de carbon la o eficiență Faraday de 100%. Este deosebit de important să se controleze consumul de anod în producția electrolitică de aluminiu, nu numai pentru că pierderea de carbon este stoichiometric, dar și pentru că particulele de carbon erodate se amestecă cu baia de criolit.
Electrozii de test pre-coapte, realizați cu liant și fine de cocs, au fost evaluați în laborator pentru reactivitatea oxidativă prin încălzirea la 950 ° C într-un cuptor cu tub vertical într-un curent lent de dioxid de carbon (Bowitz și colab., 1958, 1963). Reactivitatea a fost legată de (a) microporozitatea electrodului, adică procentul de pori mai mic de 6 μm, care poate fi determinat picnometric folosind mercur sau prin deplasarea cu abur (Darney, 1958); și (b) diferența dintre suprafața specifică a cocsului liant și cea a agregatului uscat. S-a raportat că reactivitatea unui amestec cocsificat a fost mai mare cu un factor de 10 decât cel al liantului cocsificat sau al agregatului uscat determinat individual (Bowitz și colab., 1958). Creșterea ratei de coacere a unui electrod a dus la o porozitate mai mare, diferențe mai mari în suprafața specifică și o reactivitate mai mare. Toate aceste proprietăți au fost legate de punctul de înmuiere, greutatea specifică, valoarea cocsificării și aromaticitatea liantului.
Watanabe (1963) a efectuat teste electrolitice pe anodi de tip Soderberg, realizate cu lianți din distilarea gudronului de cocs de temperatură înaltă, atât în soluție apoasă de hidroxid de sodiu, cât și în aluminiu-criolit topit. În alcalinele apoase, determinarea structurii cristaline a electrodului prin difracție cu raze X a indicat că regiunile amorfe trebuie oxidate preferențial. În ambele medii s-a observat o corelație rezonabilă între consumul de anod și gradul de oxidare selectivă a cocsului liant și a agregatului uscat. S-a recomandat utilizarea unui pitch cu o valoare de cocsificare cât mai mare posibil.
A fost investigată posibilitatea ca un consum de carbon mai mare decât stoichiometricul din celulele industriale să fie din cauza reactivității cu dioxidul de carbon. Scalliet (1963) a observat o corelație aproximativă cu anodii pre-coapte, dar nu cu anodii Soderberg. Hollingshead și Braunwarth (1963), folosind un electrolit de bază criolit într-o celulă mică încălzită extern, au descoperit că doar o mică parte din consumul în exces de specimene de anod de carbon era atribuibilă formării de monoxid de carbon; cea mai mare parte s-a datorat eroziunii particulelor de carbon prin oxidarea selectivă a cocsului liant. Un test Alcan se bazează pe această lucrare.
Mason (1970) a calculat coeficienții de corelație între diferitele proprietăți de înălțime și reactivitatea anodului. S-au observat valori mari ale coeficientului de corelație pentru raportul atomic carbon-hidrogen sau valoarea cocsificării (metoda Alcan) a următoarelor fracții de greutate moleculară mai mică: rășini C2, rășini C3 și solubile de acetonă, față de rata consumului de anod în testul Alcan. Mason a concluzionat că specificațiile actuale ale liantului, care sunt direcționate către producerea de anodi cu rezistență și porozitate adecvate, nu asigură neapărat un consum redus de anod.
Recent a fost descris un aparat de laborator care a fost folosit de câțiva ani pentru a evalua calitatea gudronului de cărbune și a lianților de petrol prin performanța electrozilor de carbon din sărurile topite (Pendley și Bullough, 1975). Două liante de gudron de cărbune utilizate ca standard aveau proprietăți tipice. Nouăsprezece gropi de petrol având în general puncte de înmuiere mai mari, conținând mult mai puțin material solubil în benzen și foarte puțin insolubile de chinolină, și cu o valoare de cocsificare și aromaticitate mai mici decât gropile de gudron de cărbune, au produs electrozi cu o densitate aparentă mai mică și o rezistență electrică mai mare, dar cu o electrolitică în general echivalentă reactivitatea în sărurile topite. Aceste date par să susțină afirmația lui Mason că consumul de anod nu este previzibil doar pe baza specificațiilor actuale ale liantului.
- Nevroza anxietății - o prezentare generală Subiecte ScienceDirect
- Antiandrogen - o prezentare generală a subiectelor ScienceDirect
- Butanol - o prezentare generală a subiectelor ScienceDirect
- Betulin - o prezentare generală Subiecte ScienceDirect
- Receptor adrenergic beta-2 - o prezentare generală a subiectelor ScienceDirect