Subiecte
Abstract
Experimentul a fost realizat pentru a examina efectul unei diete bogate în grăsimi (HFD) asupra hiperreagonității căilor respiratorii (AHR) la șoareci. Douăzeci și trei de șoareci adulți C57BL/6 J de sex masculin au fost hrăniți cu HFD sau dietă regulată de chow timp de două săptămâni. Rezistența respiratorie totală a fost măsurată prin tehnica de oscilație forțată la momentul inițial și după provocarea aerosolului cu metacolină la 1, 3, 10 și 30 mg/ml. S-a efectuat spălarea bronhoalveolară (BAL). Nivelurile lipidice și peroxidarea lipidelor în țesutul pulmonar au fost măsurate împreună cu expresia genică a citokinelor multiple. Plămânii au fost digerați și s-a determinat secreția de IL-1β prin macrofage pulmonare. Hrănirea cu HFD a dus la o greutate corporală cu 11% mai mare comparativ cu chow. HFD nu a afectat rezistența respiratorie la momentul inițial, dar a crescut semnificativ răspunsurile căilor respiratorii la metacolină comparativ cu dieta chow (creștere cu 40,5 ± 17,7% la 30 mg/ml metacolină, p
Introducere
Astmul este una dintre cele mai frecvente boli și prevalența astmului continuă să crească, care a fost atribuită epidemiilor de obezitate 1,2,3. Astmul în obezitate pare să fie diferit de astmul alergic tipic condus de TH2, demonstrând un răspuns slab la corticosteroizii inhalați 4. Mecanismele posibile includ respirația la volume pulmonare mai mici, modificarea structurii căilor respiratorii, stresul oxidativ crescut al căilor respiratorii și o inflamație sistemică mai mare 5. Reglarea în sus a inflammasomului NLRP3 și a IL-1β a fost implicată în astmul în obezitatea indusă de dieta bogată în grăsimi (HFD) 6. HFD este proinflamator datorită efectelor directe ale acizilor grași liberi 7. Cu toate acestea, efectul unei diete bogate în grăsimi în sine asupra hiperreactivității căilor respiratorii (AHR) nu a fost investigat. Ipotezăm că dieta bogată în grăsimi induce inflamații care pot afecta AHR independent de obezitate.
Metode
Animale experimentale
Douăzeci și trei de șoareci adulți C57BL/6 J de vârstă de 10 săptămâni (Laboratorul Jackson, Bar Harbor, MA) au fost hrăniți cu HFD (TD 03584, Teklad WI, 5,4 kcal/g, 35,2% grăsime, 58,4% kcal din grăsime, n = 10) sau dieta chow (3,0 kcal/g, 4,4% grăsimi, 13% kcal din grăsimi, n = 13) timp de 14 zile. Detalii despre compoziția HFD sunt furnizate în tabelul suplimentar 1. HFD a fost refrigerat la 4-8 ° C înainte de a fi adăugat în cuști. A fost asigurată hrană și apă ad libitum. Șoarecii au fost adăpostiți într-un mediu de laborator standard la 22 ° C în ciclul de lumină/întuneric de 12 ore (luminile 9:00 - 21:00 aprinse/21:00 - 9:00 luminile stinse). Pentru a asigura reproductibilitatea măsurătorilor, șoarecii au fost separați în două loturi (lot 1, HFD, n = 5, dieta chow, n = 6; lot 2, HFD, n = 5, dieta chow, n = 7), care au fost studiate la șase luni distanță folosind diferite loturi de HFD. Studiul a fost aprobat de Comitetul pentru îngrijirea și utilizarea animalelor de la Universitatea Johns Hopkins (Protocolul # MO15M257) și a respectat Ghidul Societății Fiziologice Americane pentru Studii pe Animale.
Măsurători fiziologice și histologie
În ziua 14, șoarecii au fost anesteziați cu ketamină/xilazină ip, traheostomizați și rezistența respiratorie totală (Rrs) a fost măsurată prin tehnica de oscilație forțată (Flexivent) la momentul inițial și după provocarea aerosolului cu metacolină la 1, 3, 10 și 30 mg/ml așa cum este descris 8.9. Sângele a fost colectat din aorta, spălarea bronhoalveolară (BAL) a fost efectuată cu 2 × 0,8 ml de soluție salină sterilă tamponată cu fosfat (PBS) printr-o canulă traheală. Toracele a fost deschis, iar plămânul drept a fost legat, disecat liber și înghețat imediat în azot lichid și depozitat la -80 ° C. Plămânul stâng rămas a fost umflat cu formalină la presiune de 26 cmH2O timp de 20 de minute, legat și plasat umflat în formalină timp de 2 zile. Volumul plămânului stâng a fost măsurat prin înlocuirea apei.
Pentru histologie, plămânul stâng a fost deshidratat în etanol și încorporat în parafină. Pentru morfometrie, secțiuni groase de 5 μm au fost tăiate din blocuri transversale și colorate cu tricrom Masson.
Analiza sângelui, a plasmei și a țesutului pulmonar
S-au determinat hemogramele complete (CBC). Trigliceridele și acizii grași liberi (FFA) au fost măsurați în omogenate pulmonare și plasmă cu truse de la Wako Inc (Richmond, VA). Insulina plasmatică și leptina au fost măsurate cu kituri de la Alpco Diagnostics (Salem, NH) și, respectiv, Abcam (Cambridge, MA). Nivelurile de glucoză din sânge au fost măsurate cu un glucometru (ACCU-CHECK Aviva Plus, Roche, Indianapolis, IN). ARN-ul total a fost extras din țesutul pulmonar cu un reactiv Trizol (Life Technologies, Rockville, MD). ADNc a fost produs din ARN total utilizând kitul Advantage RT pentru PCR de la Clontech (Palo Alto, CA). S-a efectuat PCR în timp real pentru panoul de citokine, inclusiv interleukinele (IL) 1β, 4, 5, 6, 10, 13, 17, TNF-α, IL-21, IL-23, adiponectină, leptină, proteina P3 a cutiei capului furcii (FOXP3), metalopeptidaza matricială (MMP 9), precum și receptorii asemănători (TLR) −2 și 4 cu grunduri premade de la Invitrogen (Carlsbad, CA) și sondele Taqman de la Applied Biosystems (Foster City, CA) folosind 18 S ca genă de menaj (Tabelul suplimentar 2).
Grundurile personalizate de 18 S au fost 5'-CTCTTTCGAGGCCCTGTAATTGT-3 ', invers, 5'-AACTGCAGCAACTTTAATATACGCTATT-3' și sonda 6FAM-AGTCCACTTTAAATCCTT. Nivelul de ARNm țintă a fost normalizat la 18 s ARNr, utilizând formula: Țintă/18 s = 2 Ct (18s) –Ct (țintă). Activitatea factorului nuclear κB (NF- κB) a fost derivată din proteina IκBα fosforilată la totală cu un kit de la Abcam. Peroxidarea lipidelor în plămâni a fost măsurată în funcție de nivelul de malondialdehidă cu un kit de la Abcam.
Secreție de citokine și citometrie în flux
Disponibilitatea datelor
Toate datele generate sau analizate în timpul acestui studiu sunt incluse în acest articol publicat.
analize statistice
Toate valorile sunt raportate ca medii ± SEM. Toate datele din studiu au fost verificate pentru normalitate cu un test de bunătate de potrivire chi pătrat. Comparațiile statistice ale valorilor distribuite în mod normal au fost efectuate prin testul U Mann-Whitney. Semnificația statistică pentru valorile distribuite în mod normal a fost determinată de testul t al studentului sau de analiza bidirecțională a testului varianței (ANOVA) cu corecția Bonferroni, atunci când este cazul. O valoare p de
Rezultate
Caracteristicile inițiale ale animalelor experimentale sunt descrise în Tabelul 1. HFD hrănirea timp de 2 săptămâni a dus la o greutate corporală cu 11% mai mare decât la șoarecii hrăniți cu chow dublând dimensiunea tampoanelor de grăsime epididimale și retroperitoneale. De remarcat, tampoanele de grăsime inghinale nu au fost crescute. Hrănirea cu HFD a indus hiperglicemie și creșteri ale nivelului de insulină și leptină în plasmă, în timp ce trigliceridele plasmatice au fost neschimbate (Tabelul 1). Nu a existat nicio diferență în CBC (Tabelul suplimentar 3). Dieta nu a afectat volumul plămânului stâng, care a fost de 0,16 ml ± 0,03 pe o dietă chow și 0,18 ± 0,03 pe HFD.
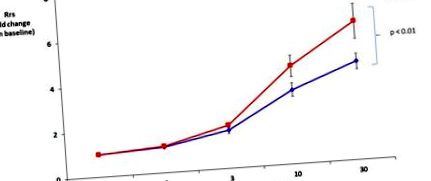
Testarea funcției pulmonare nu a evidențiat nicio diferență în rezistența pulmonară totală la momentul inițial între șoarecii hrăniți cu chow și HFD (Rrs de 0,69 ± 0,04 cm H2O * s/ml și respectiv 0,63 ± 0,03 cm H2O * s/ml). HFD a crescut semnificativ răspunsurile căilor respiratorii la metacolină în comparație cu dieta chow (Fig. 1).
Dieta bogată în grăsimi (HFD) a crescut rezistența totală a sistemului respirator (Rrs) ca răspuns la metacolină. Valorile Rrs au fost normalizate până la momentul inițial (fără diferențe semnificative între grupuri la momentul inițial).
Efectul dietei bogate în grăsimi (HFD) care se hrănește asupra populației de leucocite din plămânii de șoarece. Limfocitele CD4, CD8, macrofagele interstițiale, monocitele și macrofagele alveolare au fost identificate prin citometrie în flux conform protocolului descris de Misharin și colab. (ref. 10) în (A) suspensie totală de leucocite pulmonare și (B) populația de celule aderente așa cum este descris în metode.
Discuţie
Din câte știm, acesta este primul studiu care demonstrează că dieta bogată în grăsimi induce hiperreactivitatea căilor respiratorii (AHR) la începutul cursului, doar după două săptămâni de hrănire. O altă descoperire nouă a studiului este că alimentarea cu HFD induce expresia IL-1β în țesutul pulmonar și crește secreția de IL-1β în plămâni înainte de dezvoltarea obezității semnificative.
Care ar fi un mecanism potențial prin care grăsimile din dietă induc IL-1β în plămâni? La pacienții cu astm, o dietă bogată în grăsimi mărește inflamația căilor respiratorii și scade răspunsul căilor respiratorii la bronhodilatatoare 15. Celulele endoteliale microvasculare pulmonare sunt responsabile de absorbția trigliceridelor și de clearance-ul trigliceridelor 16. FFA poate activa calea NF-κB urmată de reglarea în sus a IL-1β 17. Un alt mecanism posibil ar fi activarea indusă de o dietă bogată în grăsimi a inflammasomului NLRP3 prin acizi grași sau cristale de colesterol în macrofagele pulmonare, rezultând producția de IL-1β. Cu toate acestea, nu am găsit o creștere a FFA sau activarea căii NF-κB. De asemenea, lipsa unui efect al HFD asupra IL-17, o componentă indispensabilă a inflammasomului poate argumenta împotriva acestui mecanism 6 .
Reglarea în sus a IL-1β nu este singurul mecanism posibil prin reactivitatea bronșică indusă de HFD. HFD a indus o creștere de 3 ori a leptinei plasmatice. La pacienții cu astm, leptina ridicată a fost asociată în mod independent cu severitatea bolii 18. Într-un model de șoarece, tratamentul cu leptină a indus răspunsul TH2 și inflamația alergică a căilor respiratorii 18. De remarcat, leptina poate crește, de asemenea, IL-1β 19.20, ceea ce ar fi în concordanță cu constatările actuale. În cele din urmă, datele noastre sugerează că alimentarea cu HFD timp de 2 săptămâni a indus manifestări timpurii ale sindromului metabolic, inclusiv depunerea de grăsime viscerală cu o dimensiune crescută a tampoanelor de grăsime viscerală (epididimale și retroperitoneale), dar nu tampoane de grăsime subcutanate (inghinale), hiperglicemie și hiperinsulinemie (tabelul 1). Coexistența sindromului metabolic și a astmului este bine documentată în literatura de specialitate 21. Inflamarea sistemică de grad scăzut observată în sindromul metabolic poate contribui la dezvoltarea astmului obez prin IL-1β și alte căi. Mai mult, tratamentul rezistenței la insulină, o manifestare distinctivă a sindromului metabolic, poate avea un efect benefic în astmul obez 22. .
Limitări
Principala limitare a studiului nostru este că rolul IL-1β în astmul indus de HFD nu a fost confirmat în experimentele mecaniciste folosind șoareci knock-out IL-1β sau blocanți ai receptorilor IL-1β. Cu toate acestea, această relație cauzală a fost demonstrată anterior de alți investigatori la șoareci cu obezitate indusă de dietă 6. Sunt necesare experimente viitoare care utilizează blocante ale receptorilor IL-1β.
Concluzie și implicații
Datele noastre sugerează că HFD poate induce rapid hipersensibilitatea căilor respiratorii înainte de dezvoltarea obezității semnificative cu implicarea timpurie a IL-1β. Având în vedere că producția de IL-1β nu răspunde la steroizi în astmul sever 23,24, datele noastre implică faptul că restricția dietetică a grăsimilor poate fi un adjuvant important la alte terapii utilizate în astmul obez.
Referințe
Akinbami, L. J. și Fryar, C. D. Prevalența actuală a astmului în funcție de greutate la adulți: Statele Unite, 2001-2014. Rezumatul datelor NCHS, 1-8 (2016).
Mosen, D. M., Schatz, M., Magid, D. J. și Camargo, C. A. Jr. Relația dintre obezitate și severitatea astmului și controlul la adulți. Jurnalul de alergie și imunologie clinică 122, 507–511.e506, https://doi.org/10.1016/j.jaci.2008.06.024 (2008).
Taylor, B. și colab. Indicele masei corporale și severitatea astmului în Studiul Național asupra Astmului. Torace 63, 14-20, https://doi.org/10.1136/thx.2007.082784 (2008).
Peters-Golden, M. și colab. Influența indicelui de masă corporală asupra răspunsului la agenții de control al astmului. Jurnalul respirator european 27, 495–503, https://doi.org/10.1183/09031936.06.00077205 (2006).
Shore, S. A. și Johnston, R. A. Obezitate și astm. Farmacologie și terapeutică 110, 83–102, https://doi.org/10.1016/j.pharmthera.2005.10.002 (2006).
Kim, H. Y. și colab. Celulele limfoide înnăscute producătoare de interleukină-17 și inflammasomul NLRP3 facilitează hiperreactivitatea căilor respiratorii asociate obezității. Medicina naturii 20, 54–61, https://doi.org/10.1038/nm.3423 (2014).
Kanneganti, T. D. și Dixit, V. D. Complicații imunologice ale obezității. Imunologia naturii 13, 707–712, https://doi.org/10.1038/ni.2343 (2012).
Bishai, J. M. și Mitzner, W. Efectul restricției severe de calorii asupra plămânului la două tulpini de șoareci. American Journal of Physiology - Lung Cellular and Molecular Physiology 295, L356 - L362, https://doi.org/10.1152/ajplung.00514.2007 (2008).
Soutiere, S. E. și Mitzner, W. La definirea capacității pulmonare totale la șoarece. Jurnal de fiziologie aplicată (Bethesda, MD: 1985) 96, 1658–1664, https://doi.org/10.1152/japplphysiol.01098.2003 (2004).
Misharin, A. V., Morales-Nebreda, L., Mutlu, G. M., Budinger, G. R. S. și Perlman, H. Analiza citometrică a fluxului de macrofage și subseturi de celule dendritice în plămânul de șoarece. Jurnalul american de celule respiratorii și biologie moleculară 49, 503–510, https://doi.org/10.1165/rcmb.2013-0086MA (2013).
Dixon, A. E. și Poynter, M. E. Mecanismele astmului în obezitate. Aspectele pleiotropice ale obezității produc fenotipuri distincte de astm. Jurnalul american de celule respiratorii și biologie moleculară 54, 601–608, https://doi.org/10.1165/rcmb.2016-0017PS (2016).
Ansell, T. K., Mitchell, H. W., McFawn, P. K. & Noble, P. B. TNF și expunerea la IL-1β cresc îngustarea căilor respiratorii, dar nu modifică răspunsul bronhodilatator la inspirația profundă în segmentele căilor respiratorii. Respirologie (Carlton, Vic.) 21, 1041–1048, https://doi.org/10.1111/resp.12800 (2016).
Scott, H. A., Gibson, P. G., Garg, M. L. & Wood, L. G. Inflamarea căilor respiratorii este crescută de obezitate și acizi grași în astm. Jurnalul respirator european 38, 594–602, https://doi.org/10.1183/09031936.00139810 (2011).
Telenga, E. D. și colab. Obezitate în astm: mai multă inflamație neutrofilă ca o posibilă explicație pentru un răspuns la tratament redus. Alergie 67, 1060-1068, https://doi.org/10.1111/j.1398-9995.2012.02855.x (2012).
Wood, L. G., Garg, M. L. și Gibson, P. G. O provocare bogată în grăsimi crește inflamația căilor respiratorii și afectează recuperarea bronhodilatatorului în astm. Jurnalul de alergie și imunologie clinică 127, 1133–1140, https://doi.org/10.1016/j.jaci.2011.01.036 (2011).
Yao, Q. și colab. Efectul hipoxiei cronice intermitente asupra absorbției trigliceridelor în diferite țesuturi. Journal of Lipid Research 54, 1058-1065, https://doi.org/10.1194/jlr.M034272 (2013).
Yang, W. și colab. Postul de zi alternativă protejează ficatul șoarecilor împotriva inflamației induse de dietă bogată în grăsimi asociată cu suprimarea semnalizării receptorului Toll-like 4/factor nuclear kappaB. Cercetare nutrițională (New York, New York) 36, 586–593, https://doi.org/10.1016/j.nutres.2016.02.001 (2016).
Zheng, H. și colab. Leptina îmbunătățește răspunsurile TH2 și ILC2 în boala alergică a căilor respiratorii. Jurnalul de chimie biologică 291, 22043-22052, https://doi.org/10.1074/jbc.M116.743187 (2016).
Boyd, C. A. Transportul placentar studiat prin intermediul veziculelor izolate cu membrană plasmatică. Proceedings of the Nutrition Society 50, 337-343 (1991).
Luheshi, G. N., Gardner, J. D., Rushforth, D. A., Loudon, A. S. & Rothwell, N. J. Acțiunile Leptinei asupra consumului de alimente și a temperaturii corpului sunt mediate de IL-1. Lucrările Academiei Naționale de Științe din Statele Unite ale Americii 96, 7047–7052 (1999).
Baffi, C. W. și colab. Sindromul metabolic și plămânul. Cufăr 149, 1525–1534, https://doi.org/10.1016/j.chest.2015.12.034 (2016).
Carpaij, O. A. și van den Berge, M. Relația astm-obezitate: mecanisme subiacente și implicații de tratament. Opinia actuală în medicina pulmonară 24, 42–49, https://doi.org/10.1097/mcp.0000000000000446 (2018).
Hew, M. și colab. Insensibilitate relativă la corticosteroizi a celulelor mononucleare din sângele periferic în astmul sever. Revista americana de medicina respiratorie si de ingrijire critica 174, 134–141, https://doi.org/10.1164/rccm.200512-1930OC (2006).
Kim, R. Y. și colab. Rolul Răspunsurilor dependente de IL-1beta mediate de NLRP3 în astmul sever, rezistent la steroizi. Revista americana de medicina respiratorie si de ingrijire critica 196, 283–297, https://doi.org/10.1164/rccm.201609-1830OC (2017).
Mulțumiri
NNH și VYP sunt susținute de acordul NIEHS P50 ES018176 și acordurile EPA 83615201 și 83451001. VYP este, de asemenea, susținut de granturile NHLBI R01 HL128970, HL133100 și HL138932. Această publicație nu a fost revizuită oficial de EPA. Opiniile exprimate în acest document sunt doar cele ale lui Fricke și ale colegilor și nu reflectă neapărat cele ale Agenției. EPA nu aprobă produsele sau serviciile comerciale menționate în această publicație.
Informatia autorului
Kathrin Fricke, Marcela Vieira și Haris Younas au contribuit în mod egal la această lucrare.
Afilieri
Divizia de Medicină Pulmonară și de Critică, Departamentul de Medicină, Școala de Medicină a Universității Johns Hopkins, Baltimore, MD, SUA
Kathrin Fricke, Marcela Vieira, Haris Younas, Mi-Kyung Shin, Shannon Bevans-Fonti, Slava Berger, Rachel Lee, Franco R. D'Alessio, Qiong Zhong, Nadia N. Hansel și Vsevolod Y. Polotsky
Departamentul de Sănătate și Inginerie a Mediului, Școala de Sănătate Publică Johns Hopkins Bloomberg, Baltimore, MD, SUA
Andrew Nelson, Jeff Loube, Ian Sanchez și Wayne Mitzner
Divizia de Medicină Pulmonară, Departamentul de Medicină Internă, Facultatea de Medicină din Hanovra, Hanovra, Germania
Puteți căuta acest autor și în PubMed Google Scholar
- Dieta cu conținut ridicat de grăsimi saturate și carbohidrați scade durata de viață independent de greutatea corporală la șoareci
- Dieta bogată în grăsimi induce formarea liposarcomului spontan în țesutul adipos de șoarece cu
- Mecanismele afectării funcției celulelor β pancreatice la șoarecii obezi induși în dietă bogată în grăsimi
- Dieta bogată în grăsimi modulează conținutul de proteine al transportorilor de nutrienți din intestinul subțire al șoarecilor
- Îmbunătățirea polarizării macrofagelor adipoase la șoarecii knock-out GHSR obezi induși în dietă bogată în grăsimi