Annie George
1 Biotropics Malaysia Berhad, Lot 21 Jalan U1/19, Section U1, Hicom-Glenmarie Industrial Park, 40150 Shah Alam, Selangor, Malaysia
Sasikala Chinnappan
1 Biotropics Malaysia Berhad, Lot 21 Jalan U1/19, Section U1, Hicom-Glenmarie Industrial Park, 40150 Shah Alam, Selangor, Malaysia
Yogendra Choudhary
2 Laboratoare Ethix Pharma, Karbala Road, Bilaspur 495001, Chhattisgarh, India
Vandana Kotak Choudhary
2 Laboratoare Ethix Pharma, Karbala Road, Bilaspur 495001, Chhattisgarh, India
Praveen Bommu
2 Laboratoare Ethix Pharma, Karbala Road, Bilaspur 495001, Chhattisgarh, India
Hoi Jin Wong
1 Biotropics Malaysia Berhad, Lot 21 Jalan U1/19, Section U1, Hicom-Glenmarie Industrial Park, 40150 Shah Alam, Selangor, Malaysia
Abstract
tabelul 1
Parametrii testului de legare a receptorului de adenozină A2A.
| Sursă | Celule HEK-293 recombinate umane |
| Ligand | 0,05 μM [3] CGS-21680 |
| Vehicul | 1% DMSO |
| Timp/temp. De incubație. | 90 minute la 25 ° C |
| Tampon de incubare | 50 mM Tris-HCI, pH 7,4, 10 mM MgCl 2, 1 mM EDTA, 2 U/mL adenozin Deaminază |
| Ligand nespecific | 50 μM NECA (5-N-etilcarboxamidă adenozină) |
| KD | 0,064 μM |
| B max | 19 pmol/mg proteină |
| Legare specifică | 85% |
| Metoda de cuantificare | Legarea radioligandului |
| Criterii de semnificație | ≥50% din stimularea maximă |
| Referințe | CGS-21680 |
masa 2
Parametrii de testare funcționali ai receptorului adenosinei A2A.
| Sursă | Celule HEK-293 recombinate umane |
| Control | 0,1 uM NECA |
| Vehicul | 0,40% DMSO |
| Timp/temp. De incubație. | 10 minute la 37 ° C |
| Tampon de incubare | Soluție de sare echilibrată Hank (HBSS) modificată pH 7,4 |
| Metoda de cuantificare | Cuantificarea HTRF a acumulării AMPc |
| Criterii semnificative pentru agonist | Creșterea ≥50% a AMPc în raport cu răspunsul NECA |
| Criterii semnificative pentru antagonist | Inhibarea ≥50% a creșterii AMPc indusă de NECA |
Tabelul 3
Parametrul testului funcțional al receptorului de adenozină A1.
| Sursă | Wistar rat vas deferens |
| Control | 0,3 μM CHA (N6-ciclohexiladenozină) |
| Vehicul | 0,10% DMSO |
| Timp/temp. De incubație. | 5 minute la 32 ° C |
| Tampon de incubare | KREBS pH 7,4 |
| Metoda de cuantificare | Izometric (modificări gram) |
| Criterii semnificative pentru agonist | Reducerea ≥50% a zvâcnirii neurogene față de 0,3 μM răspuns CHA |
| Criterii semnificative pentru antagonist | Inhibare ≥50% a relaxării induse de CHA 0,3 μM |
2.3. Animale
Nouăzeci de șobolani SD bărbați adulți (în vârstă de 3 luni, 200-250 g) și șobolani masculi juvenili din aceeași tulpină (în vârstă de 35-40 de zile, 75-100 g) de la Institutul Național de Nutriție, Tarnaka, Hyderabad, au fost utilizate așa cum este descris în Tabelul 4. Dieta cuprindea dieta standard cu pelete de la Provimi (rozătoarele Nutrilab). Șobolanii juvenili au fost ținuți în grupuri de câte zece pe cușcă și au servit drept stimul social pentru șobolanii adulți. Animalele au fost menținute într-o cameră sub temperatură controlată (22 ± 2 ° C), cu umiditate relativă cuprinsă între 50 și 70% și au fost supuse unui ciclu de lumină de 12 ore (luminile aprinse la 8:00 am) cu acces gratuit la alimente și apă. Toate procedurile experimentale (numărul de aprobare IAEC/CPCSEA 1412/a/11 în februarie 2012) au fost efectuate în conformitate cu liniile directoare privind îngrijirea animalelor din Principiile OCDE de bune practici de laborator, revizuite în 1997 și adoptate la 26 noiembrie 1997, de către decizia Consiliului OECD [C (97) 186/Final].
Tabelul 4
Gruparea animalelor în funcție de materialele testate, doză și cale de administrare.
| 1 | Controlul vehiculului | p.o. | 10 |
| 2 | BT 00119 (200 mg/kg) | p.o. | 10 |
| 3 | BT 00119 (300 mg/kg) | p.o. | 10 |
| 4 | BT 00119 (600 mg/kg) | p.o. | 10 |
| 5 | PME 00012 (200 mg/kg) | p.o. | 10 |
| 6 | GBE 000120 (120 mg/kg) | p.o. | 10 |
| 7 | Donepezil (3 mg/kg) | i.p. | 10 |
| 8 | BT 00119 (60 mg/kg) | i.p. | 10 |
| 9 | BT 00119 (120 mg/kg) | i.p. | 10 |
2.4. Tratament
Extractul vegetal de O. stamineus (doze 60, 120, 200, 300 și 600 mg/kg greutate corporală), un extract comercial de G. biloba (120 mg/kg, standardizat la 27,25% flavonglicozide Ginkgo, 6% lactone terpenice, și ≤ 5 ppm acid ginkgolic determinat prin metode HPLC), extract de apă de P. minus (200 mg/kg) și medicamentul donepezil (comprimat ARICEPT, Zydus Cadila Ltd., 3 mg/kg) au fost dizolvate în apă distilată. Soluția de control a constat din apă distilată (vehicul). Extractul de O. stamineus a fost testat i.p. și oral. Extractele de O. stamineus în doze de 60 și 120 mg/kg b.w. și donepezil la 3 mg/kg b.w. au fost administrate i.p. pentru o comparație directă cu activitatea donepezilului, cu 120 de minute înainte de a doua întâlnire C2. În plus, extracte de O. stamineus la doze de 200, 300 și 600 mg/kg greutate corporală, extract de G. biloba la o doză de 120 mg/kg, o concentrație derivată din studiile anterioare de G. biloba efectuate pe animale în investigațiile [32] și 200 mg/kg extract de apă din P. minus (ca o comparație directă cu doza mai mică a extractului testat) și vehicul au fost administrate pe cale orală, cu 120 de minute înainte de a doua întâlnire C2.
2.5. Test de recunoaștere socială
Toate valorile sunt exprimate ca medii ± SEM (n este egal cu numărul șobolanilor incluși în fiecare analiză). RI (RI = C2/C1) a fost calculat pentru testul de recunoaștere socială. Datele au fost analizate prin compararea controlului versus tratament și standard și a modificărilor de activitate înainte și după tratament (C1 versus C2) și RI versus control, standard și tratament utilizând testul t Student de software Graph Pad Prism 4.0.
3. Rezultatul
3.1. Caracterizarea extractului etanolic O. stamineus
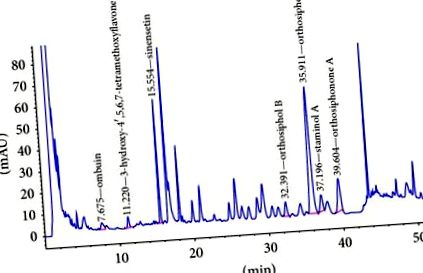
Profilul cromatografic al compoziției extractului etanolic O. stamineus și a compușilor de referință sunt așa cum se arată în figurile din figurile 1 1 și respectiv 2, 2. Vârfurile corespunzătoare celor șapte compuși selectați au fost identificate pe baza timpului de retenție față de standardele de referință și a spectrului UV. Vârfurile ombuinei (3,3 ′, 5-trihidroxi-4 ′, 7-dimetoxiflavonei) (0,14%), 3′-hidroxi-4 ′, 5,6,7-tetrametoxiflavonei (0,10%), sinensetin (0,07%) ), ortosifolul B (0,26%), ortosifolul A (0,67%), staminolul A (0,45%) și ortosifonona A (0,12%) sunt eluate la timpi de reținere 7,675 min, 11,220 min, 15,554 min, 32,391 min, 35,911 min, 37,196 min, respectiv 39,604 min. Extractul standardizat rezultat se bazează pe grupul de compuși markeri.
Cromatograme HPLC de extract etanolic de frunze de O. stamineus.
- Supliment de extract de semințe de struguri Fapte, dozare, utilizări și efecte secundare
- Extract de guarana Beneficii pentru sănătate, efecte secundare și consum
- Efectele extractului de cohosh negru asupra creșterii în greutate corporală, acumulării de grăsime intraabdominală, plasmă
- Extract de schinduf Beneficii pentru sănătate, studii de caz, dozare și efecte secundare
- Utilizări clinice ale extractului de frunze de anghinare American Journal of Health-System Pharmacy Oxford Academic