Luis Rodrigo
1 Unitate de gastroenterologie, Spitalul Universitar Central din Asturia (HUCA), Avda. de Roma s/n, 33011 Oviedo, Asturias, Spania; moc.liamg@hzeravlaairun
Valia Beteta-Gorriti
2 Unitatea de dermatologie, Spitalul Universitar Central din Asturia (HUCA), Avda. de Roma s/n, 33011 Oviedo, Asturias, Spania; moc.liamtoh@gb_atilav (V.B.-G.); moc.liamtoh@88_zemogailec (C.G.d.C.); moc.liamg@levidedla (A.d.D.); moc.liamtoh@soicalapaniruall (L.P.)
Nuria Alvarez
1 Unitatea de gastroenterologie, Spitalul Universitar Central din Asturia (HUCA), Avda. de Roma s/n, 33011 Oviedo, Asturias, Spania; moc.liamg@hzeravlaairun
Celia Gómez de Castro
2 Unitatea de dermatologie, Spitalul Universitar Central din Asturia (HUCA), Avda. de Roma s/n, 33011 Oviedo, Asturias, Spania; moc.liamtoh@gb_atilav (V.B.-G.); moc.liamtoh@88_zemogailec (C.G.d.C.); moc.liamg@levidedla (A.d.D.); moc.liamtoh@soicalapaniruall (L.P.)
Alvaro de Dios
2 Unitatea de dermatologie, Spitalul Universitar Central din Asturia (HUCA), Avda. de Roma s/n, 33011 Oviedo, Asturias, Spania; moc.liamtoh@gb_atilav (V.B.-G.); moc.liamtoh@88_zemogailec (C.G.d.C.); moc.liamg@levidedla (A.d.D.); moc.liamtoh@soicalapaniruall (L.P.)
Laura Palacios
2 Unitatea de dermatologie, Spitalul Universitar Central din Asturia (HUCA), Avda. de Roma s/n, 33011 Oviedo, Asturias, Spania; moc.liamtoh@gb_atilav (V.B.-G.); moc.liamtoh@88_zemogailec (C.G.d.C.); moc.liamg@levidedla (A.d.D.); moc.liamtoh@soicalapaniruall (L.P.)
Jorge Santos-Juanes
2 Unitatea de dermatologie, Spitalul Universitar Central din Asturia (HUCA), Avda. de Roma s/n, 33011 Oviedo, Asturias, Spania; moc.liamtoh@gb_atilav (V.B.-G.); moc.liamtoh@88_zemogailec (C.G.d.C.); moc.liamg@levidedla (A.d.D.); moc.liamtoh@soicalapaniruall (L.P.)
3 Facultatea de Medicină, Universitatea din Oviedo, 33003 Oviedo, Asturias, Spania
Abstract
Boala celiacă (CD) este o enteropatie mediată de imunitate, indusă de gluten, care afectează indivizii predispuși de toate vârstele. Mulți pacienți cu CD nu raportează simptome gastro-intestinale, ceea ce face dificilă obținerea unui diagnostic precoce. Pe de altă parte, CD este legat de un spectru larg de manifestări extraintestinale, dermatita herpetiformă (DH) fiind cea mai bine caracterizată. Aceste condiții asociate pot reprezenta indiciul pentru a ajunge la diagnosticul de CD. În ultimii ani, au existat mai multe rapoarte de asociere între CD și mai multe manifestări cutanate care se pot îmbunătăți cu o dietă fără gluten (GFD). Prezența unora dintre aceste boli ale pielii, chiar și în absența simptomelor gastrointestinale, ar trebui să dea naștere unei metode adecvate de screening pentru CD. Scopul acestei lucrări este de a descrie diferitele manifestări cutanate care au fost asociate cu CD și posibilele mecanisme implicate.
1. Introducere
Boala celiacă (CD) este o boală sistemică autoimună cronică asociată cu o enteropatie declanșată de aportul de gluten care afectează indivizii predispuși genetic de ambele sexe și se poate dezvolta la orice vârstă. Glutenul și principalele sale fracțiuni proteice, gliadina și glutenina, sunt prezente în grâu, secară, orz, ovăz, specii și hibrizi înrudite și alimente procesate [1]. Aproape toți pacienții cu CD prezintă antigenul leucocitar uman (HLA) DQ2 (> 90%) sau HLA DQ8 (5-10%); cu toate acestea, până la 40% dintre oamenii din America, Europa și Asia de Sud-Est poartă, de asemenea, aceste alele, indicând faptul că aceste gene sunt necesare, dar nu suficiente pentru dezvoltarea CD [2]. Descoperirile modificărilor inflamatorii în biopsiile intestinale, variind de la enterita limfocitară la diferite grade de atrofie viloasă, reprezintă standardul de aur pentru diagnosticarea CD, chiar și în prezența unei serologii negative pentru CD. Transglutaminazele anti-țesut IgA sunt anticorpii cei mai sensibili și mai rentabili pentru diagnosticul CD, deși anticorpii IgG peptidici gliadinici deamidați pot fi utili la pacienții seronegativi cu deficit de IgA înnăscut. O dietă fără gluten pe tot parcursul vieții (GFD) este obligatorie, realizând recuperarea clinică și histologică la majoritatea pacienților [1].
În ultimele decenii, CD a fost considerată a fi o boală mai puțin frecventă care afectează în principal copii și limitată la persoanele cu ascendență europeană. În prezent, știm că această tulburare poate fi detectată la orice vârstă și este considerată una dintre cele mai frecvente boli cronice întâlnite la nivel mondial, cu o prevalență de aproximativ 1-2% [3]. Vârsta medie a diagnosticului de CD pentru adulți este de 45 de ani, deși până la 20% dintre pacienți sunt diagnosticați la vârsta de 60 de ani sau peste. CD este probabil o entitate subdiagnosticată la vârsta adultă, în parte, deoarece mulți pacienți din această grupă de vârstă nu au simptomele clasice, cum ar fi diareea sau semnele de malabsorbție. De fapt, la majoritatea pacienților adulți, simptomele gastro-intestinale sunt subtile sau chiar absente, iar suspiciunea clinică apare din manifestările extra-intestinale (CD non-clasic sau atipic), cum ar fi anemia, tulburările cutanate, bolile neurologice, osteoporoza și funcția hepatică anormală. teste [2,4]. Subliniem importanța luării în considerare a simptomelor netipice pentru diagnosticarea CD adult și căutarea activă a manifestărilor asociate extraintestinale pentru a începe o GFD precoce și a preveni apariția complicațiilor pe termen lung.
Pacienții cu CD sunt mai frecvent afectați de alte tulburări mediată imun (ID) comparativ cu populația generală, așa cum sa raportat în studiile anterioare, în principal boli tiroidiene și de piele și diabet zaharat de tip 1 [5,6]. Această observație poate fi explicată parțial printr-o posibilă răspândire a răspunsului imun adaptiv, declanșat inițial în tractul gastro-intestinal, către alte țesuturi [4,6]. Tiroidita Hashimoto este cel mai frecvent asociat ID, urmată de mai multe afecțiuni ale pielii, cum ar fi psoriazisul, dermatita atopică (AD), vitiligo, lupus eritematos sistemic (LES), alopecia areata (AA) și lichenul plan oral (OLP) [6] . Interesant este că 60% dintre pacienții cu CD cu boală tiroidiană asociată care dezvoltă un al treilea ID sunt legați de piele. Aceste date sugerează o relație între sistemele imunologice ale tiroidei, pielii și intestinului subțire, care par a fi mai susceptibile la dezvoltarea unor răspunsuri imunologice aberante împotriva auto-antigenelor. [6,7,8,9,10,11,12].
Manifestările cutanate asociate cu CD, altele decât dermatita herpetiformă (DH), sunt slab cunoscute. În prezent se recunoaște că DH este o manifestare extra-intestinală fără îndoială a CD. În plus, există dovezi în creștere care susțin legătura dintre CD și mai multe afecțiuni ale pielii. În 2006, Humbert și colab. a propus o clasificare a bolilor de piele asociate cu CD, împărțindu-le în patru categorii: autoimune, alergice, inflamatorii și diverse (Tabelul 1) [9,10,11,12,13,14,15,16,17,18,19 ]. Recent, Bonciolini și colab. au descris 17 pacienți afectați de sensibilitate la gluten non-celiac cu manifestări cutanate similare cu eczeme, psoriazis și DH care nu au prezentat un model histologic specific [20]. Singurele constatări frecvente la majoritatea acestor pacienți au fost mâncărime severă, prezența C3 la joncțiunea dermo-epidermică și rezoluția rapidă după adoptarea unui GFD. Autorii au subliniat importanța unei colaborări strânse între gastroenterologi și dermatologi, datorită asocierilor multiple dintre tulburările gastrointestinale și ale pielii. În lucrarea de față, ne propunem să descriem tulburările multiple ale pielii asociate cu CD și posibilele mecanisme implicate.
tabelul 1
Puterea dovezilor pentru asocierea dintre boala celiacă și bolile pielii.
| Alergic | Urticaria Urticarie cronică Dermatita atopica | HR: 1,51 (CI = 1,36-1,68) [12] HR: 1,92 (CI = 1,48-2,48) [12] SAU: 3,17 (CI = 1,02-9,82) [13] | Prurigo nodularis |
| Inflamator | Pitiriazis rubra pilaris Eritroderma Eritemul elevatum diutinum Eritem migrator necrolitic Pitenoza lichenoide Eritem nodos | ||
| Mediat imun | Psoriazis | HR: 1,72 (CI = 1,54-1,92) [14] SAU: 1,44 (CI = 1,40-1,92) [15] SAU: 3,09 (CI = 1,92-4,97) [16] IgA anti-gliadină: SAU: 2,36 (CI = 1,15-4,83) [17] | |
| Autoimun | Alopecia areata Vasculită cutanată Ig A dermatoză liniară Dermatomiozita Vitiligo Lupus eritematos Lichen sclerosus | ||
| Diverse | Stomatita aftoasă Rozacee | SAU: 3,79 (CI = 2,67-5,39) [18] HR: 1,46 (CI = 1,11-1,93) [19] | Amiloidoză cutanată Eritem inelar Lipodistrofie parțială Cutis laxa generalizată dobândită Ictioza Leuconichie transversă Porfiria Hipertricoza lanuginosa |
GFD: dietă fără gluten; CD: boala celiaca; HR: raportul de pericol; SAU: raport de cote; CI: interval de încredere de 95%; IgA: imunoglobulină A.
2. Imunopatogenia leziunilor cutanate și orale asociate cu CD
Răspunsurile imune în CD sunt foarte largi. O explicație probabilă constă în prezența unei creșteri a permeabilității intestinale la ambele grupuri de pacienți, în raport cu efectul toxic direct al gliadinei pe suprafața epiteliului intestinal [21,22]. Acest lucru permite trecerea peptidelor de gluten și a altor peptide înrudite în sânge, provocând apariția diferitelor procese inflamatorii sau autoimune care pot afecta orice organ sau țesut, care poate fi rezultatul răspunsurilor imune aberante [21,23,24]. După cum a afirmat Hadjivassiliou în urmă cu mai bine de 15 ani, „faptul că sensibilitatea la gluten este considerată în principal ca o boală a intestinului subțire este o concepție greșită istorică”. [22.25].
În submucoasa intestinului subțire, începând cu acțiunea transglutaminazei tisulare tip 2 care desfășoară glutenul, apare o cascadă de evenimente, provocând un răspuns Th1 care stimulează limfocitele B care eliberează IgE și alte imunoglobuline [26] care joacă un rol important în apariția urticariei și a AD și o stimulare a Th2 mediată de limfocitele T care produce eliberarea de citokine pro-inflamatorii, precum TNF-α și interferon gamma (IFNγ), printre altele [27], și care joacă roluri importante în mai multe tipuri de dermatită mediată imun, cum ar fi psoriazisul. În plus, aceste răspunsuri imunologice pot provoca, de asemenea, producerea de imunocomplexe circulante datorită interacțiunilor antigen-anticorp care predomină în leziunile vasculitice.
3. Dermatita Herpetiformă
4. Urticaria
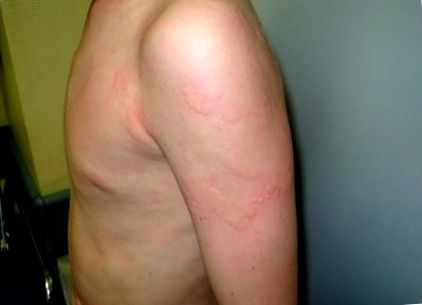
Urticaria se caracterizează prin apariția wheals, angioedem sau ambele (Figura 1) [29]. Urticaria este o tulburare frecventă, care apare la 15-25% dintre indivizi la un moment dat în viață [29,30]. Urticaria cronică (CU) (durata ≥ 6 săptămâni) se observă la aproximativ 0,5-1% din populația generală [31,32]. CU este asociată cu o scădere substanțială a calității vieții [31]. Se consideră că etiopatogeneza CU este asociată cu mecanisme autoimune [33,34,35,36]. CU s-a dovedit a avea o asociere genetică cu antigenul leucocitar uman alele HLA-DQ8 [37]. Interesant este că HLADQ8 are o asociere cu CD [37,38].
Urticaria. Umflături tranzitorii palide până la roșii, bine delimitate, care implică dermul, în principal la nivelul toracelui și brațului stâng.
În 1987, Hauteke și colab. a descris mai întâi asocierea dintre CD și urticaria cronică [39], deși relația dintre aceste două boli nu este pe deplin clară. Recent, Kolkhir și colab. a declarat că urticaria cronică spontană este puternic asociată cu diferite boli autoimune, inclusiv tiroidita Hashimoto, anemia pernicioasă, vitiligo, diabetul zaharat de tip 1, boala Grave, artrita reumatoidă și CD [40]. Într-un studiu cu populație amplă, 453 de pacienți cu DC și fără diagnostic anterior de urticarie au dezvoltat urticarie, iar 79 dintre acești 453 de pacienți au avut urticarie cronică [12]. Raporturile de pericol corespunzătoare au fost 1,51 pentru orice urticarie (95% CI = 1,36-1,68) și 1,92 pentru urticaria cronică (95% CI = 1,48-2,48). Aceste date susțin o prevalență crescută a urticariei și a urticariei cronice la pacienții cu CD [12].
În unele cazuri de CU, adoptarea GFD și-a dovedit eficacitatea în controlul erupțiilor cutanate [41,42], susținând în continuare că CU poate fi o manifestare cutanată a CD și nu doar o asociere fortuită [11].
5. Dermatita atopică
Dermatita atopica. Papule și plăci biliare eritematoase bilaterale excoriate pe suprafața cotului flexor drept.
AD a fost, de asemenea, legat de CD. Ress și colab. a analizat prevalența CD la 351 copii cu AD comparativ cu o populație generală de copii și a prezentat un risc de patru ori mai mare de a dezvolta CD la pacienții cu AD (OR, 4,18; IC 95%, 1,12-15,64) [60]. Acest studiu subliniază, de asemenea, necesitatea evaluării rentabilității screening-ului pacienților cu AD pentru CD în timp, pentru a preveni complicațiile pe termen lung. Mai mult, Ciacci și colab. a efectuat un studiu de control al cazului care a implicat 4114 pacienți adulți, cu sau fără CD și a observat că AD a fost de trei ori mai frecventă la pacienții cu CD și de două ori mai frecventă la rudele lor decât la soții lor (OR, 3,17; IC 95%, 1,02-9,82) [13].
6. Psoriazis
Psoriazisul este o boală inflamatorie cronică autoimună a pielii, cu o prevalență estimată de 2-4% la populația adultă [61,62]. Afectează peste 7,5 milioane de oameni din Statele Unite și aproximativ 125 de milioane de oameni din întreaga lume [54]. Psoriazisul este considerat a fi o boală multifactorială, în care fundalul genetic interacționează cu factorii de mediu pentru a defini riscul unui individ [62,63,64]. Manifestările clinice clasice ale psoriazisului constau în prezența plăcilor roșii, infiltrate, acoperite cu o scalare grosieră, argintie (Figura 3 și Figura 4). Siturile de predilecție includ coatele și genunchii, scalpul și regiunile periumbilicale și lombare, deși orice sit anatomic ar putea fi afectat [65]. Cursul clinic al psoriazisului este marcat de recidive frecvente cu rate fluctuante [62].
Placă extinsă de psoriazis la partea extensorului cotului stâng.
Psoriazis. Plăci bine delimitate, eritematoase, solzoase, care sunt relativ simetrice pe spate.
Deși datele disponibile cu privire la coexistența CD și psoriazisului sunt încă neconcludente, există o cantitate considerabilă de dovezi care sugerează că pacienții psoriazici cu CD concomitent pot beneficia de o GFD [17,21,80,89]. Mai mult, prevalența anticorpului anti-gliadină IgA este semnificativ mai mare la pacienții cu psoriazis fără diagnostic de tulburări legate de gluten. Din acest motiv, testarea anti-gliadină IgA poate identifica pacienții care ar putea beneficia de GFD [90].
Pentru a rezuma, coexistența relativ frecventă a CD și psoriazisului justifică monitorizarea pacienților cu oricare dintre afecțiuni pentru evidența clinică a celeilalte. Acest lucru este deosebit de important în cazul psoriazisului, deoarece ar putea fi singura manifestare a unui CD nediagnosticat, chiar și în absența simptomelor digestive evidente. Este recomandabil să efectuați întregul protocol pentru a căuta în mod activ CD, inclusiv biopsiile duodenale, chiar și atunci când markerii serologici sunt negativi. În cazul descoperirilor CD negative, efectuarea unui studiu cu GFD este în prezent metoda de diagnostic recunoscută [23].
7. Stomatita aftoasă
Numeroși autori au descris o mare varietate de tulburări ale cavității bucale la pacienții cu DC și unele dintre aceste manifestări pot fi considerate indicii de diagnostic în formele tăcute și atipice ale CD [91].
Stomatita aftoasă recurentă (RAS) este o afecțiune clinică obișnuită care produce ulcerații dureroase în cavitatea bucală. RAS se caracterizează prin ulcere recurente multiple, mici, rotunde sau ovoidale, cu margini circumscrise, nimburi eritematoase și podele galbene sau gri, care se prezintă de obicei în copilărie sau adolescență [92,93] (Figura 5). RAS a fost recunoscut de mulți ani ca un simptom al CD (CD) [93,94,95,96]. O meta-analiză recentă a arătat că pacienții celiaci au o frecvență mai mare a RAS (OR = 3,79, 95% CI = 2,67-5,39). Când au fost luați în considerare numai copiii, OR a fost de 4,31 (95% CI = 3,03-6,13), în timp ce la adulți, OR a unui singur studiu a fost de 47,90 (95% CI 6,29-364,57) [18]. Pacienții cu RAS ar trebui considerați subiecți cu risc, chiar și în absența oricăror simptome gastro-intestinale și, prin urmare, ar trebui să fie supuși unei proceduri de diagnostic pentru CD [97]. RAS poate fi prezent și la pacienții cu DH [98]. Un studiu a raportat ulcere mucoase nespecifice la până la 40% dintre pacienții cu DH [99]. Etiopatologia RAS este obscură; nu se știe dacă leziunile RAS sunt influențate direct de tulburarea de sensibilitate la gluten sau dacă acestea sunt legate de deficiența hematinică cu niveluri scăzute de fier seric, acid folic și vitamina B12 sau deficiențe de oligoelemente datorate malabsorbției la pacienții cu CD netratată [ 96].
- Dieta asociată cu inflamația și boala Alzheimer
- Dieta și psoriazisul, partea II boala celiacă și rolul unei diete fără gluten - PubMed
- Urmând o varietate de modele de alimentație sănătoasă asociate cu un risc mai mic de boli de inimă -
- Dieta fără gluten în timpul sarcinii ameliorează semnele de diabet și boală celiacă la șoarece NOD
- Intoleranță la gluten sau boală celiacă Sănătate digestivă Bon Secours