James E Foley
1 Cercetare și dezvoltare clinică, Novartis Pharmaceutical Corporation, East Hanover, New Jersey, SUA;
Jens Jordan
2 Institutul de farmacologie clinică, Facultatea de Medicină din Hanovra, Hanovra, Germania
Abstract
Introducere
Excesul de greutate și/sau obezitatea contribuie la riscul apariției diabetului de tip 2 și confundă controlul glicemic odată ce boala se dezvoltă.1 Se recomandă intervenții vizând pierderea în greutate pentru aproximativ 80% -90% dintre pacienții cu diabet de tip 2 a căror greutate depășește normalul. .2-4 La astfel de pacienți, pierderea în greutate reușită poate îmbunătăți controlul glicemic, precum și reduce factorii de risc cardiovascular concomitent, de exemplu, hipertensiune și dislipidemie.1 Prin urmare, medicii trebuie să acorde o atenție deosebită efectelor terapiilor cu diabet asupra greutății corporale și adipozității.
În termeni generali, efectele potențiale ale diferitelor clase de medicamente antidiabetice asupra echilibrului ponderal sunt bine recunoscute. Atât insulina cât și secretagogii de insulină (sulfoniluree și glinide) promovează creșterea în greutate, în special în regimurile menite să realizeze un control glicemic intens. Tiazolidindionele (TZD) sunt asociate cu creșterea în greutate, în timp ce metformina este în general asociată cu neutralitatea în greutate sau cu scăderea în greutate. Terapiile bazate pe incretină, incluzând agoniști ai receptorului peptidei de tip glucagon (GLP) -1 și inhibitorilor dipeptidil peptidazei (DPP) -4, sunt asociați cu scăderea în greutate sau neutralitatea în greutate.1
O apreciere mai detaliată a modului în care medicamentele pentru diabet pot afecta greutatea pacientului și implicațiile unor astfel de interacțiuni asupra factorilor-cheie, inclusiv sensibilitatea la insulină, necesită luarea în considerare a diferiților factori de confuzie. Acești factori includ mecanisme compensatorii care intră în joc la extreme glicemice (irosirea caloriilor în hiperglicemie și consumul defensiv la cuspida hipoglicemiei), precum și efectele tratamentelor specifice asupra metabolismului lipidelor. Acest articol examinează rolul acestor factori și al altor factori, cu un accent special pe neutralitatea în greutate a inhibitorului DPP-4 vildagliptin.
Greutatea corporală și controlul glicemic
Obezitatea contribuie la riscul de diabet de tip 2 al unei persoane, în mare parte prin contribuția sa la rezistența la insulină.5 Celulele grase mari rezistă la supresia lipolizei mediată de insulină, rezultând eliberarea în exces a acidului gras liber (FFA). FFA promovează în continuare rezistența la insulină, în special la nivelul mușchilor scheletici și la nivelul ficatului. Celulele musculare necesită mai multă insulină decât în mod normal pentru a elimina excesul de glucoză din sânge, în timp ce în ficat nivelurile normale de insulină nu reușesc să suprime în mod adecvat eliberarea glucozei în sânge.4,6,7 Pentru a compensa rezistența la insulină, celulele β pancreatice produce insulină suplimentară, rezultând niveluri ridicate de insulină din sânge. Diabetul Frank apare atunci când celulele β nu reușesc să compenseze pe deplin rezistența la insulină
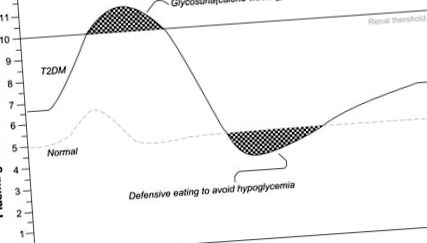
Diabetul necontrolat suficient de sever pentru a produce simptomele clasice ale setei excesive, foametei și urinării implică de obicei pierderea în greutate în ciuda aportului ridicat de calorii, deoarece țesuturile dependente de insulină „mor de foame în mijlocul abundenței”, iar rinichii răspund la hiperglicemie severă prin eliminarea excesului de glucoză în urină. Chiar și în absența unei boli simptomatice, rinichii vor elimina glucoza și vor pierde astfel calorii, atunci când nivelurile de glucoză din sânge depășesc pragul de glucoză renală, de obicei în jur de 180 mg/dL (10 mmol/L, Figura 1), deși această valoare variază substanțial la indivizi.8,9 O persoană ale cărei niveluri glicemice depășesc frecvent pragul renal se pot angaja într-o supraalimentare compensatorie pentru a recupera caloriile pierdute în urină. La un astfel de pacient, inițierea sau intensificarea controlului glicemic cu un agent care crește disponibilitatea insulinei sau mărește acțiunea insulinei poate duce la creșterea în greutate, deoarece glucoza care altfel ar fi fost excretată este acum preluată de țesuturile corpului. Reducerea glicozuriei prin îmbunătățirea controlului glicemic ar putea produce astfel creșterea în greutate.
Consumul de calorii și alimentația defensivă sunt posibilele rezultate ale nivelurilor fluctuante de glucoză plasmatică în diabetul de tip 2, confundând gestionarea greutății.
Abreviere: T2DM, diabet de tip 2.
La celălalt capăt al spectrului glicemic (vezi Figura 1), agenții capabili să declanșeze episoade hipoglicemice pot promova, de asemenea, creșterea în greutate, mai ales ca parte a unui regim intensificat care vizează atingerea nivelurilor glicemice normale sau aproape normale. Fenomenul a fost inițial demonstrat la pacienții cu diabet zaharat de tip 1 în cadrul controlului diabetului și al complicațiilor, unde la cinci ani, pacienții randomizați la terapia intensivă cu insulină au obținut o medie cu 4,6 kg mai mult decât cei care au primit terapie convențională. grupul a prezentat, de asemenea, episoade hipoglicemiante semnificativ mai multe și mai severe. Pacienții cu diabet zaharat de tip 2 care participă la studiul privind diabetul prospectiv din Regatul Unit au fost randomizați la terapie intensivă cu sulfoniluree sau insulină sau la terapie „convențională” mai puțin agresivă. Pacienții din grupul de terapie intensivă au experimentat mai multe episoade de hipoglicemie și s-au îngrășat mai mult, în special cei care au luat insulină.11 Creșterea în greutate poate fi legată parțial de o creștere a „alimentației defensive” pentru a preveni o scădere de la normoglicemie la hipoglicemie.
Efecte specifice agentului și clasei
Terapiile medicamentoase pot influența, de asemenea, echilibrul ponderal în virtutea efectelor lor asupra depozitării grăsimilor. Insulina inhibă puternic lipoliza la adipocite, promovând astfel stocarea intracelulară a trigliceridelor.4 Într-un studiu comparativ al terapiei cu insulină și sulfoniluree la pacienții cu diabet de tip 2, Birkeland și colab. Au demonstrat o creștere semnificativă a masei corporale la pacienții tratați cu insulină, dintre care doar 30% era atribuibilă masei corporale slabe.12
Două clase de agenți de diabet de tip 2, agoniștii receptorilor GLP-1 și inhibitori DPP-4, reduc hiperglicemia prin imitarea sau intensificarea acțiunilor incretinei. Incretinele sunt hormoni eliberați din intestin ca răspuns la aportul de alimente care cresc sensibilitatea la glucoză a celulelor β- și α pancreatice.18 Cele două incretine principale, GLP-1 și polipeptida insulinotropă gluco-dependentă (GIP), sunt responsabile de amplificare de secreție de insulină care apare după o sarcină de glucoză orală, spre deosebire de o sarcină intravenoasă echivalentă, adică efectul incretin. Farmacoterapia pe bază de incretină îmbunătățește controlul glicemic la pacienții cu diabet zaharat de tip 2, la care răspunsul la incretină este frecvent afectat.19,20
Hormonii incretinici stimulează secreția de insulină de către celulele β numai în contextul creșterii glucozei, adică într-o manieră dependentă de glucoză.20 Studii timpurii ale potențialului terapiei pe bază de incretină, care implică perfuzii directe de GLP-1 atât în normal cât și în tip 2 indivizi diabetici au confirmat un astfel de efect autolimitat de scădere a glucozei.21,22 Ca urmare, spre deosebire de secretagogii de insulină fără discriminare, cum ar fi sulfoniluree și glinide, terapiile pe bază de incretină sunt asociate cu un risc de hipoglicemie destul de scăzut și, prin urmare, sunt mai puțin probabil pentru a promova creșterea în greutate legată de alimentația defensivă.
Mimeticul injectabil GLP-1 injectabil de două ori pe zi, exenatidă, prezintă un risc minim de hipoglicemie atunci când este administrat ca monoterapie.20,23 Studiile de perfuzie timpurie cu GLP-1 au arătat, de asemenea, că la doze mari, hormonul crește sațietatea subiectivă și întârzie golirea gastrică.24 Aceste caracteristici sunt, de asemenea, observate cu terapiile cu exenatidă și liraglutidă, care s-au demonstrat în mod constant că produc scăderea în greutate la pacienții cu diabet zaharat de tip 2. 23,25 În cele șase studii de fază III ale programului Efect și acțiune în diabet Liraglutidă (LEAD), s-a observat scăderea în greutate cu tratamentul cu liraglutidă în toate studiile și în LEAD-6, care a comparat în mod direct liraglutida și exenatida, s-a dovedit că pierderea în greutate este comparabilă pentru ambii agenți pe parcursul a 26 de săptămâni (−3,2 kg pentru liraglutidă, −2,9 kg pentru exenatidă) .26,27
Inhibitorii DPP-4 se leagă și inhibă enzima care clivează și inactivează GLP-1 și GIP. Inhibarea degradării acestor hormoni de scurtă durată le crește concentrația și le prelungește activitatea. Spre deosebire de agoniștii receptorilor GLP-1, inhibitorii DPP-4 îmbunătățesc acțiunea incretinelor endogene fiziologic, în momentul secreției lor.18
Vildagliptin
Inhibitorul DPP-4 studiat pe larg, vildagliptin, îmbunătățește sensibilitatea celulelor β și α la glucoză, rezultând un răspuns de insulină postprandial îmbunătățit și secreție de glucagon bont, precum și glicemie îmbunătățită în repaus alimentar. să fie asociat cu un risc scăzut de hipoglicemie într-o gamă largă de setări și regimuri, 30-39 și probabil cu un risc scăzut de alimentație defensivă legată de hipoglicemie.
Spre deosebire de exenatidă, vildagliptin nu imită GLP-1 perfuzat în ceea ce privește sațietatea subiectivă sau volumul gastric, 40 de efecte care au fost asociate cu o pierdere semnificativă în greutate. Neutralitatea generală a greutății a fost observată cu vildagliptin, 1,31,32,34,37-39,41, spre deosebire de creșterea în greutate observată la insulină și sulfoniluree.1,11
Neutralitatea globală a greutății observată cu vildagliptin pare a fi un efect de clasă, deoarece inhibitorii DPP-4, saxagliptin și sitagliptin, s-au dovedit, de asemenea, că îmbunătățesc controlul glicemic, atât ca monoterapie, cât și ca terapie suplimentară pentru alți agenți orali, fără schimbare semnificativă a greutății corporale în majoritatea studiilor clinice.42–50
Într-un studiu clinic randomizat cap la cap la pacienți cu valori glicemice inițiale relativ scăzute (media HbA1C 7,3%, glucoză plasmatică în repaus alimentar [FPG] 9,2 mmol/L [165 mg/dl]), pacienții care au controlat inadecvat metformina care au fost randomizați la vildagliptin 50 mg bid au fost stabili în greutate la 52 de săptămâni (-0,2 kg), ceea ce a fost foarte semnificativ în comparație cu creșterea în greutate observată în grupul comparativ care a primit glimepiridă ≤6 mg zilnic (diferență între grupuri -1,8 kg, Figura P 2). Această noțiune este în concordanță cu constatările la rozătoare, în care GLP-1 exogen a inhibat absorbția trigliceridelor intestinale și perfuzia GIP a promovat clearance-ul trigliceridelor chilomicronice. Posibilitatea ca vildagliptinul să inhibe extracția grăsimilor din intestin, deși într-un grad mai mic decât un inhibitor al lipazei, cum ar fi orlistat, constituie o cale provocatoare prin care își poate exprima profilul de greutate favorabil.53
Mecanisme care pot atenua creșterea în greutate cu vildagliptin în timpul meselor. După o masă bogată în grăsimi, s-a constatat că vildagliptina reduce nivelurile de chilomicron apo B-48, sugerând că poate inhiba absorbția trigliceridelor mediată de chilomicron din intestin. lipoliza în țesutul adipos și oxidarea acizilor grași în mușchiul scheletic, sugestivă a mobilizării lipidice mediată simpatic și a catabolismului în starea postabsorptivă.54
Abrevieri: FFA, acizi grași liberi; NU, norepinefrina; TG, trigliceride.
Într-un alt studiu al efectelor vildagliptinului asupra parametrilor metabolici postprandiali, Boschmann și colab. Au efectuat un studiu randomizat, dublu-orb, încrucișat la 20 de pacienți cu diabet zaharat de tip 2 randomizat la vildagliptin (100 mg pe zi) sau placebo. În ziua 7, după un post peste noapte, subiecții au fost echipați cu catetere venoase și sonde de microdializă în țesutul adipos subcutanat și mușchiul scheletic. Apoi, după o masă standardizată, mai mulți factori lipidici, endocrini, neuroendocrini și metaboliți au fost testați la intervale frecvente pe parcursul a patru ore.54
Vildagliptin a crescut concentrațiile de norepinefrină venoasă postprandială. În același timp, vildagliptina a crescut concentrațiile postprandiale de lactat și glicerol în țesutul adipos și a scăzut nivelul lactatului și piruvatului în mușchiul scheletic. Aceste constatări indică faptul că, spre deosebire de efectele anabolice pe care le-ați putea aștepta ca răspuns la secreția de insulină postprandială îmbunătățită cu incretină, vildagliptina promovează de fapt lipoliza în țesutul adipos în starea postprandială, coroborată cu oxidarea crescută a acidului gras în mușchiul scheletic. Anchetatorii postulează că principalul impuls pentru aceste efecte nu provine din căile endocrine, ci din stimularea simpatică, după cum sugerează nivelurile ridicate de noradrenalină. Aceste dovezi pentru mobilizarea și cheltuirea caloriilor de grăsime stocate concomitent cu influxul de calorii din dietă oferă o altă cale interesantă prin care vildagliptina poate promova un echilibru favorabil al greutății.54 Figura 2 oferă o descriere integrată a celor două căi tocmai descrise.
Studiile mecaniciste limitate cu alți inhibitori DPP-4 exclud o generalizare a constatărilor mecaniciste pentru vildagliptin la clasa inhibitorilor DPP-4 în ansamblu. De exemplu, nu este clar că dozarea o dată pe zi cu saxagliptin are același efect asupra nivelurilor de GLP-1 ca în cazul vildagliptin 50 mg bid și se știe că nivelurile crescute de GLP-1 observate la debutul meselor sunt menținută perioade mult mai lungi de timp cu vildagliptin decât sitagliptin.55
Greutate și rezistență la insulină
Datele studiilor clinice și experiența practică susțin un consens general larg cu privire la efectele potențiale în greutate ale diferitelor clase de medicamente pentru diabetul de tip 2 și ale agenților individuali. Mai mult, dacă un anumit regim susține o greutate la starea de echilibru „de dorit”, atinge neutralitatea în greutate sau chiar promovează o pierdere semnificativă în greutate, nu reflectă în sine starea anumitor procese de bază ale bolii, de exemplu, rezistența la insulină și disfuncția celulelor β.
De exemplu, în mai multe studii clinice cuprinse între 24 și 52 de săptămâni de urmărire, exenatida a fost asociată cu o scădere semnificativă în greutate ca monoterapie, 56 sau când a fost adăugată la metformină, 57,58 sulfoniluree, 59 sau terapie combinată metformină-sulfoniluree. aceste studii, IMC-ul mediu la momentul inițial a fost mai mare de 30, adică, punctul limită al Institutului Național al Pulmonului și Sângelui pentru „obezi”. Deși capacitatea pierderii în greutate de a ameliora rezistența la insulină este bine recunoscută, 1 singurul studiu care a evaluat sensibilitatea la insulină (prin clemă hiperglicemică) într-un cadru de pierdere în greutate asociată exenatidei a constatat că sensibilitatea la insulină s-a îmbunătățit în același grad atât în exenatidă, cât și în pacienți tratați cu insulină glargină.57 Grupul cu exenatide a înregistrat o reducere medie a greutății la un an de 3,6 kg, în timp ce grupul tratat cu glargină a crescut cu 1 kg. Disparitatea semnificativă statistic între grupuri în controlul greutății nu a generat, așa cum ne-am fi putut aștepta, o îmbunătățire mai mare a sensibilității la insulină în grupul cu exenatide.57
Spre deosebire de aceasta, în ciuda beneficiilor greutății mai modeste în contrast cu exenatida, sa constatat că tratamentul cu vildagliptin îmbunătățește sensibilitatea la insulină ca monoterapie sau ca supliment la metformină într-o serie de studii în care sensibilitatea la insulină a fost evaluată prin clema de insulină, model de sensibilitate la insulină la glucoză, 62 sau teste frecvente de toleranță intravenoasă la glucoză. 2 pacienți diabetici.61
Motivele acestor discrepanțe între efectele asupra greutății și sensibilitatea la insulină nu sunt clare. Acestea pot reflecta dinamica echilibrului caloric la pacienții tratați cu exenatidă sau vildagliptin, adică pacienții care au pierdut în greutate în studiile cu exenatidă au pierdut în greutate inițial și apoi au avut o perioadă susținută cu un grad foarte mic de echilibru caloric pozitiv, în timp ce cei care iau vildagliptin ar fi putut persista, într-o măsură foarte mică, într-o stare continuă de echilibru caloric negativ, în ciuda modificării minime a greutății nete.
Sensibilitatea îmbunătățită la insulină observată după șase săptămâni de terapie cu vildagliptin, evaluată prin clema euglicemică-hiperinsulinemică descrisă mai sus, a fost, de asemenea, asociată cu scăderea lipolizei de post și scăderea oxidării grăsimilor, 61 care este în concordanță cu reducerea trigliceridelor stocate în țesuturile negrase. Această constatare susține potențialul terapeutic al vildagliptinului pentru ameliorarea bolii hepatice grase nealcoolice
Concluzii
Vildagliptin este un inhibitor DPP-4 puternic și specific, care a demonstrat neutralitate în greutate la pacienții cu diabet de tip 2 în monoterapie multiplă și studii combinate. Riscul redus de hipoglicemie cu vildagliptin, care rezultă din mecanismul său de acțiune dependent de glucoză, contribuie probabil la această neutralitate a greutății prin evitarea „consumului defensiv” care poate apărea cu secretorii de insulină exogeni sau insulina independentă de glucoză. Cu toate acestea, dovezi suplimentare sugerează că vildagliptina poate influența metabolismul lipidelor și lipoproteinelor postprandiale prin inhibarea absorbției trigliceridelor din intestin53 și/sau promovarea mobilizării lipidice și catabolismului mediată simpatic în starea postabsorptivă. efecte favorabile asupra greutății asociate terapiei cu vildagliptin. În plus, insulina are acțiuni mediate central asupra foamei care ar putea fi atenuate de profilul insulinei mai sensibil la glucoză al vildagliptinei, iar acestea nu au fost încă evaluate.
Mulțumiri
Îi mulțumim lui Joe Hirsch, de la BioScience Communications, care a oferit asistență pentru scrierea medicală finanțată de Novartis.
- Unele relații între greutatea corporală, grăsimea corporală și aportul de calorii The American Journal of Clinical
- Vildagliptin îmbunătățește HbA1c, nu afectează greutatea corporală în diabetul de tip 2
- Victoria se află în centrele clinice de rutină pentru scăderea în greutate
- Antrenor personal de pierdere în greutate NYC 29 de ani de experiență Antrenor în pierdere în greutate
- De ce nu pot să slăbesc