Abstract
Vindecarea rănilor este un proces complex, foarte reglementat, care este esențial în menținerea funcției de barieră a pielii. Cu numeroase procese de boală, cascada evenimentelor implicate în vindecarea rănilor poate fi afectată, rezultând răni cronice, care nu vindecă, care supun pacientul la un disconfort și o suferință semnificative în timp ce drenează sistemul medical de o cantitate enormă de resurse. Vindecarea unei plăgi superficiale necesită mulți factori pentru a funcționa în mod concertat, iar pansamentele și tratamentele pentru plăgi au evoluat considerabil pentru a aborda posibilele bariere în calea vindecării rănilor, de la infecție la hipoxie. Chiar și în mod optim, țesutul plăgii nu atinge niciodată puterea pre-rănită și stările multiple de vindecare aberante pot duce la răni cronice care nu se vindecă. Acest articol va analiza fiziologia vindecării rănilor și va discuta abordările actuale pentru tratarea unei plăgi.
Introducere
Vindecarea ranilor fiziologice
După o rană superficială, o multitudine de sisteme sunt activate la fața locului pentru a elimina materialul străin, deoarece funcția principală de barieră a pielii se pierde și pentru a restabili în cele din urmă structura normală a pielii. În timp ce acest lucru poate avea succes doar într-o măsură limitată - o rană nu va atinge niciodată rezistența maximă la tracțiune a pielii neîncetate și, în cel mai bun caz, atinge aproximativ 70% [4] - majoritatea funcțiilor esențiale ale pielii vor fi readuse la o rană. Acest lucru necesită, cu toate acestea, livrarea diferitelor celule inflamatorii, chemokine, citokine, molecule matrice și substanțe nutritive la locul plăgii, cu o creștere concordantă a cererii metabolice. Aceste procese au loc simultan și sunt, în general, împărțite în trei faze principale ale vindecării rănilor: inflamatorii, proliferative și remodelate.
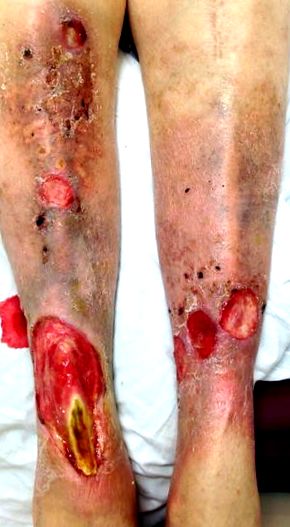
Având în vedere reglementarea strânsă a unei multitudini de factori necesari pentru vindecarea corectă a rănilor, nu este surprinzător faptul că rănile cronice sunt destul de frecvente. După o rană acută, cum ar fi traume, intervenții chirurgicale sau chiar o mușcătură de insecte, intră în joc seria bine coordonată de mai sus. Durata finală și rezultatul vor depinde de natura plăgii acute - locația, dimensiunea, adâncimea și tipul acesteia. Cu toate acestea, atunci când intră în joc alți factori patologici, cum ar fi starea de bază a bolii, se poate forma o rană cronică (vezi Fig. 1). Aceasta se referă la o rană care s-a abătut cumva de la evoluția fiziologică naturală descrisă anterior și s-a blocat la un moment dat. Mecanismul de bază variază foarte mult, dar include factori care influențează aportul de sânge (boala vasculară periferică), funcția imunitară (cum ar fi imunosupresia sau imunodeficiența dobândită), bolile metabolice (cum ar fi diabetul), medicamentele sau leziunile anterioare ale țesuturilor locale (cum ar fi radioterapia) . Factorii externi, cum ar fi presiunea susținută, temperatura și umiditatea, joacă, de asemenea, un rol important în a permite vindecarea unei plăgi. Deoarece fiziopatologia vindecării acute normale a rănilor a fost bine descrisă, această revizuire se va concentra în principal pe rănile cronice și tratamentul acestora.
Ulcerele cronice ale bolii vasculare periferice
Infecții ale rănilor
Cea mai frecventă provocare care poate fi prevenită pentru vindecarea rănilor este posibila infecție, iar antimicrobienele topice au fost utilizate de mult timp empiric pentru a încerca să prevină infecția rănilor. În timp ce bacteriile sunt o parte normală a florei pielii și, prin urmare, rănile, un prag critic de 105 bacterii a fost propus ca delimitare între colonizare și o infecție relevantă clinic care poate împiedica vindecarea rănilor [21]. De asemenea, este necesar să se facă distincția între o cultură pozitivă incidentală și un agent patogen adevărat care afectează o rană. Culturile de suprafață repetate într-o rană sunt de utilizare limitată, nici confirmând, nici excludând o infecție continuă; mai degrabă, diagnosticul clinic al unei plăgi infectate rămâne de primă importanță [22]. Culturile de țesuturi adânci sunt oarecum mai controversate. Deși au o sensibilitate și o specificitate mai bune în izolarea unui organism cauzator într-o rană infectată, acesta nu este încă perfect; s-a demonstrat că izolatele din diferite părți ale aceleiași plăgi au organisme diferite [23]. În plus, practicantul, în esență, exacerbează rana inițială cu o rană și mai profundă, dar aceasta poate fi totuși un compromis util dacă garantează o acoperire antimicrobiană adecvată.
Există multe abordări atât pentru tratamentul, cât și pentru prevenirea infecțiilor rănilor. Argintul a fost folosit ca adjuvant în îngrijirea rănilor de peste 2000 de ani [24] și rămâne un ingredient popular pentru îngrijirea rănilor astăzi. Are un spectru larg de activitate și este disponibil în numeroase forme. Progresele mai noi în utilizarea argintului pentru vindecarea rănilor s-au concentrat pe permiterea eliberării susținute de argint în concentrații suficient de mari pentru a permite eficacitatea menținută. Pansamentele de argint nanocristalin au fost dezvoltate având în vedere acest lucru și ajută la soluționarea deficienței pe care o are azotatul de argint - pentru a funcționa corect, ar trebui administrat de 12 ori pe zi [25]. Mai mult, o recenzie recentă nu a găsit dovezi convingătoare că sulfadiazina de argint are vreun efect asupra vindecării rănilor în general, în ciuda utilizării sale comune în rândul practicienilor [26]. În mod similar, compușii care conțin iod au fost folosiți de mult timp în vindecarea rănilor, dar au existat unele preocupări cu privire la toxicitatea compușilor care conțin iod, în special în zonele mari ale plăgii. Cu toate acestea, pentru răni limitate, iodul cadexomer (iodul dintr-o rețea de amidon formată în microbere) are o mulțime de date care susțin utilizarea acestuia ca adjuvant rentabil pentru vindecarea rănilor [27, 28].
Îngrijirea rănilor și pansamente
Câteva evoluții mai recente în pansamentele plăgii s-au concentrat pe integrarea compușilor antimicrobieni în pansamentul propriu-zis. Aceste materiale combină pansamente tradiționale pentru răni, cum ar fi spume sau hidrogeluri, cu compuși antimicrobieni precum argintul, betaina, chitina sau polihizametilen biguanida (Kendall AMD). Aceste materiale, așa cum s-a discutat anterior, s-ar putea să nu fie adecvate pentru aplicarea cu spectru larg la vindecarea rănilor, dar pot fi adecvate în ulcerele cronice ale piciorului inferior, unde infecția poate fi o problemă, în special cu formarea biofilmelor. Mulți agenți patogeni sunt capabili să adere împreună în biofilme, care reprezintă mase strâns înconjurate de o matrice polimerică, ajutând astfel la evitarea distrugerii de către antibiotice. Acest lucru creează nu numai o barieră fizică în calea vindecării rănilor, ci una în care rezoluția normală a fazei inflamatorii poate fi prelungită, iar abordarea biofilmelor a devenit o provocare majoră în vindecarea rănilor. Atât testele in vitro, cât și datele pacienților arată că aceste pansamente antimicrobiene pot fi utile în apariția ulcerelor cronice/venoase care pot fi afectate de aceste biofilme [43, 44].
Înlocuitori ai pielii
O altă opțiune care a primit o nouă indicație FDA în 2016 pentru ulcerele piciorului diabetic este Șablonul de regenerare cutanată Integra (Omnigraft). Acest material este o matrice bicelulară celulară formată din colagen, glicozaminoglican și condroitin-6-sulfat, cu un strat de silicon pentru funcția de barieră [50]. Acesta a fost folosit din 1996 pentru arsuri, cu o aprobare ulterioară pentru cicatricile provocate de arsuri, dar mai recent a obținut aprobarea pentru ulcerele piciorului diabetic pe baza unui studiu pivot de la 32 de locuri și peste 300 de pacienți. Datele au arătat că tratamentul cu Omnigraft a crescut rata de închidere a plăgii cu 50% comparativ cu standardul de îngrijire, cu timpul până la închiderea plăgii redus cu 5 săptămâni. Un beneficiu major al Omnigraft este că, în marea majoritate a cazurilor (72%), este necesară o singură aplicare a substratului pentru vindecarea completă a rănilor, peste 90% din răni necesitând două sau mai puține aplicații [50].
Terapia cu răni prin presiune negativă
Factori de creștere
Oxigen hiperbaric
Camera de terapie a plăgilor cu oxigen hiperbaric (Sigma 34 Hyperbaric Chamber, Perry Biomedical, Riviera Beach, FL, SUA)
- O revizuire a nutraceuticelor actuale în gestionarea osteoartritei
- Programul de instruire pentru managementul nutriției bolilor cronice renale NIDDK
- Boala renală cronică în Japonia de la predicțiile timpurii până la faptele actuale - FullText - Nephron
- Diagnosticul și managementul pancreatitei cronice - Biblioteca de știri din sudul sănătății
- Tratamente dietetice și medicale ale obezității O revizuire evaluativă - ScienceDirect