Hua V. Lin
1 Diabet și farmacologie in vivo, Merck Research Laboratories, Rahway, New Jersey, Statele Unite ale Americii,
Andrea Frassetto
1 Diabet și farmacologie in vivo, laboratoare de cercetare Merck, Rahway, New Jersey, Statele Unite ale Americii,
Edward J. Kowalik Jr.
1 Diabet și farmacologie in vivo, laboratoare de cercetare Merck, Rahway, New Jersey, Statele Unite ale Americii,
Andrea R. Nawrocki
1 Diabet și farmacologie in vivo, laboratoare de cercetare Merck, Rahway, New Jersey, Statele Unite ale Americii,
Mofei M. Lu
1 Diabet și farmacologie in vivo, laboratoare de cercetare Merck, Rahway, New Jersey, Statele Unite ale Americii,
Jennifer R. Kosinski
1 Diabet și farmacologie in vivo, laboratoare de cercetare Merck, Rahway, New Jersey, Statele Unite ale Americii,
James A. Hubert
1 Diabet și farmacologie in vivo, Merck Research Laboratories, Rahway, New Jersey, Statele Unite ale Americii,
Daphne Szeto
1 Diabet și farmacologie in vivo, laboratoare de cercetare Merck, Rahway, New Jersey, Statele Unite ale Americii,
Xiaorui Yao
1 Diabet și farmacologie in vivo, laboratoare de cercetare Merck, Rahway, New Jersey, Statele Unite ale Americii,
Gail Forrest
1 Diabet și farmacologie in vivo, laboratoare de cercetare Merck, Rahway, New Jersey, Statele Unite ale Americii,
Donald J. Marsh
2 Evaluarea siguranței, Merck Research Laboratories, West Point, Pennsylvania, Statele Unite ale Americii,
Conceput și proiectat experimentele: HVL AF ARN DJM. Au efectuat experimentele: HVL AF EJK ARN MML JRK JAH DS XY. Analizate datele: HVL AF EJK DS XY GF. Am scris lucrarea: HVL DJM.
Abstract
Introducere
Acizii grași cu lanț scurt (SCFA) sunt produși de microbiota în colon și în intestinul subțire distal din amidon rezistent, fibre dietetice și alte polizaharide slab digerabile într-un proces de fermentare [1]. Acetatul, propionatul și butiratul sunt SCFA predominante în lumenul intestinal la om și la rozătoare și sunt prezente la niveluri ridicate de mM [2]. Odată produse, SCFA sunt ușor absorbite de colonocite. Butiratul este utilizat în mare măsură de epiteliul colonic ca sursă de energie, iar propionatul este utilizat în principal de către ficat, unde o cantitate semnificativă de acetat intră în circulația sistemică și ajunge în țesuturile periferice. Pe lângă faptul că acționează ca surse de energie, SCFA sunt și molecule de semnalizare. Receptorii cuplați cu proteina G Receptorul liber al acidului gras 2 (FFAR2, GPR43) și FFAR3 (GPR41) au fost identificați ca receptori endogeni pentru SCFA. Acetatul activează preferențial FFAR2 in vitro; propionatul prezintă un agonism similar pe FFAR2 și FFAR3; și butiratul activează preferențial FFAR3 [3], [4].
În acest studiu, am examinat efectele SCFA asupra greutății corporale, a metabolismului glucozei și a hormonilor intestinali la șoarecii knockout de tip sălbatic și Ffar3. Arătăm că butiratul și propionatul suprimă consumul de alimente, protejează împotriva creșterii în greutate induse de dietă bogată în grăsimi și a intoleranței la glucoză și stimulează secreția hormonului intestinal predominant prin mecanisme independente de FFAR3. De asemenea, arătăm că FFAR3 nu este necesar pentru greutatea corporală normală și pentru homeostazia glucozei.
Rezultate
SCFA suprimă obezitatea indusă de dietă prin mecanisme distincte
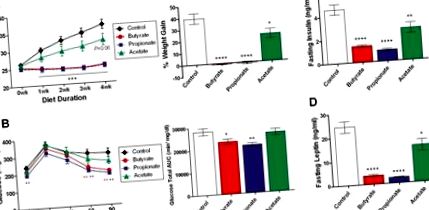
Șoarecii slabi C57BL/6N în vârstă de trei luni au fost comutați la HFD conținând săruri de sodiu de butirat (5% g/g), propionat (4,3%) și acetat (3,7%) cu molaritate, timp de patru săptămâni. (A) Greutatea corporală a fost măsurată săptămânal, iar creșterea în greutate cumulată de patru săptămâni este exprimată ca procent din greutatea corporală inițială. (B) Testul oral de toleranță la glucoză a fost efectuat la șoareci la jeun peste noapte la patru săptămâni după trecerea dietei. Sunt prezentate nivelurile de glucoză din sânge și suprafața totală a glucozei sub curbă (ASC). (C, D) Nivelurile plasmatice ale insulinei și leptinei au fost determinate la șoareci la jeun peste noapte la patru săptămâni după trecerea dietei. Datele sunt medii ± SEM. N = 8. * P Figura 3A-C) și nivelurile ambilor hormoni s-au normalizat până la momentul inițial la șaizeci de minute după administrare (datele nu sunt prezentate). PYY a arătat, de asemenea, o creștere moderată în zece minute după administrarea orală de butirat (Figura 3D). Aceste modificări au fost asociate cu creșterea insulinei plasmatice și a amilinei (Figura 3E, F) la șoarecii tratați cu butirat, în concordanță cu stimularea celulelor β pancreatice de către incretine. Propionatul de sodiu a crescut semnificativ GIP, insulina și amilina, dar nu GLP-1 sau PYY. Un amestec SCFA care imită proporțiile endogene prezente în colon (acetat 260mpk, propionat 80mpk și butirat 60mpk) a provocat, de asemenea, o creștere modestă a GIP. În schimb, niciunul dintre hormonii examinați nu a fost modificat semnificativ de acetat de sodiu dozat fie la 400 mg/kg (Figura 3), fie la 300 mg/kg (molaritate potrivită cu provocarea cu butirat de sodiu, date neprezentate). În plus, acidul octanoic cu acid gras cu lanț mediu (OA) și acidul α-linolenic (LA) cu acid gras cu lanț lung nu au prezentat niciun efect semnificativ. Este demn de remarcat faptul că ordinea de rang a butiratului> propionatului> acetatului în stimularea peptidelor anorexigenice GLP-1, PYY și amilină este în concordanță cu efectele lor asupra inhibării consumului de alimente, butiratul fiind cel mai puternic (Figura 2A).
(AF) Șoarecii slabi C57BL/6N în vârstă de trei luni au fost postiti peste noapte și dozați oral cu soluție salină, butirat de sodiu, propionat de sodiu, acetat de sodiu, un amestec SCFA (65% acetat de sodiu, 20% propionat de sodiu, 15% butirat de sodiu), acid octanoic (OA) sau acid α-linolenic (LA), totul la 400 mg/kg greutate corporală. Nivelurile plasmatice ale GLP-1 total, GLP-1 activ, GIP, PYY, insulină și amilină au fost măsurate la 10 minute după administrare. CV intra-test% a fost sub 8,9% pentru toate imunoanalizele. Datele sunt medii ± SEM. N = 8. * P Figura 4A). Șoarecii au fost apoi comutați la HFD suplimentat cu butirat și propionat timp de opt zile. Atât butiratul, cât și propionatul au inhibat creșterea în greutate și aportul de alimente în eliminările Ffar3 în aceeași măsură ca la șoarecii de tip sălbatic (Figura 4B-D). Interesant, deși eliminările Ffar3 la controlul HFD nu au arătat nicio diferență în greutatea corporală în comparație cu colegii de tip sălbatic, au arătat o creștere modestă cu 9% a consumului de alimente (Figura 4E), în concordanță cu eficiența redusă a recoltei energetice din dieta raportată într-un eliminator separat Ffar3 linie [11].
(A) Greutatea corporală a eliminatorilor Ffar3 în vârstă de trei luni și a colegilor de tip sălbatic la dieta standard de chow și la o săptămână după trecerea la HFD. N = 34-41. (B-D) După o săptămână de hrănire HFD, eliminările Ffar3 și colegii de tip sălbatic au fost trecuți la HFD conținând butirat de sodiu (5%) sau propionat de sodiu (4,3%) timp de opt zile. Sunt prezentate modificările cumulate ale greutății corporale și aportul zilnic de alimente. Datele sunt medii ± SEM. N = 8-13. * P Figura 5A). Acest model de expresie este în concordanță cu un rol potențial în secreția peptidică din L, K și alte celule enteroendocrine. Knockout-urile Ffar3 au prezentat niveluri normale de GLP-1 la post total și active, dar secreția totală de GLP-1 indusă de butirat a fost atenuată în absența FFAR3 (Figura 5B, C). Nivelurile GIP în eliminările Ffar3 au avut tendințe mai mici decât controalele de tip sălbatic în condiții bazale și stimulate de butirat, dar gradul de stimulare de către butirat a fost similar între genotipuri, iar cel de propionat a arătat o ușoară creștere a eliminărilor (Figura 5D, E). Stimularea PYY și a insulinei de către butirat a fost tocită în această cohortă, probabil din cauza expunerii la HFD timp de patru săptămâni și nu a prezentat nicio diferență semnificativă între genotipuri (Figura 5F, G). Aceste date sugerează stimularea butiratului secreției GLP-1 din celulele L este mediată parțial de FFAR3, în timp ce efectele stimulatoare ale butiratului și propionatului asupra secreției GIP din celulele K sunt independente de FFAR3. Interesant este că butiratul a redus semnificativ nivelurile plasmatice de grelină în eliminările Ffar3, în timp ce acest efect nu a atins semnificația statistică la șoarecii martori (Figura 5H).
(A) Compoziția corpului a fost determinată prin RMN cantitativă la eliminările Ffar3 și la colegii de tip sălbatic după cinci luni de hrănire cu HFD. (B, C) Nivelurile de leptină plasmatică au fost determinate în eliminările nocturne Ffar3 postite peste noapte și în colegii de tip sălbatic menținuți pe dieta standard de chow sau HFD. (D) Glicemia a fost măsurată la șoareci hrăniți ad libitum menținuți pe HFD la trei ore după începerea fazei luminoase. (E) Test de toleranță orală la glucoză după post peste noapte și (F) test de toleranță la insulină intraperitoneală după post de cinci ore în timpul zilei în eliminările Ffar3 și colegii de tip sălbatic menținuți pe HFD. Datele sunt medii ± SEM. N = 8-14.
Discuţie
S-a raportat că nivelurile de SCFA în lumenul intestinal au atins niveluri ridicate de mM în colonul uman și al porcilor, dar sunt mult mai mici în jejun și ileon [21]. În studiul actual, dozele de SCFA-uri alese au fost în domeniul mM ridicat, realizând probabil niveluri suprafiziologice in vivo, în special în intestinul proximal. Astfel, efectele asupra hormonilor intestinali pot să nu reflecte acțiunea fiziologică a SCFA, dar sugerează potențialul beneficiu al tratamentului farmacologic cu SCFA. SCFA administrate oral pot ajunge probabil la intestinul subțire proximal în decurs de 10 minute - momentul timpuriu ales pentru studiile acute - deoarece golirea gastrică a unui bolus lichid la șoareci este foarte rapidă și poate depăși 80% în decurs de 15 minute [22]. Cu toate acestea, este puțin probabil ca bolusul SCFA oral să ajungă la intestinul subțire distal și colon în 10 minute. Prin urmare, efectele asupra GLP-1 și GIP pot reflecta stimularea directă a celulelor enteroendocrine în intestinul subțire proximal, unde pot fi găsite atât celulele L, cât și celulele K. Pe de altă parte, celulele L care exprimă PYY sunt prezente numai în colon și în intestinul subțire distal, sugerând un mod indirect de acțiune al butiratului asupra acestui hormon intestinal.
Inhibarea dependentă de butirat și propionat a aportului de alimente și creșterea în greutate a fost intactă la șoarecii knockout Ffar3, implicând alți mediatori endogeni în aceste efecte. Este demn de remarcat faptul că eliminările Ffar3 la controlul HFD au prezentat hiperfagie modestă, dar au avut greutate corporală normală și adipozitate. Acest lucru este în concordanță cu un raport anterior care arată tranzitul intestinal accelerat și creșterea excreției energiei fecale într-o linie de eliminare Ffar3 independentă [11], sugerând că FFAR3 este necesar pentru motilitatea intestinală normală și absorbția nutrienților. Mecanismele responsabile pentru creșterea aportului de alimente și normalizarea greutății corporale în absența FFAR3 sunt necunoscute. S-a demonstrat că SCFA reglează secreția de leptină din țesutul adipos. Cu toate acestea, rolul FFAR3 în medierea acestor efecte rămâne controversat [23], [24]. Am arătat că eliminările Ffar3 mențin nivelurile normale de leptină plasmatică, sugerând că leptina nu are un rol major în normalizarea homeostaziei energetice în eliminările Ffar3. S-a raportat recent că șoarecii knock-out Ffar3 au redus ritmul cardiac în repaus și activitatea simpatică [19]. Cu toate acestea, este de așteptat ca acest efect să reducă cheltuielile cu energia și nu poate explica eficiența redusă a hranei pentru eliminările Ffar3.
Studii privind provocarea acută și suplimentarea dietei
Butirat de sodiu, propionat de sodiu, acetat de sodiu, acid octanoic și acid α-linolenic au fost obținute de la Sigma-Aldrich (St. Louis, MO). Pentru studii acute, șoarecii au fost postiti peste noapte și li s-a administrat p.o. la 6ml/kg cu compuși dizolvați în soluție salină. Pentru studii de suplimente alimentare, sărurile de sodiu ale SCFA-urilor în formă solidă au fost bine amestecate într-o dietă bogată în grăsimi folosind un robot de bucătărie la 300-400 rpm, formate în bile de 50-60g și utilizate imediat. Dieta de control a fost procesată în mod similar fără adăugarea de SCFA. În studii mai lungi de 10 zile, dieta proaspătă a fost făcută și completată săptămânal. Pentru studiile acute efectuate la șoareci knockout Ffar3 și colegii de tip sălbatic, aceeași cohortă care a fost utilizată pentru studiul de suplimente alimentare de 8 zile a fost readusă la HFD normal timp de 3 săptămâni, apoi re-randomizată și utilizată pentru experimentele de provocare acută cu butirat/propionat din cauza disponibilitate limitată a animalelor. Amploarea stimulării GLP-1 și GIP active de către butirat a fost similară între șoarecii de tip sălbatic din dieta regulată cu chow și cei de pe HFD de 4 săptămâni.
Măsurători plasmatice
Sângele a fost colectat prin puncție cardiacă sau sângerări submandibulare în tuburi EDTA care conțin inhibitor DPP4 (Millipore, Billerica, MA) și cocktail inhibitor de protează (Sigma-Aldrich). GLP-1 total și GLP-1 activ au fost măsurate folosind imunoanalize de la Meso Scale Discovery (Gaithersburg, MD). GIP total, PYY activ, insulină, amilină, leptină și grelină totală au fost măsurate folosind panoul hormonal intestinal Milliplex (Millipore).
Analize metabolice
Testul de toleranță la glucoză (3g/kg po) a fost efectuat în urma unui post peste noapte la șoareci C57BL/6N care au fost hrăniți cu HFA cu SCFA suplimentat timp de patru săptămâni și la Ffar3 -/- și colegii de gunoi de tip sălbatic de cinci până la șase luni care a fost hrănit cu HFD timp de șase săptămâni. Testul de toleranță la insulină (0,75 U/kg i.p.) a fost efectuat la colegii de litere Ffar3 -/- în vârstă de șase până la șapte luni pe HFD timp de zece săptămâni după o îndepărtare de 5 ore pe zi. Glucoza a fost măsurată din sângele din coadă cu un contor OneTouch Ultra (LifeScan, Milpitas, CA). Compoziția corpului a fost determinată cu un Bruker minispec RMN (Bruker Optics, Billerica, CA) la Ffar3 -/- în vârstă de opt luni și colegii de așternut de tip sălbatic care au fost hrăniți cu HFD timp de douăzeci de săptămâni. Activitatea locomotorie a fost măsurată utilizând un sistem cuprinzător de monitorizare a animalelor de laborator (Columbus Instruments, Columbus, OH) așa cum s-a descris anterior [31].
Analize statistice
Datele au fost analizate prin testul t Student sau ANOVA unidirecțional cu testul Bonferroni post. Valorile P mai mici de 0,05 au fost considerate semnificative.
Mulțumiri
Mulțumim lui A. Pocai, D.E. Kelley, M. Trujillo și alți colegi de la Merck Research Laboratories pentru discuții utile și lectură critică a manuscrisului.
Note de subsol
Interese concurente: Toți autorii sunt angajați ai Merck Research Laboratories, Rahway. Nu există brevete, produse în curs de dezvoltare sau produse comercializate de declarat. Acest lucru nu modifică aderarea autorilor la toate politicile PLoS ONE privind schimbul de date și materiale.
Finanțarea: Autorii nu au sprijin sau finanțare de raportat.
- Butiratul, dar nu propionatul, inversează deficitele neurocognitive induse de dieta maternă la descendenți
- Rezumat P436 Rolul acizilor grași liberi la pacienții cu obezitate și insuficiență cardiacă cu
- Biomateriale care reglează digestia grăsimilor pentru tratamentul obezității - ScienceDirect
- Evaluarea șobolanilor obezi induși de dietă ca model de obezitate prin genomică funcțională comparativă -
- Obezitate bivolă Articolul despre obezitate bivolă de The Free Dictionary