Termeni asociați:
- Recuperarea memoriei
- Amigdala
- Hipocamp
- Lobul temporal medial
- Neuroni
- Stres post traumatic
- Cortexul frontal
- Segmentare
Descărcați în format PDF
Despre această pagină
Îmbunătățirea performanței pentru acțiune și percepție
Edward F. Pace-Schott, Rebecca M.C. Spencer, în curs de cercetare a creierului, 2011
Studii de consolidare dependente de somn la îmbătrânirea sănătoasă
O mână de studii recente au cercetat dacă procesele de memorie dependente de somn se schimbă și odată cu creșterea vârstei. Înainte de evaluările experimentale, două lucrări teoretice au emis ipoteza că consolidarea dependentă de somn ar fi diminuată la adulții în vârstă. Hornung și colab. (2005) au prezis o relație între reducerea memoriei și modificările fiziologiei somnului care sunt frecvent observate la adulții în vârstă. Conform acestei lucrări teoretice, reducerea somnului și a memoriei poate împărtăși o sursă comună, cum ar fi reducerea volumului creierului sau modificări cardiovasculare sau neurochimice. În schimb, relația poate fi directă: schimbările în somn - cum ar fi reducerea SWS, REM sau densitatea axului - pot duce la reducerea memoriei.
Conform ipotezei lui Buckley și Schatzberg (2005), modificările axei hipotalamo - hipofiză - suprarenale (HPA) la adulții în vârstă stau la baza reducerii calităților somnului și, prin urmare, a reducerii memoriei la adulții în vârstă. Axa HPA este o buclă de feedback care controlează răspunsul la stres și alte procese prin eliberarea cortizolului. Cortizolul fluctuează, de asemenea, într-un ritm circadian, cu un vârf dimineața și scăzând pe tot parcursul zilei până la un nadir de seară. Ritmul circadian este aplatizat la adulții în vârstă, iar axa HPA devine hiperactivă. Combinația acestor două modificări, potrivit lui Buckley și Schatzberg (2005), are ca rezultat modificări legate de vârstă ale somnului care, la rândul lor, reduc consolidarea memoriei dependente de somn.
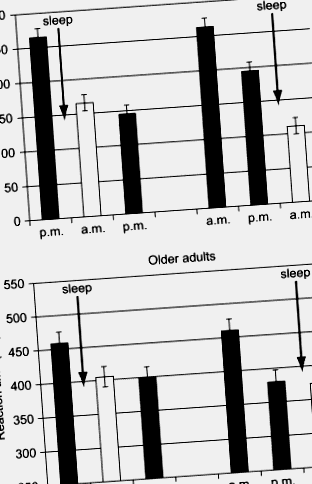
FIG. 2. Timpul de reacție la o sarcină explicită de învățare a secvenței după intervale de 12 ore, fie conținând somn peste noapte (de exemplu, 20:00 până la 20:00) sau petrecut treaz (de exemplu, 20:00 la 20:00). Adulții tineri (panoul superior) arată în mod constant cele mai mari îmbunătățiri ale performanței (scăderea timpului de reacție) după somn, indiferent dacă prima dintre cele trei sesiuni are loc seara (partea stângă) sau dimineața (dreapta). În timp ce adulții în vârstă prezintă o îmbunătățire după prima ședință, această modificare nu depinde de somn.
Siengsukon și Boyd (2008, 2009) au examinat dacă modificările de performanță legate de somn ar fi evidente la indivizii după accident vascular cerebral. Participanții adulți sănătoși, cu vârsta de aproximativ 55-75 de ani, au servit drept controale. Și ei au descoperit că performanța a fost neschimbată după somn la adulții în vârstă sănătoși. De fapt, într-un al doilea studiu care a comparat modificările off-line asupra sarcinilor de învățare motorie explicite și implicite, adulții vârstnici sănătoși au prezentat modificări similare ale performanței la intervale de somn și intervale de trezire, indiferent de conștientizare (Siengsukon și Boyd, 2009). Cu toate acestea, performanța grupului poststroke a arătat modificări semnificative ale performanței după somn. Autorii sugerează că acest beneficiu de somn păstrat, care a fost absent în controalele sănătoase potrivite vârstei, este legat de creșterea somnului nREM2 și a densității fusului, care a fost observată după accident vascular cerebral (Vock și colab., 2002).
Două studii recente au examinat consolidarea dependentă de somn a învățării nemotorii la adulții în vârstă. Aly și Moscovitch (2010) au comparat amintirea episodică după un interval de somn peste noapte în raport cu amintirea după un interval de zi petrecut treaz. În timp ce adulții mai în vârstă (69-80 de ani) au prezentat o uitare mai mare în ambele intervale față de grupul de adulți tineri (19-29 de ani), protecția memoriei oferite de somn nu a diferit în funcție de grupele de vârstă, indicând o economie a somnului dependent procesul de consolidare a memoriei. De asemenea, am găsit o consolidare a memoriei dependente de somn la adulții mai în vârstă cu o sarcină de învățare în perechi de cuvinte. Am comparat modificările procesării memoriei dependente de somn a unei sarcini de învățare a secvenței motorii cu modificările off-line în învățarea perechii de cuvinte (Wilson și colab., Prezentat). Din nou, adulții în vârstă (55-70 de ani) nu au prezentat modificări de performanță dependente de somn în sarcina de învățare motorie. Cu toate acestea, aceiași indivizi au prezentat o protecție similară a performanței în funcție de somn în sarcina pereche de cuvinte.
Acest studiu (Wilson și colab., Prezentat) a inclus, de asemenea, adulți de vârstă mijlocie (35-50 de ani) și raportăm că modificările lor de performanță în timpul somnului și al trezirii au fost similare cu adulții tineri în ambele sarcini. Cu toate acestea, Backhaus și colab. (2007) sugerează că consolidarea dependentă de somn a amintirilor declarative este redusă în această grupă de vârstă (48-55 ani) în comparație cu adulții tineri. Adulții tineri și-au amintit mai multe perechi de cuvinte în sarcina de învățare a perechilor de cuvinte asociate după somnul devreme (bogat în SWS) decât somnul târziu (bogat în REM). Grupa de vârstă mijlocie nu a prezentat nicio modificare semnificativă în niciunul dintre intervale. Cu toate acestea, atunci când au luat în considerare măsurile fiziologice la acești subiecți, au constatat că indivizii de vârstă mijlocie care au obținut aceeași cantitate de SWS ca adulții tineri au prezentat o consolidare mai mare după somn decât cei de vârstă mijlocie care au rămas treji.
Abordări farmacologice pentru a înțelege, preveni și atenua amintirile dureroase. Lecții din tulburările de stres posttraumatic
3.3 Principalele strategii farmacologice pentru a atenua sau preveni memoria traumatică: rezultate din studiile empirice
Deoarece norepinefrina joacă un rol central în codificarea și consolidarea memoriei emoționale încă de la începutul oricărei expuneri traumatice și deoarece hiperarousarea noradrenergică poate duce atât la afectări de bază ale controlului cognitiv, cât și la modularea eficientă a excitației emoționale mediată în mod normal de sistemele prefrontale, contracarând hiperactivitatea noradrenergică. să fie un prim pas promițător pentru a preveni o tranziție riscantă la PTSD după stresul traumatic. Hiperactivitatea noradrenergică poate fi redusă atât prin antagonismul β- și α1-adrenergic postsinaptic, cât și prin agonismul α2-adrenergic presinaptic (Schwabe, Nader, Wolf, Beaudry și Pruessner, 2012). Sunt disponibile mai multe instrumente farmacologice și au fost investigate în studii empirice. Până în prezent, rezultatele au fost inconsistente.
Pitman, Sanders și Zusman (2002) au făcut un prim studiu pilot. Au recrutat 41 de persoane care au prezentat criteriile DSM-IV A1 și A2 și semne de activitate autonomă crescută (puls de odihnă> 80/min) într-o cameră de urgență imediat după un eveniment traumatic (în mare parte accidente grave de vehicule cu motor). Pacienții au fost înrolați într-un studiu randomizat, dublu-orb și controlat cu placebo, primind fie 4 × 40 mg propranolol/zi, fie placebo pe parcursul a 10 zile. După o lună, doi pacienți din grupul cu propranolol au îndeplinit criteriile de diagnostic ale PTSD în conformitate cu Scala PTSD administrată de clinicieni, totuși șase pacienți din grupul placebo (p = 0,19). La urmărirea de 3 luni, un pacient din grupul cu propranolol și trei pacienți din grupul placebo au prezentat PTSD (p = 0,35). Această tendință pozitivă, dar statistic nesemnificativă (datorită unei puteri mult prea mici) a fost subliniată într-o investigație psihofiziologică suplimentară, bazată pe scripturi, care indică hiperarousal autonom la niciunul dintre pacienții din grupul cu propranolol și la opt pacienți din grupul placebo (p = 0,004). Alte studii controlate, dar neblindite și non-randomizate, de asemenea, au vorbit în favoarea unei blocade β-adrenergice în această indicație (Taylor și colab., 2002; Vaiva, Ducrocq și Jezequel, 2003). Un studiu randomizat, dublu-orb și controlat cu placebo sau cu gabapentină, cu pacienți după leziuni traumatice, nu a putut confirma niciun avantaj al propranololului (Stein, Kerridge, Dimsdale și Hoyt, 2007). Există rezultate negative dintr-o utilizare profilactică a propranololului la pacienți după arsuri severe în ceea ce privește incidența PTSD ulterioară (McGhee, Maani și Garza, 2009; Sharp, Thomas și Rosenberg, 2010).
Studiile deschise cu substanțe α2-agoniste, cum ar fi clonidina sau guanfacina, care reduc ambele eliberarea de norepinefrină din veziculele presinaptice în fanta sinaptică promit un potențial preventiv (Morgan, Krystal și Southwick, 2003). Cu toate acestea, până în prezent, niciun studiu controlat prospectiv nu a investigat nicio utilizare preventivă a acestor substanțe. Studiile controlate în tratamentul veteranilor cu PTSD cronică au găsit rezultate negative ale guanfacinei (Davis și colab., 2008; Neylan, Lenoci și Samuelson, 2006). Prazosina antagonistă α1, ale cărei efecte pozitive asupra tulburărilor de somn și a coșmarurilor legate de PTSD au fost bine stabilite în mai multe studii controlate randomizate (Germain, Richardson și Moul, 2012; Raskind, Peskind și Hoff, 2007; Raskind, Peskind și & Kanter, 2003; Taylor, Martin și Thompson, 2008), ar putea fi un alt candidat promițător în prevenirea posibilă a tranziției la PTSD după expunerea la traume. Această indicație necesită totuși o investigație farmacologică adecvată.
În general, contracararea hiperactivității noradrenergice ulterioare stresului traumatic pare să fie încă o opțiune interesantă pentru studiile timpurii pentru prevenirea sau reducerea riscului de tranziție la PTSD. Studiile randomizate controlate cu placebo efectuate până acum sunt rare și, de regulă, au inclus doar probe mici de pacienți. Rezultatele studiilor sunt inclusive (Hoge, Worthington și Nagurney, 2012). Orice intervenție, cum ar fi cu o blocadă β-adrenergică, trebuie să evalueze foarte atent semnele clinice ale hiperarousalului autonom și să aprecieze fiziopatologia generală care poate fi destul de complicată în stările de leziuni corporale (de exemplu, arsuri) sau boli somatice asociate (Schelling, 2008 ).
Este bine stabilit că sistemul endogen de opiacee participă la reglarea învățării emoționale și a memoriei și, prin urmare, joacă un rol central în timpul și după expunerea la traume (Garakani și colab., 2009). Pe baza rapoartelor clinice, utilizarea timpurie a opiaceelor la pacienții cu arsuri traumatice severe pare să fie corelată cu o incidență mai mică a PTSD ulterioară (Saxe, Stoddard și Courtney, 2001; Stoddard, Sorrentino și Ceranoglu, 2009). Experiențele medicale militare cu soldați grav răniți în timpul luptei consolidează, de asemenea, o strategie de utilizare timpurie a opiaceelor (Holbrook, Galarneau și Dye, 2010). Durerea persistentă și incontrolabilă poate fi considerată un factor de risc adecvat pentru PTSD ulterior (Norman, Stein, Dimsdale și Hoyt, 2008; Schelling, 2008). Cu toate acestea, încă nu a fost stabilit dacă opiaceele produc un efect general autentic de reducere a riscului de PTSD dincolo de un efect analgezic special (Bryant, Creamer, O'Donnell, Silove și McFarlane, 2009).
Serotonina modulează reactivitatea noradrenergică și excitația autonomă. Are un impact asupra funcționării axei HPA. În general, mediază efecte inhibitoare atât asupra activității neuronale, cât și asupra plasticității. O neurotransmisie serotoninergică bine echilibrată este o condiție prealabilă de bază pentru orientarea flexibilă a realității și reacția adecvată. Orice stres prelungit și incontrolabil, ca în situații traumatice, poate duce la disfuncții serotoninergice (Krystal & Neumeister, 2009). Antidepresivele serotoninergice joacă un rol primordial în tratamentul farmacologic al PTSD stabilit. Cu toate acestea, au existat doar foarte puține încercări de a demonstra empiric orice potențial preventiv al substanțelor serotoninergice la scurt timp după expunerea la traume (Zohar, Sonnino, Juven-Wetzler și Cohen, 2009). Un studiu randomizat, dublu-orb și controlat cu placebo nu a putut stabili un efect superior al escitalopramului în această indicație la adulți după diferite traume (Shalev și colab., 2012). Cu copiii care suferă de arsuri grave, cu toate acestea, sertralina a demonstrat un efect preventiv semnificativ statistic, care trebuia considerat, din punct de vedere clinic, cel mult mediu (Stoddard, Luthra și Sorrentino, 2011).
Potențialul translațional al reconsolidării memoriei
Philip R. Corlett, Jane R. Taylor și Memory Reconsolidation, 2013
13.1 Introducere
Amintirile ne permit să ne bazăm pe experiența noastră din trecut pentru a răspunde adaptativ în prezent și a planifica viitorul nostru (Dudai & Eisenberg, 2004). Cu toate acestea, ele nu sunt pur și simplu o înregistrare a trecutului care poate fi redată după cum este necesar și nu sunt întotdeauna veridice sau adaptative (Estes, 1997). Apariția neuroștiinței cognitive și aplicarea acesteia la problemele din psihiatrie - neuropsihiatria cognitivă - a determinat oamenii de știință clinicieni să caracterizeze multe dintre simptomele bolilor mintale ca patologii ale formării, întreținerii și utilizării memoriei (Halligan și David, 2001). În acest capitol, revizuim unele dintre aceste afirmații cu privire la reconsolidarea memoriei, fie ca mecanism fiziopatologic (Corlett și colab., 2009), fie ca o fereastră terapeutică potențială (Debiec, 2012; Taylor și colab., 2009), evaluând veridicitatea acestora. comparativ cu datele clinice disponibile. Discutăm despre implicațiile etice ale terapiilor de modificare a memoriei. De asemenea, prezentăm câteva dintre ceea ce credem că vor fi obstacole practice și complexități asociate cu încercarea de a modifica amintirile aberante la pacienții umani, evidențiate prin lucrări preclinice care explorează condițiile limită și idiosincrasiile reconsolidării memoriei (Inda și colab., 2011).
Fenomenul reconsolidării memoriei este observat atunci când, după codificarea și consolidarea memoriei, o procedură de reamintire reactivează memoria inițială într-o stare labilă în care devine susceptibilă la intervenții care împiedică consolidarea ulterioară a acesteia (Misanin și colab., 1968; Nader și colab., 2000; Przybyslawski și Sara, 1997). Aceste intervenții destabilizante pot degrada recuperarea ulterioară a memoriei inițiale, poate chiar ștergând-o complet (Kindt și colab., 2009). Desigur, nu este sigur dacă memoria este cu adevărat ștearsă sau, mai degrabă, este anulată și inhibată de o nouă învățare de dispariție (Osan și colab., 2011). Echilibrul dintre dispariție și reconsolidare este un alt aspect cheie al potențialului aport fiziopatologic și potențial terapeutic al proceselor de memorie aberante (Corlett și colab., 2009; Eisenhardt și Menzel, 2007; Pedreira și colab., 2004). Apelul clinic de a avea capacitatea de a elimina sau inhiba amintirile nedorite a fost mult timp apreciat; aici, Macbeth al lui Shakespeare îl imploră pe doctor să-și trateze soția:
Nu poți sluji o minte sfidată,
Scoate din memorie o durere înrădăcinată,
Rasește necazurile scrise ale creierului,
Și cu niște dulci antidot ignoranți
Curăță-ți sânul de lucruri periculoase
Care cântărește asupra inimii?
Acest potențial nu a fost încă realizat, dar există câteva constatări inițiale interesante în tratarea pacienților umani cu tulburare de stres post-traumatică (PTSD), anxietate și dependență. Mai mult, având în vedere ce funcție ar putea servi reconsolidarea memoriei (Alberini, 2011; Stickgold și Walker, 2007), modelele teoretice ale unor simptome au implicat reconsolidarea excesivă a memoriei ca proces fiziopatologic. De exemplu, iluziile care apar la boli mintale grave, cum ar fi schizofrenia, ar putea fi menținute în fața dovezilor contradictorii din cauza reconsolidării necorespunzătoare a memoriei (Corlett și colab., 2009); adică, dacă funcția reconsolidării memoriei este de a actualiza și eficientiza amintirile în lumina noilor informații (Alberini, 2011; Stickgold & Walker, 2007), atunci reconsolidarea excesivă ar putea explica elasticitatea nedumeritoare a credințelor delirante (Simpson & Done, 2002) prin care, atunci când se confruntă cu dovezi incontestabile că iluziile lor nu aparțin, pacienții vor încorpora cu îndemânare aceste informații în iluzia lor, făcând informațiile explicabile și întărind credința (Milton și colab., 1978). Înainte de a ne extinde asupra potențialelor extensii teoretice ale reconsolidării, prezentăm câteva dintre descoperirile preclinice cu potențial de traducere în psihiatrie.
Manual de recunoaștere a noutăților obiectelor
Nick van Goethem,. Jos Prickaerts, în Handbook of Behavioral Neuroscience, 2018
8.3 Lobul temporal medial versus cortexul prefrontal
Influențe culturale asupra dezvoltării memoriei și cunoașterii copiilor
3.1 Codificarea memoriei
FIG. 3. Un exemplu al sarcinii de iluzie Ebbinghaus. . În experimentul lui Imada și al colegilor, au variat dimensiunea cercului țintă potrivit pe parcursul procesului.
Această figură a fost creată pe baza figurii din Imada, T., Carlson, S. M. și Itakura, S. (2013). Diferențele culturale est-vest în sensibilitatea la context sunt evidente în copilăria timpurie. Știința dezvoltării, 16 (2), 198-208. doi: 10.1111/desc.12016.
Neuroștiința cognitivă a somnului
Gina R. Poe,. Theresa E. Bjorness, în progres în cercetarea creierului, 2010
Hipocampus pentru învățarea asociativă și consolidarea memoriei
Structura de codificare rapidă a hipocampului este locul în care a fost descoperit elementul de bază pentru codificarea memoriei, potențarea pe termen lung (LTP) (Bliss și Lomo, 1973). Consolidarea memoriei este transferul acestei plasticități hipocampice către site-uri de stocare pe termen lung mai permanente distribuite pe tot neocortexul. LTP necesită depolarizarea membranei postsinaptice coincidentă cu potențialele de acțiune presinaptice pentru a permite cascada intracelulară de evenimente moleculare, care crește efectul pe termen lung al puterii sinaptice. LTP este ușor indus în timpul stării de veghe și a somnului REM în hipocamp (Bramham și Silver, 1989).
Modele computaționale și de proces de luare a deciziilor în psihologie și economie comportamentală
Eric J. Johnson, Roger Ratcliff, în Neuroeconomie (ediția a doua), 2014
Componenta nedecizie
În afara acumulării de dovezi captate de particula în derivă, există alte procese, cum ar fi codificarea stimulului, accesul la memorie și procesele de mișcare care produc răspunsul comportamental al subiectului. Există, de asemenea, procesul de transformare a reprezentării stimulului într-o variabilă legată de decizie care conduce procesul decizional. Aceste componente ale procesării necesită timp care nu este captat direct de model și sunt combinate într-o componentă „nedecisională” care are o durată medie de Ter. Timpul total de procesare pentru o decizie este astfel luat ca fiind suma timpului luat de procesul decizional și timpul luat de componenta nedecizie.
Hipocampul, memoria și conștiința
Concluzii
Înțelegerea traumei psihologice și a tulburării de stres posttraumatic (PTSD)
Julian D. Ford,. Christine A. Courtois, în Tulburarea de stres posttraumatică (ediția a doua), 2015
Înțelegerea traumei psihologice și a tulburării de stres posttraumatic (PTSD)
- Agricultura insectelor - o prezentare generală Subiecte ScienceDirect
- MacConkey Agar - o prezentare generală a subiectelor ScienceDirect
- Maltodextrina - o prezentare generală a subiectelor ScienceDirect
- Lactobacillus - o prezentare generală Subiecte ScienceDirect
- Stomatita herpetică - o prezentare generală Subiecte ScienceDirect