Fabiana Valadares
Departamentul Clinica de Nutriție - Universitatea din Brasilia-DF, Brazilia
Maria Rita Carvalho Garbi Novaes
1 Departamento de Farmacologia- Facultatea de Medicină Institutul de Științe ale Sănătății-ESCS, Universitatea din Brasilia, Brazilia
Roberto Cañete
2 Departamentul de Parazitologie - Centrul de Igienă, Epidemiologie și Microbiologie-Matanzas și Institutul Cuban de Gastroenterologie-Orașul Havanei, Cuba
Abstract
Fundal:
Cancerul de sân (BC) reprezintă cea mai mare incidență a malignității la femeile din întreaga lume. Ciupercile medicinale pot stimula organismul, pot reduce efectele secundare asociate chimioterapiei și pot îmbunătăți calitatea vieții la pacienții cu cancer.
Pentru a evalua efectele suplimentării dietetice cu Agaricus sylvaticus asupra parametrilor clinici și nutriționali la pacienții BC care urmează chimioterapie.
Materiale și metode:
Un studiu clinic randomizat, controlat cu placebo, dublu-orb, a fost efectuat la clinica de oncologie, spitalul din districtul federal-Brazilia din septembrie 2007 până în iulie 2009. Patruzeci și șase de pacienți cu BC, Stadiul II și III, au fost repartizați aleatoriu la primiți fie supliment nutritiv cu A. sylvaticus (2,1 g/zi), fie placebo. Pacienții au fost evaluați în timpul perioadei de tratament.
Rezultate:
Pacientul suplimentat cu A. sylvaticus a îmbunătățit parametrii clinici și funcțiile gastro-intestinale. Apetitul slab a scăzut cu 20%, fără modificări ale funcțiilor intestinului (92,8%), greață și vărsături (80%).
Concluzie:
Suplimentarea alimentară cu A. sylvaticus a îmbunătățit starea nutrițională și a redus funcțiile anormale ale intestinului, greață, vărsături și anorexie la pacienții cu BC care primesc chimioterapie.
Introducere
Cancerul de sân (BC) reprezintă cea mai mare incidență a malignității la femeile din întreaga lume. [1] Ministerul Sănătății din Brazilia estimează o creștere a incidenței cu peste 49.000 de cazuri noi în următorii 5 ani. [2] Au fost efectuate diferite studii pentru a identifica factorii de risc asociați cu BC. Unii dintre ei sunt factori de risc bine stabiliți, cum ar fi menarche timpurie, paritate și prima sarcină peste 30 de ani, utilizarea contraceptivelor orale, menopauză târzie și terapia de substituție hormonală. Deși s-a raportat că alăptarea, activitatea fizică și obiceiurile alimentare sănătoase cu menținerea greutății corporale pot reduce riscul de BC. [3,4] A fost sugerată și o relație între dietă și cancer, precum și alte boli cronice netransmisibile. [ 1]
Efectele secundare induse de medicamentele împotriva cancerului pot reduce aportul caloric și pot reduce absorbția nutrienților. Terapiile adjuvante, cum ar fi suplimentarea alimentară cu Agaricus sylvaticus, ar putea fi utile pentru a depăși aceste efecte secundare [1,5,6] și scopul acestui studiu a fost de a evalua efectele suplimentării dietetice cu A. sylvaticus asupra stării clinice și nutriționale.
Materiale și metode
Un studiu randomizat, dublu-orb, controlat cu placebo, a fost efectuat la clinica de oncologie, spitalul din districtul federal-Brazilia din septembrie 2007 până în iulie 2009. Protocolul de studiu a fost aprobat de Comitetul de etică al Ministerului Sănătății al Federal District, conform protocolului nr. 041/2007. Consimțământul informat scris a fost obținut de la pacienții incluși în studiu.
Proiectare experimentală
Se extrage cu A. sylvaticus
A. sylvaticus al cărui nume popular este Cogumelo do Sol (Ciuperca Soarelui) a fost obținut de la un producător acreditat de Empresa Brasileira de Agropecuária-Embrapa, din regiunea Tapiraí, statul São Paulo. Extractul de ciupercă a fost obținut prin înmuierea materialului uscat în apă fierbinte timp de 30 de minute, lichidat, cernut și uscat într-un disector. Analiza compoziției A. sylvaticus a fost realizată de Japan Food Research Laboratories Center și a relevat prezența carbohidraților (18,51 g/100 g), lipidelor (0,04 g/100 g), ergosterol (624 mg/100 g), proteine (4,99 g/100 g), aminoacizi (arginină - 1, 14%, lizină - 1, 23%, histidină - 0, 51%, fenilalanină - 0, 92%, tirozină - 0, 67%, leucină - 1, 43% - metionină 0,32%, valină - 1, 03%, alanină - 1, 28% glicină - 0, 94% prolină - 0, 95%, acid glutamic - 3, 93%, serină - 0, 96%, treonină 0,96%, acid aspartic - 1, 81%, triptofan - 0, 32%, cisteină - 0, 25%) și micronutrienți în cantități necuantificate.
Ciuperca a fost administrată în pastile la doza de 2,1 g, împărțită în două administrări zilnice. Pacienții cărora li s-au administrat tablete placebo au primit aceleași cantități, cu aceleași ingrediente și calorii, dar fără extractul de A. sylvaticus. Toți pacienții au ingerat șase comprimate pe zi (trei dimineața și trei după-amiaza între mese) pentru o perioadă de 6 luni.
Înscrierea și selectarea subiectului
Patruzeci și șase de femei cu BC care au primit chimioterapie au fost selectate în conformitate cu criteriile de includere: (1) pacienți cu BC, (2) cu vârste cuprinse între 40 și 65 de ani și (3) în stadiul II sau III care primesc chimioterapie. La început pacienții au fost împărțiți în funcție de ciclurile de chimioterapie prescrise de personalul medical, 26 de femei cu trei cicluri și 20 de femei cu șase cicluri. Dintre femeile cu trei cicluri de chimioterapie, 14 au fost diagnosticate în stadiul II și 12 în stadiul III al bolii. Dintre pacienții cu 6 cicluri de chimioterapie, 10 au fost în stadiul II și 10 în stadiul III al bolii.
Pacienții au fost separați aleatoriu în grupul placebo ([grup de 3 cicluri, n = 13], [grup de 6 cicluri, n = 10]) și suplimentați cu A. sylvaticus (grup [3 cicluri, n = 13], [grup de șase cicluri, n = 10]). Toți pacienții au fost tratați cu medicația lor de bază pentru BC (ciclofosfamidă, metotrexat, fluorouracil) sau (fluorouracil, adriblastină, ciclofosfamidă) în cicluri de 21 de zile, conform recomandărilor liniilor directoare braziliene și urmate de oncologii responsabili în fiecare caz.
Datele au fost stocate și procesate de programul de calculator EpiInfo 6.04. Nici investigatorii, nici pacienții nu au avut informații despre medicamentul utilizat pe tot parcursul studiului. Adulții care (a) erau eligibili, (b) îndeplineau toate criteriile de includere și (c) își acordaseră consimțământul în scris pentru proces, au fost incluși în studiu. A fost elaborat un tabel aleator pentru a aloca (orbește) fiecare dintre acești 46 de pacienți pentru a primi fie A. sylvaticus, fie placebo. Medicamentul a fost furnizat gratuit. S-a calculat dimensiunea eșantionului pentru fiecare grup de tratament (n) necesar pentru a asigura o putere statistică suficientă (80%), un nivel de încredere de 90% și un raport de șanse = 7.
Un formular standard de la fiecare pacient a fost completat pentru a colecta toate informațiile legate de proces. Formularul a fost aplicat în prima zi de consultare și în programările ulterioare. Datele colectate au fost efectuate de cercetători instruiți. Caracteristicile populației studiate, socioeconomice (venitul familiei, locul de reședință, rasa, starea civilă, educație), stilul de viață (fumatul, consumul de alcool și inactivitatea fizică) și informații cu privire la numărul de sarcini și durata alăptării la primul născut a fost obținut. Pacienții au fost urmăriți timp de 3-6 luni și evaluați la fiecare 30 de zile sau la fiecare ciclu de chimioterapie. Pacienții au fost rugați să mențină o dietă normală. Evaluarea siguranței a fost efectuată printr-un chestionar standardizat.
Evenimentul advers a fost definit ca dezvoltarea oricărui semn sau simptom care nu exista înainte sau a devenit mai grav după începerea tratamentului. Evenimentele adverse grave au fost definite ca moarte, orice evenimente care pun viața în pericol, invalidante sau incapacitante sau cele care necesită spitalizare.
Evaluarea conformității
Una dintre următoarele cerințe a fost luată în considerare pentru a indica tratamentul de neconformitate: (1) neparticiparea la vizitele de urmărire; (2) să nu luați una sau mai multe doze la nivelul și durata indicată; (3) a întrerupt medicamentul fără să întrebe medicul curant.
Managementul datelor și analiza statistică
Datele privind răspunsul la tratament și evenimentele adverse au fost notate pe formulare de înregistrare prestabilite și ulterior analizate pentru a determina frecvența fiecărui răspuns/efect utilizând software-ul EpiInfo 6.04 (Public Health Domain Software, CDC, Atlanta, GA, SUA). Semnificația statistică a diferențelor dintre valorile medii a fost determinată folosind testul t Student. Testul exact Fisher a fost utilizat pentru a stabili semnificația diferențelor de proporții. Pd ”0,05 a fost considerat semnificativ statistic.
Rezultate
După urmărire, 46 de femei cu BC au finalizat studiul, 26 (56,5%) în grupul celor trei cicluri de chimioterapie și 20 (43,4%) în șase cicluri de chimioterapie. Dintre acești pacienți, 23 (50%) au primit placebo, iar ceilalți au primit A. sylvaticus. Pacienții din grupul placebo (n = 23) au avut o vârstă medie de 49,5 ani, în timp ce în grupul suplimentat cu A. sylvaticus (n = 23), vârsta medie a fost de 52,7 ani. Grupul placebo de pacienți aparținea stadiului II, în timp ce grupul suplimentat se afla în stadiul III al bolii [Tabelul 1].
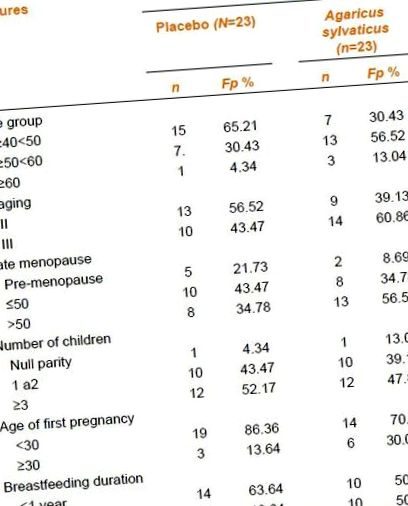
tabelul 1
Date generale despre pacienții cu cancer de sân
Menopauza, la pacienții suplimentați, a fost de 50 de ani, în timp ce grupul placebo a avut menopauză târzie. În grupul suplimentat, trei pacienți au fost nulipari, în timp ce în grupul placebo a fost un singur pacient [Tabelul 1]. Majoritatea femeilor au avut prima sarcină înainte de vârsta de 30 de ani, 86,36% (n = 19) în grupul placebo și 70,0% în grupul suplimentat [Tabelul 2].
masa 2
Caracteristicile socio-demografice și obiceiurile de viață ale pacienților cu cancer de sân
Doisprezece pacienți nu au fumat niciodată în grupul suplimentat și placebo. Toți pacienții au raportat că nu consumă alcool [Tabelul 2]. Analiza datelor despre activitatea fizică a relevat că majoritatea (82,61% [n = 19]) dintre pacienții din grupul placebo și din grupul suplimentat au fost sedentari [Tabelul 2].
Ambele grupuri au fost analizate separat în funcție de ciclurile de chimioterapie și de tipul de supliment care caută simptome gastro-intestinale. După 3 luni de chimioterapie, 4 pacienți (30,77%) din grupul placebo au prezentat pierderea poftei de mâncare, în timp ce pacienții tratați suplimentat cu A. sylvaticus nu s-au plâns de anorexie [Tabelul 3]. Un număr bun de pacienți din grupul placebo au prezentat plângeri de diaree sau constipație, în timp ce 92,31% (n = 12) dintre pacienții suplimentați cu ciuperci nu au avut astfel de modificări.
Tabelul 3
Simptome clinice și gastro-intestinale ale pacienților cu cancer de sân care au primit trei cicluri de chimioterapie
Doar 2 (15,3%) pacienți tratați cu A. sylvaticus au raportat greață și vărsături, în timp ce majoritatea pacienților 11 (84,62%) din grupul placebo au notificat greață și vărsături. Doar 7,69% (n = 1) dintre pacienții suplimentați au avut febră în primele 10 zile după chimioterapie, cu toate acestea 23,08% (n = 3) dintre pacienții cu placebo au raportat astfel de reclamații.
Pacienții cu șase cicluri de chimioterapie au arătat că 60% (6) dintre pacienții din grupul placebo s-au plâns de pierderea poftei de mâncare. La finalizarea tratamentului, 80% (n = 8) dintre pacienți au raportat reducerea poftei de mâncare.
În timp ce 6 luni cu tratament medicamentos funcțiile intestinului nu au fost afectate. Cu toate acestea, 80% (n = 8) dintre pacienții din grupul placebo au prezentat tulburări ale funcției intestinale. În ceea ce privește greața și vărsăturile, la finalizarea tratamentului după 6 luni de tratament, la pacienții suplimentați doar 20% (2) au raportat greață și 10% (1) vărsături, în timp ce 100% (10) și 70% (7) din grupul placebo au raportat greață sau vărsături, respectiv [Tabelul 4].
Tabelul 4
Simptome clinice și gastro-intestinale ale pacienților cu cancer de sân care au primit șase cicluri de chimioterapie
După 6 luni, 70% (n = 7) dintre pacienții cu placebo au raportat febră, în timp ce nu a fost raportată febră de la pacienții suplimentați cu A. sylvaticus [Tabelul 4].
Evaluarea nutrițională a fost efectuată utilizând: parametri de greutate, indicele de masă corporală (IMC), raportul talie-șold (W/HR), adecvarea procentului tricepsului și suma pliului pielii (triceps skinfold [TSF]). Pentru analiza statistică, testul t a fost efectuat pentru probele asociate [Tabelul 5].
Tabelul 5
Parametrii nutriționali ai pacienților cu cancer mamar supuși a trei sau șase cicluri de chimioterapie cu supliment alimentar Agaricus sylvaticus
A existat o diferență semnificativă de parametri atunci când se compară prima și a treia lună de tratament cu procentul adecvat de triceps și suma cutelor cutanate (TSF). În ceea ce privește IMC și W/HR, indiferent de tipul de tratament, pacienții au fost clasificați ca fiind supraponderali și au risc cardiovascular datorită acumulării de grăsime viscerală.
Discuţie
Mai multe studii au raportat că pacienții aflați într-o uniune conjugală stabilă au șanse mai mari de recuperare și îmbunătățesc calitatea vieții în timpul tratamentului. [10,12] Acest studiu a constatat o prevalență mai mare a femeilor căsătorite în ambele grupuri, 65,21% și respectiv 52,17%. În ambele grupuri, femeile au avut venituri până la salariul minim lunar. Unele studii efectuate în spitalele unificate ale sistemului de sănătate din Brazilia au raportat venitul familial scăzut ca factor de risc pentru BC, în principal în cazurile de diagnostic tardiv. [1,12,13]
O dietă sănătoasă este esențială în toate etapele. [1,3] Pacienții cu trei cicluri de chimioterapie la momentul inițial au raportat apetit slab, prin care 23,08% dintre acești pacienți au fost în grupul placebo, iar 53,85% dintre acești pacienți au fost în grupul cu A. sylvaticus . După 3 luni, 30,77% dintre pacienții din grupul placebo au raportat o scădere a poftei de mâncare, în timp ce în grupul suplimentat nu au existat astfel de reclamații. Comparativ cu pacienții cu șase cicluri de chimioterapie și utilizarea mai îndelungată a ciupercilor A. sylvaticus, datele arată că spre sfârșitul tratamentului, reclamațiile privind pierderea poftei de mâncare s-au redus în timp, spre deosebire de cele din grupul placebo, care după 6 luni de tratament au arătat 80% din acești pacienți cu plângeri de apetit slab. Aceste date relevă potențialele efecte bioactive ale suplimentării cu A. sylvaticus.
Diferite studii au arătat că utilizarea ciupercilor medicinale ca terapie adjuvantă în tratamentul afecțiunilor maligne este capabilă să promoveze îmbunătățirea semnificativă a poftei de mâncare, să reducă oboseala și să stabilizeze astfel parametrii hematologici și imunologici, îmbunătățind bunăstarea acestor pacienți. [1, 14,15] Principala substanță găsită în ciuperci care are acțiune funcțională medicinală este â-Glucanul și are o cantitate mare de alte fibre dietetice; posibilele beneficii cauzate de aceste ciuperci în funcția intestinului se pot datora fibrelor conținute în compoziția lor. â-Glucanul acționează în corpul uman prin creșterea funcțiilor imune, stimulând celulele ucigașe naturale, limfocitele T, limfocitele B și celulele complementare; prin creșterea numărului și funcției macrofagelor și monocitelor, promovarea proliferării și/sau producției de anticorpi și diverse citokine precum IL -2 și IL-6, astfel încât să se evite metastaza cancerului. [14,16]
Studiile întăresc rolul esențial al fibrelor dietetice asupra metabolismului intestinal datorită concentrațiilor crescute de SCFA, care acționează și asupra integrității celulelor colonice intensificând reabsorbția sodiului și a apei, luând o importanță crucială pentru cazurile diareice. [1,3]
Datele referitoare la starea nutrițională a pacienților diagnosticați cu BC găsite în literatură legitimează datele găsite în acest studiu. [17,18] Literatura arată că majoritatea pacienților cu BC au un profil nutrițional de supraponderalitate și obezitate. Pacienții cu trei cicluri de chimioterapie au început tratamentul cu un IMC mediu de 26,53 ± 4,65 kg/m2 și o greutate medie de 67,93 ± 11,61 kg. Pacienții cu șase cicluri de chimioterapie au avut o greutate medie de 66,60 ± 9,44 kg și IMC 27,21 ± 3,68 kg/m 2. IMC este parametrul nutrițional cel mai utilizat pentru clasificarea profilului nutrițional. Cu toate acestea, acesta este un fapt care izolat nu raportează starea nutrițională reală a pacienților. Friedenreich a legat obezitatea, creșterea necontrolată în greutate, IMC ridicat și W/HR la riscul BC și în principal la un prognostic slab al bolii, cu șanse mai mari de recurență pentru astfel de pacienți. [19] Kim, într-un studiu cu 833 de femei, a găsit o asociere puternică între IMC ridicat și diagnosticul BC în stadionul egal sau mai mare decât II al bolii. [20]
Studiile epidemiologice utilizează relația W/HR și circumferința taliei (WC) pentru evaluarea distribuției grăsimii corporale. Printre punctele limită stabilite pentru a discrimina valorile adecvate de cele inadecvate în ceea ce privește W/HR, cel mai utilizat a fost 0,85 pentru femei. Cu toate acestea, Pereira și colab., [21] într-un studiu bazat pe populație efectuat în Rio de Janeiro, a arătat că utilizarea punctului de tăiere de 0,80 pentru femei avea o asociere mai bună cu predicția bolilor legate de obezitate.
Ronco a găsit femei diagnosticate cu BC cu valori ridicate ale pliurilor cutanate și WC (93,12 ± 14,12). El a menționat, de asemenea, că valorile TSF erau strâns legate de riscul BC, cu o valoare P de 0,0004. [4] Analiza datelor privind WC, W/HR,% grăsime corporală și adecvarea procentului de piele triceps în acest studiu au fost cu mult peste limitele normale, relevând că aproape întreaga populație din studiu deține riscul bolilor asociate obezității, cum ar fi BC.
Studiile clinice au arătat că suplimentele precum A. sylvaticus (Cogumelo do Sol) sunt capabile să reducă efectele secundare ale medicamentelor anticanceroase, să îmbunătățească funcția intestinului, să susțină starea nutrițională, să stimuleze sistemul imunitar și hematologic și să îmbunătățească calitatea vieții de pacienți cu cancer. [1,5,6]
Concluzie
Suplimentarea alimentară cu A. sylvaticus a îmbunătățit starea nutrițională și a redus reacțiile adverse la medicamente în funcțiile intestinului, greață, vărsături, anorexie și febră la pacienții cu BC tratați cu chimioterapie.
- Evaluarea efectului suplimentării orale cu taurină asupra nivelurilor de post ale creșterii fibroblastelor
- Efectele suplimentării cu pulbere de ghimbir asupra stării glicemice și a profilului lipidic la pacienții cu tip
- Efectul suplimentării cu aminoacizi cu lanț ramificat asupra recuperării după exerciții excentrice acute
- Cafeaua slăbitoare mAi Dark Mocha chiar funcționează Jessy The KL Chic - Malaezia Food, Fashion, Events
- GUAM Cele mai bune creme anticelulitice cu alge marine, efect de slăbire; Etichetat; preț crescător