Massimo Conese
1 Centrul de cercetare biomedicală „E. Altomare ”, Laboratorul de Medicină Experimentală și Regenerativă, Departamentul de Științe Medicale și Chirurgice, Universitatea din Foggia, c/o Ospedali Riuniti, Via L. Pinto 1, 71122, Tel.: +39 0881 588014; Fax: +39 0881 588047;, Foggia, Italia
Annalucia Carbone
2 Departamentul de Științe Medicale și Chirurgice, Universitatea din Foggia, Foggia, Italia
Elisa Beccia
2 Departamentul de Științe Medicale și Chirurgice, Universitatea din Foggia, Foggia, Italia
3 Departamentul de Medicină și Știința Sănătății „V. Tiberio ”, Universitatea Molise, Campobasso, Italia
Antonella Angiolillo
3 Departamentul de Medicină și Știința Sănătății „V. Tiberio ”, Universitatea Molise, Campobasso, Italia
Abstract
1. Introducere
În secolul al XVI-lea, celebrul explorator și cuceritor spaniol Juan Ponce de León a condus expediția în jurul insulelor din Caraibe și în cele din urmă în Florida pentru a găsi Fântâna Tineretului, o sursă magică de apă presupusă capabilă să inverseze procesul de îmbătrânire și să vindece boala [1] . Deși exploratorul nu a menționat Fântâna Tineretului în scrisorile sale, conduse de zvonuri, expediția a continuat căutarea și mulți au pierit. Fântâna nu se găsea nicăieri, deoarece localnicii nu erau conștienți de locația sa exactă. Fontaneda a scris în memoriile sale: „Cu atât de mult s-au angajat în urmărire, încât nu a rămas nici un râu și nici un pârâu în toată Florida, nici măcar lacuri și iazuri, în care nu se scăldau; și până astăzi persistă în căutarea acelei ape și niciodată nu sunt mulțumiți. […]… Și s-a încheiat cu atât de mulți oameni care s-au dus la Carlos formând o așezare: dar până în zilele noastre tinerii și vârsta găsesc la fel că sunt batjocoriți și mulți s-au distrus ”.
Acesta este doar un exemplu de căutare continuă pe care oamenii au dedicat-o găsirii unei modalități de a trăi pentru totdeauna. Interesant este că o altă abordare frecvent citată pentru întinerire a fost încercarea de a transfera căldura și fluidele tinerilor de la tineri la bătrâni. Câteva exemple ale acestei abordări au fost culcarea cu fecioare, o practică prescrisă și de medicii științifici în secolele 17 și 18 [2], sau scăldatul sau băutul de sânge [3].
Sângele, plasma și derivații lor sunt ceea ce medicina modernă a produs pentru a ajuta la funcționarea celulelor stem și la regenerarea și repararea țesuturilor. Derivații din sânge bogate în trombocite, cum ar fi plasma bogată în trombocite (PRP) și fibrina bogată în trombocite, produc și furnizează factori de creștere cu proprietăți antiapoptotice și angiogene, sporind capacitatea regenerativă a celulelor stem și progenitoare, fie rezidente local, fie administrate exogen [4] ]. PRP a devenit popular pentru utilizarea în diverse proceduri chirurgicale ortopedice pentru tratarea diferitelor afecțiuni, inclusiv osteoartrita [5, 6], în chirurgia plastică pentru îmbunătățirea supraviețuirii grefei [7, 8] și pentru tratarea necrozei cutanate iminente [9]. Astfel, nu există nicio îndoială că sângele și derivații pot fi folosiți cu succes în strategiile medicinei regenerative, dar chiar și pentru „sfântul graal” al întineririi - inversarea procesului de îmbătrânire.
2. O poveste de parabioză
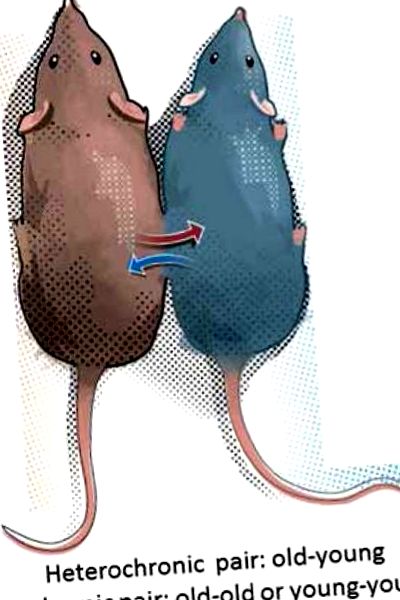
Parabioză. Doi șoareci sunt cusuti împreună împărtășind un flux sanguin comun. Parabioza heterocronică este atunci când un șoarece tânăr este legat chirurgical de partenerii în vârstă, în timp ce parabioza izocronică se referă la perechi de animale tinere-tinere sau bătrâne. Modificat din ref. [36] cu permisiunea Nature Publishing Group.
Îmbătrânirea mușchilor, ficatului și creierului la șoareci bătrâni și întinerire prin parabioză heterocronică. Regenerarea mușchiului scheletic la rănire este legată de reglarea în sus a ligandului Notch Delta, care se pierde odată cu vârsta (panourile superioare). Proliferarea hepatocitelor la animalele tinere se corelează cu scăderea complexului cEBP-α-brahma (cEBP-α-Brm) în comparație cu șoarecii în vârstă (panourile medii). În timp ce animalele tinere își pot crește neurogeneza și angiogeneza în zona subventriculară a creierului, unde sunt prezente celule stem neuronale, animalele în vârstă nu pot (panouri inferioare). În principiu, parabioza heterochonică revine la toate caracteristicile fenotipice și moleculare ale îmbătrânirii prin transferarea factorilor solubili și a celulelor.
Pentru a înțelege care factor este implicat în reglarea funcției celulelor de nișă, autorii au căutat să investigheze dacă factorul de creștere asemănător insulinei (IGF-1) ar putea juca un rol. IGF-1 s-a dovedit a fi un regulator de îmbătrânire și longevitate conservat evolutiv [24]. Experimentele in vitro și in vivo au demonstrat că IGF-1 local, nu sistemic, pare să inducă îmbătrânirea celulelor de nișă de reglementare HSC și că neutralizarea semnalizării IGF-1 în microambientul măduvei osoase revine la modificările legate de vârstă ale celulelor de nișă osteoblastice care afectează reglementarea corespunzătoare a HSC-urilor.
În general, aceste constatări au sugerat că, în timp ce în condiții tinere celulele de nișă osteoblastice promovează întreținerea celulelor stem homeostatice, acestea sunt modificate prin îmbătrânire astfel încât, în schimb, să permită acumularea sporită de HSC disfuncționale. Aceste modificări specifice vârstei în celulele de nișă par a fi semnalate de un factor circulant necaracterizat care acționează parțial prin modificarea semnalizării IGF-1 în celula de nișă (Fig. 3). Este probabil ca IGF-1 să nu aibă un rol major pentru toate țesuturile în vârstă, deoarece, în timp ce rolul său în nișa osteoblastică promovează vârsta, spre deosebire de expresia locală a mușchilor scheletici a IGF-1 menține capacitatea regenerativă la animalele în vârstă.
Model propus care descrie modificările legate de vârstă în nișa celulară osteoblastică și HSC și modul în care aceste modificări pot fi inversate prin parabioză heterocronică. Modificările specifice vârstei în efectele autocrine sau paracrine ale IGF-1 asupra celulelor de nișă osteoblastice sunt semnalate de factori solubili circulanți care se modifică ei înșiși odată cu vârsta. Semnalizarea IGF-1 în celule de nișă osteoblastice în vârstă (A) contribuie direct la disfuncția legată de vârstă în HSC, incluzând supraacumularea HSC și alegerea destinului limfoid B (celule B)/mieloid (My). După parabioză heterocronică sau după neutralizarea in vivo a semnalizării IGF-1 (b), activitatea „tinerească” a celulelor de nișă în vârstă este restabilită, astfel încât acestea să nu mai inducă supraacumulare sau distorsionarea descendenței HSC-urilor. Din ref. [11] cu permisiunea Nature Publishing Group.
În octombrie 2010, trei dintre cei patru autori, inclusiv Amy J. Wagers, au retras această lucrare, în special pentru rolul celulelor de nișă osteoblastice în întinerirea HSC la șoarecii în vârstă [25]. S-a constatat că primul autor a manipulat imaginile pentru nodulii osoși formați în celule de nișă osteoblastice de la șoareci tineri și vârstnici (Retraction Watch, http://retractionwatch.com/2012/08/29/ori-finds-harvard-stem-cell -lab-post-doc-mayack-images-manipulate /). Astfel, ar trebui obținută o confirmare suplimentară a problemei sale, având în vedere că modelul parabiozei a fost exploatat pentru studierea întineririi altor organe vechi. Într-adevăr, au apărut ulterior două lucrări care arată că expunerea unui șoarece la un mediu sistemic vechi poate inhiba miogeneza [26] și neurogeneza [27].
În cealaltă lucrare de Wagers și colegi [30], s-a demonstrat că celulele satelit sortate de la șoareci vârstnici-heterocronici au îmbunătățit capacitatea de diferențiere miogenică, precum și leziuni mai mici ale ADN-ului în comparație cu celulele satelit de la controalele izochronice în vârstă. În ceea ce privește reversia hipertrofiei cardiace legate de vârstă [28], tratamentul șoarecilor în vârstă cu injecții intraperitoneale zilnice de GDF11 recombinant timp de 4 săptămâni a crescut numărul de celule satelit cu ADN intact, comparativ cu celulele de la șoareci în vârstă care primeau vehicul singur. Mai mult, într-un model de leziune musculară, tratamentul GDF11 al șoarecilor în vârstă cu 28 de zile înainte de rănire și continuat timp de 7 zile după aceea a restabilit mai multe tinere profiluri de calibru miofiber în mușchiul regenerant. Șoarecii în vârstă tratați cu GDF11 au arătat, de asemenea, rezistență medie crescută la exerciții și rezistență la aderență.
În această ultimă lucrare, au descoperit, de asemenea, că expunerea in vitro a celulelor satelit în vârstă la GDF11, dar nu miostatina (un alt membru al superfamiliei TGF-β) sau TGF-β1, a produs creșteri receptive la doză în proliferarea și diferențierea celulelor satelite, sugerând că GDF11, spre deosebire de miostatină, poate acționa direct asupra celulelor satelit pentru a le modifica funcția.
3. O poveste de surpriză și droguri noi
Deși la prima vedere datele generate de Egerman și colegii păreau să intre în conflict cu rezultatele echipei Amy Wagers, ar putea exista mai multe forme de GDF11 și doar una ar putea scădea odată cu vârsta, așa cum a raportat The Scientist într-o corespondență prin e-mail cu Amy Wagers [ 33]. Mai mult, grupul Novartis a rănit mușchiul mai mult și apoi l-a tratat cu mai mult GDF11 decât a făcut grupul Wagers, astfel încât rezultatele nu pot fi direct comparabile (echipa Novartis a folosit animale tinere și o doză de GDF11 de trei ori mai mare). Faptul este că rezultatele publicate de Egerman și colegii ar putea ajuta la explicarea mecanismului din spatele bimagrumabului, un tratament experimental Novartis pentru slăbiciune și irosire musculară [34]. Medicamentul, care se află în prezent în studii clinice, blochează miostatina - și poate și GDF11 [35].
Pe scurt, nu se îndoiește că sângele tânăr reînnoiește șoarecii bătrâni, dar echipa Novartis spune că explicația grupului Harvard este greșită. Probabil adevărul rămâne la mijloc și menținerea nivelurilor GDF11 într-un interval fiziologic adecvat ar fi esențială pentru sănătatea musculară. De asemenea, este important să ne amintim de ceea ce a spus Amy Wagers: „Nu suntem animale care dezinvechim. Restabilim funcția țesuturilor ”[36]. Alternativ, alți factori pot acționa în acest context. În 2014, Irina și Michael Conboy au identificat [37] unul dintre factorii anti-îmbătrânire care circulă în sânge: oxitocina, o nonapeptidă produsă de hipotalamus, care este implicată în naștere și legare. Ei au observat că nivelurile de oxitocină au scăzut la șoarecii bătrâni (18-24 luni) și, atunci când au fost injectate subcutanat la șoareci în vârstă, oxitocina a recuperat capacitatea de regenerare a celulelor musculare după leziunea cardiotoxinei.
4. Pro și contra ale sângelui integral față de factori specifici
5. Concluzii
Aceasta este o poveste despre căutarea îndelungată de către ființele umane a „fântânii tinereții”. Parabioza a sugerat pe o perioadă lungă de timp că factorii din sângele tânăr pot ajuta la regenerarea țesuturilor bolnave sau în vârstă. Unii ar prefera să administreze sânge integral sau derivații săi, cum ar fi plasma, în timp ce alții sunt mai asemănători cu livrarea unor factori specifici sau cocktailuri de factori. Cel mai bun scenariu ar fi utilizarea citokinelor plasmatice sau derivate din trombocite ale pacientului și a factorilor de creștere pentru a stimula vindecarea rănilor și regenerarea țesuturilor. Unele sugestii apar din studiile pe animale, dar legătura cu oamenii este încă de găsit.
Note de subsol
Declarație privind conflictul de interese: Autorii nu declară niciun conflict de interese
- Tampa Pierdere în Greutate Vitamină Injecții Tampa întinerire
- Analiza transcriptomului în celulele sanguine de la copii relevă potențiali biomarkeri precoci ai metabolizării
- Tratamentul supraponderalității și obezității la copii și tineri o revizuire sistematică și meta-analiză
- Secretele de top ale sănătății câștigă o sănătate perfectă, pierderea în greutate, întinerire și niveluri crescute de energie
- Top 4 sfaturi pentru pierderea în greutate de sărbători Centrul de întinerire a întregului corp