Abstract
fundal
Conceptul unui punct de referință pentru greutatea corporală, determinat în principal de mecanisme genetice, a fost propus pentru a explica rezultatele slabe pe termen lung ale dietelor convenționale cu restricție energetică în tratamentul obezității.
Obiectiv
Obiectivul acestui studiu a fost de a examina dacă compoziția dietetică afectează adaptările hormonale și metabolice la restricția de energie.
Proiecta
Un design randomizat, încrucișat, a fost utilizat pentru a compara efectele unui indice glicemic ridicat (IG ridicat) și al unui indice glicemic scăzut (IG scăzut) cu restricție energetică. Compoziția macronutrienților din dieta bogată în IG a fost (ca procent de energie) 67% carbohidrați, 15% proteine și 18% grăsimi, iar cea a dietei cu IG scăzută a fost 43% carbohidrați, 27% proteine și 30% grăsimi; dietele aveau energie totală similară, densitate de energie și conținut de fibre. Subiecții, 10 tineri cu greutate moderată, au fost studiați timp de 9 zile în 2 ocazii separate. În zilele −1 la 0, au consumat alimente autoselecționate ad libitum. În zilele 1-6, aceștia au primit o dietă cu conținut ridicat sau scăzut de IG. În zilele 7-8, dietele cu conținut ridicat sau scăzut de IG au fost consumate ad libitum.
Rezultate
Leptina serică a scăzut într-o măsură mai mică din ziua 0 până în ziua 6 cu dieta bogată în IG decât cu dieta cu IG scăzută. Cheltuielile energetice de repaus au scăzut cu 10,5% în timpul dietei bogate în IG, dar cu doar 4,6% în timpul dietei cu IG scăzut (7,38 ± 0,39 și respectiv 7,78 ± 0,36 MJ/zi, în zilele 5-6; P = 0,04). Bilanțul de azot a avut tendința de a fi mai negativ, iar aportul de energie din gustări în zilele 7-8 a fost mai mare, cu un IG ridicat decât dieta cu un IG scăzut.
Concluzie
Dietele cu conținut identic de energie pot avea efecte diferite asupra concentrațiilor de leptină, cheltuielilor de energie, aportului voluntar de alimente și echilibrului de azot, sugerând că adaptările fiziologice la restricția energetică pot fi modificate prin compoziția dietetică.
INTRODUCERE
Greutatea corporală excesivă se numără printre cele mai importante afecțiuni medicale din Statele Unite, cu rate de prevalență de ~ 25% la copii (1) și> 50% la adulți (2). Deși consecințele asupra sănătății și costurile economice ale obezității sunt enorme (3), în prezent nu există un tratament dietetic eficient pentru această problemă (4). O explicație pentru rezultatele slabe pe termen lung ale dietelor convenționale implică conceptul unui punct de referință pentru greutatea corporală (5).
Rezultatele numeroaselor studii sugerează că greutatea corporală este reglementată într-un anumit domeniu. Când subiecții slabi sau obezi stabili în greutate au fost subalimentați pentru a obține o modificare de 7,5-10% a greutății corporale, cheltuielile totale de energie (TEE) au scăzut cu ± 12-15% (5-8). Alte modificări fiziologice induse de restricția energetică includ creșterea foametei și reducerea reglării funcțiilor neuroendocrine (9-12). Aceste adaptări împreună pot acționa pentru a contracara pierderea în greutate. Se știe că factorii genetici influențează intervalul în care greutatea corporală este reglementată (13). Cu toate acestea, prevalența crescândă a obezității în rândul populațiilor stabile genetic (14) indică faptul că mediul trebuie să joace, de asemenea, un rol important în reglarea greutății corporale.
SUBIECTE ȘI METODE
Subiecții au fost bărbați tineri cu o vârstă medie de 27,9 y (interval: -18-34 y) care au fost supraponderali moderat [x ̄ ± indicele de masă corporală SEM (în kg/m 2): 30,6 ± 1,5, interval: 28,7-32,2) . Subiecții au avut o stare bună de sănătate, altfel determinată de examinarea fizică și testele de laborator (hemogramă, hemoglobină glicozilată, funcția tiroidiană și funcția hepatică). Toți subiecții au fost grei stabili (în limita a 5% din greutatea corporală actuală în ultimii 6 luni, prin auto-raportare). Am recrutat subiecți prin publicitate prin ziare locale, pliante și radio. Zece subiecți au finalizat cu succes protocolul; un subiect a renunțat la studiu și datele sale nu au fost incluse în rezultate. Cercetarea a fost realizată în Centrul General de Cercetare Clinică (GCRC), Spitalul pentru Copii, Boston, cu aprobarea Comitetului de revizuire instituțională și consimțământul scris, informat de la subiecți.
Protocolul experimental a urmat un design aleatoriu, încrucișat, care implică două admisii de 9 zile la GCRC, separate printr-o perioadă de spălare de 2-6 săptămâni. În primele 2 zile ale fiecărei admiteri (ziua -1 și ziua 0), subiecții au consumat o dietă auto-selectată ad libitum și s-au obținut măsurători de bază. În următoarele 6 zile (zilele 1-6), subiecții au consumat fie o dietă de testare cu conținut ridicat de IG, fie o dietă cu conținut redus de IG. În zilele 7 și 8, subiecții au continuat să mănânce diete cu conținut ridicat sau scăzut de IG, dar li s-a permis să mănânce alimente suplimentare ad libitum dintr-un bar privat. Studiul a fost încheiat la cină în ziua 8, permițând un total de 34 de ore pentru consumul alimentar ad libitum. Subiecții au fost obligați să facă exerciții zilnice pe o bandă de alergat până când 10% din TEE a fost atins. TEE a fost determinat pentru fiecare subiect prin ecuația Harris-Benedict înmulțită cu un factor de activitate de 1,4 (28). Înainte și între admiterile la GCRC, subiecții au fost instruiți să urmeze dieta obișnuită și tiparele de exerciții fizice și să evite cafeina, alcoolul și produsele din tutun.
Cheltuielile de energie în repaus (REE) au fost măsurate prin calorimetrie indirectă în post (Vmax 29; SensorMedics Corporation, Yorba Linda, CA) pentru o durată totală de 20-30 minute, în timp ce subiecții s-au odihnit în pat. Probele de sânge au fost obținute după măsurarea REE și înainte de micul dejun. În plus, probele de sânge au fost obținute în ziua 1 la fiecare 30 de minute prin cateter venos intern pentru măsurarea răspunsurilor la glucoză plasmatică și insulină serică la micul dejun, prânz și cină pentru a verifica diferențele prevăzute în GI (vezi mai jos).
tabelul 1
Unul din cele 2 meniuri alternative pentru dietele cu indice glicemic ridicat (IG ridicat) și cu indice glicemic scăzut (IG scăzut)
| Carbohidrați (% din energie) | 67 | 43 |
| Proteine (% din energie) | 15 | 27 |
| Grăsimi (% din energie) | 18 | 30 |
| Mic dejun | Fulgi de ovăz (fulgi de ovăz instant, lapte 2% -gras cu lactază adăugată, jumătate și jumătate smântână, dextroză, tărâțe de grâu) Banană | Omletă (1 ou întreg, 1 albus de ou, spanac, roșii, brânză cheddar cu conținut scăzut de grăsimi) Măr, cu coajă Pâine cu nichel Jeleu dietetic |
| Masa de pranz | Sandwich de friptură de vită (friptură de vită, rotundă de sus; pâine de grâu; maioneză; salată iceberg; roșii) Stafide Caise uscate Iaurt congelat fără grăsime | Sandwich cu piept de curcan (pâine integrală cu 3 sâmburi, piept de curcan fără piele, maioneză, salată iceberg) Salată (salată iceberg, țelină, castravete, sos italian) Roșii fierte Măr, cu coajă Gelatină fără zahăr |
| Masa de seara | Pui Jambalaya (orez alb cu bob lung, fiert; piept de pui; unt; ardei gras dulce verde; sos de roșii; ceapă tocată) Dovlece de nucă, gătită Tort cu mâncare înger Lapte degresat cu lactază adăugată | File de somon Fasole verde Ardei gras roșu dulce Unt Salată (salată iceberg, castraveți, roșii, sos francez fără grăsimi) Pâine cu nichel Grapefruit |
| Gustare | Sandwich cu jumătate de curcan (pâine de grâu, piept de curcan afumat, maioneză, brânză americană fără grăsimi) Sos de mere, îndulcit | Conserve de piersici în sirop ușor Brânză de vaci din lapte integral Jumătate și jumătate de cremă |
Probele de sânge au fost analizate cu următoarele instrumente sau truse: glucoză plasmatică, Glucose Analyzer (APEC, Inc, Peabody, MA); insulină serică, Abbott IMx (Abbott Laboratories, Abbott Park, IL); și leptina serică, kitul de radioimunotest (Linco Research, Inc., St Charles, MO). Colecțiile de urină de 24 de ore au fost analizate pentru azot total utilizând metoda Kjeldahl (29) și au fost analizate și pentru creatinină pentru a evalua adecvarea colectării. Bilanțul de azot, raportat ca medie a valorilor obținute în zilele 3 și 6, a fost calculat utilizând următoarea ecuație (30):
Zonele sub curbele de glucoză și insulină au fost determinate utilizând regula trapezoidală (software FIGP 2.98; BIOSOFT, Cambridge, Marea Britanie) și efectele dietelor au fost comparate utilizând un test t Student pereche. Modificările leptinei serice în timpul celor 2 diete au fost comparate utilizând analiza măsurilor repetate GLM (SPSS 9.0.0; SPSS Inc, Chicago). Efectele dietei asupra REE la sfârșitul tratamentului (media zilelor 5 și 6) și modificarea REE față de valorile inițiale au fost evaluate utilizând teste t asociate. Rezultatele sunt raportate ca medii (± SEM).
REZULTATE
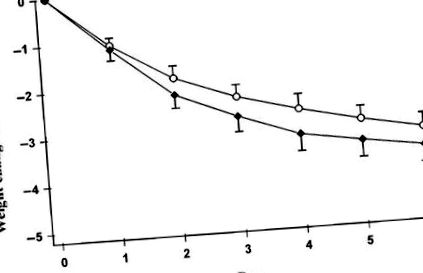
Pierderea în greutate nu a diferit semnificativ între cele 2 diete (3,62 ± 1,14 kg cu dieta cu IG scăzută și 3,23 ± 0,92 kg cu dieta cu IG ridicată), așa cum se arată în Figura 1. Aria medie sub curba de răspuns glicemic a fost de două ori mai mare cu dieta bogată în IG (2,69 ± 0,47 mmol · h/L) ca în dieta cu IG scăzută (1,30 ± 0,19 mmol · h/L; P = 0,001). Suprafața medie sub curba de răspuns insulinemic a fost cu aproape 50% mai mare cu dieta bogată în IG (700 ± 98,4 pmol · h/L) decât cu dieta cu IG scăzută (478 ± 82,2 pmol · h/L; P = 0,01) (Figura 2).
Pierderea medie în greutate (± SEM) de la momentul inițial în timpul a 6 zile de restricție de energie. Greutatea inițială pentru dieta cu indice glicemic ridicat (○) a fost de 98,5 ± 2,7 kg, iar pentru dieta cu indice glicemic scăzut (◆) a fost de 99,2 ± 2,9 kg (NS; n = 10).
Răspunsurile glicemice (A) și insulinemice (B) măsurate la intervale de 0,5 ore. Curbele sunt valori medii (± SEM) după micul dejun, prânz și cină din ziua 1. Coloanele reprezintă aria sub curba concentrație-timp calculată utilizând regula trapezoidală. Glicemia inițială efectivă pentru dieta cu indice glicemic ridicat (IG) ridicat (○) a fost de 5,5 ± 0,2 mmol/L și pentru dieta cu indice glicemic scăzut (IG) scăzut (() a fost de 5,3 ± 0,2 mmol/L (NS; n = 10).
Leptina serică (Figura 3) a scăzut mai rapid și într-o măsură mai mare în timpul dietei cu IG scăzut decât în timpul dietei cu IG ridicat (P = 0,03). În ziua a 6-a, leptina scăzuse cu 50,0 ± 5,5% față de valoarea inițială cu dieta cu IG scăzută, comparativ cu 38,3 ± 3,5% cu dieta cu IG ridicată.
Media (± SEM) leptină serică de post zilnică ca procent din valorile inițiale. Leptina serică inițială pentru dieta cu indice glicemic ridicat (() a fost de 14,9 ± 1,7 mg/L, iar pentru dieta cu indice glicemic scăzut a fost de 13,4 ± 1,2 mg/L (NS; n = 10).
REE (Figura 4) a scăzut de la momentul inițial până la sfârșitul perioadei de restricție a energiei (media zilelor 5 și 6) cu 4,6% cu dieta cu conținut scăzut de IG (P = 0,03) și cu 10,5% cu dieta cu conținut ridicat de IG P = 0,005). REE medie a fost mai mică în zilele 5 și 6 ale dietei bogate în IG (7,38 ± 0,39 MJ/zi) decât în zilele 5 și 6 ale dietei cu IG scăzută (7,78 ± 0,36 MJ/zi; P = 0,04).
Cheltuielile energetice zilnice medii de odihnă (± SEM) zilnice cu dietele cu indice glicemic ridicat (○) și scăzut (◆) (n = 10).
Bilanțul de azot a fost pozitiv cu dieta cu conținut scăzut de IG și negativ cu dieta cu conținut ridicat de IG (25,7 ± 14,1 și −9,7 ± 5,5 mg N · kg −1 · d −1, respectiv; P = 0,06).
Aportul alimentar ad libitum în zilele 7 și 8 a fost cu 25% mai mare la dieta bogată în IG (17,0 ± 2,2 MJ) decât la dieta cu IG scăzută (13,5 ± 1,9 MJ; P = 0,009). Evaluarea subiectului a gustului alimentar ad libitum nu a diferit semnificativ între diete (7,2 ± 0,8 cu dieta bogată în IG și 6,3 ± 0,9 cu dieta cu IG scăzută).
DISCUŢIE
Dietele convenționale cu restricție energetică au rezultate foarte slabe pe termen lung în ceea ce privește pierderea în greutate (4), probabil pentru că aceste diete determină modificări ale foametei și metabolismului care promovează recâștigarea greutății (5). Rezultatele prezentului studiu sugerează că compoziția dietetică poate modifica adaptările fiziologice la restricția energetică, care ar putea avea relevanță pentru proiectarea de noi tratamente dietetice pentru obezitate.
Pierderea în greutate nu a diferit semnificativ între dieta bogată în IG și dieta cu IG scăzută, așa cum ar fi de așteptat din conținutul de energie identic al dietelor. Cu toate acestea, leptina serică a scăzut într-o măsură mai mare odată cu dieta cu conținut scăzut de IG. Această diferență poate fi explicată prin concentrațiile mai mici de insulină asociate acestei diete, deoarece insulina este secretar de leptină (31, 32) sau prin metabolizarea scăzută a glucozei adipocite (33). Această observație este în concordanță cu cea a lui Jenkins și colab (34), care au arătat o asociere pozitivă între consumul de carbohidrați și concentrația de leptină în timpul restricției de energie. Interesant este faptul că concentrația mai mică de leptină cu dieta cu IG scăzută a avut loc fără dovezi ale creșterii foametei (consumul de alimente ad libitum a fost de fapt mai mic cu această dietă), sugerând o îmbunătățire funcțională a rezistenței la leptină asociată cu obezitatea (35, 36). Este necesară o investigație suplimentară asupra semnificației acestui fenomen.
REE a scăzut într-o măsură mai mică cu IG scăzut decât cu dieta bogată în IG. În concordanță cu această constatare, Whitehead și colab. (37) au arătat că rata metabolică a somnului a scăzut mai puțin rapid cu o dietă bogată în proteine decât o dietă cu conținut scăzut de proteine. În studiul de față, dieta cu conținut scăzut de IG conținea mai multe proteine decât dieta bogată în IG. Observăm, totuși, că rezultatele actuale nu au fost cauzate de efectul termic crescut al proteinelor față de cel al altor macronutrienți, deoarece rata metabolică a fost măsurată la 10 ore după ultima masă. Conservarea REE în timpul restricționării energiei cu dieta cu conținut scăzut de IG, împreună cu diferențele de aport voluntar de hrană și de sațietate prezentate de noi și de alții (21-26), sugerează că dietele cu conținut scăzut de IG pot fi mai bine tolerate decât dietele cu conținut ridicat de GI.
În rezumat, acest studiu a arătat efectele benefice ale unei diete cu conținut scăzut de IG, cu conținut mediu de grăsimi, comparativ cu o dietă cu conținut ridicat de IG, cu conținut scăzut de grăsimi, în conformitate cu recomandările nutriționale actuale. Această constatare sugerează că răspunsurile hormonale și metabolice la restricția energetică - care implică concentrații de leptină, cheltuieli energetice, aport voluntar de alimente și echilibru de azot - pot fi afectate de compoziția dietetică. Sunt necesare cercetări suplimentare pentru a confirma aceste rezultate la alte populații și pe o perioadă mai lungă, pentru a determina care factori dietetici specifici mediază aceste evenimente fiziologice și pentru a examina efectele pe termen lung ale IG asupra reglării greutății corporale.
Mulțumiri
Mulțumim personalului de asistență medicală GCRC de la Children’s Hospital, Boston; personalul bucătăriei metabolice de la Brigham and Women’s Hospital, Boston; și Kate Donovan, fără de care studiul nu ar fi fost posibil.
Sprijinit de subvenții de la Fundația Charles H Hood, Fundația Endocrine Fellows, Knoll Pharmaceutical Company, Centrul General de Cercetare Clinică (M01 RR02172, M01 RR02635) și Institutul Național de Diabet și Boli Digestive și Renale (la DSL; 1K08 DK02440).
- Densitatea energetică dietetică este asociată pozitiv cu riscul de cancer pancreatic în Shanghaiul urban
- Obiceiuri de consum dietetic și antrenament controlat asupra compoziției și puterii corpului la femeile de elită
- Intervenții dietetice pentru restricția creșterii fetale - potențial terapeutic al azotatului dietetic
- Emulgatorii alimentari modifică direct compoziția microbiotei umane și expresia genei ex vivo
- Raporturile de grăsime dietetice și compoziția lipidică a membranei plasmatice hepatice SpringerLink